Dạng bài tập liên kết hóa học
PHẦN LIÊN KẾT HÓA HỌC
Bài tập 1: Vẽ sơ đồ mô tả sự hình thành liên kết ion trong phân tử potassium oxide (K2O).
Bài tập 2: Vẽ sơ đồ mô tả sự hình thành liên kết cộng hóa trị trong phân tử hydrogen chloride (HCl).
Bài tập 3: Hợp chất NaCl thuộc loại liên kết hóa học nào? Giải thích?
Bài tập 4: Kết quả thử nghiệm tính chất của hai chất A và B được trình bày ở bảng bên. Dựa vào bảng hãy cho biết, chất nào là chất cộng hoá trị, chất nào là chất ion?
Tính chất | Chất A | Chất B |
Thể (25oC) | Rắn | Lỏng |
Nhiệt độ sôi (oC) | 1500 | 64,7 |
Nhiệt độ nóng chảy (oC) | 770 | -97,6 |
Khả năng dẫn điện của dung dịch | Có | Không |
Bài tập 1: Sơ đồ mô tả sự hình thành liên kết ion trong phân tử potassium oxide (K2O)
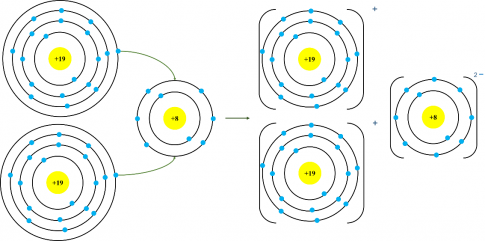
Bài tập 2: Sơ đồ mô tả sự hình thành liên kết cộng hóa trị trong phân tử hydrogen chloride (HCl)
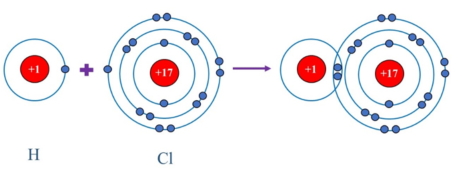
Bài tập 3: NaCl thuộc loại liên kết ion.
- Giải thích: Khi hình thành phân tử sodium chloride (NaCl), các nguyên tử đã có sự nhường và nhận electron như sau:
+ Nguyên tử natri (Na) nhường một electron ở lớp electron ngoài cùng cho nguyên tử chlorine (Cl) để tạo thành ion dương Na$^{+}$ có vỏ bền vững giống vỏ nguyên tử khí hiếm Ne.
+ Nguyên tử Cl nhận vào lớp electron ngoài cùng một electron của nguyên tử Na để tạo thành ion âm Cl$^{-}$ có vỏ bền vững giống vỏ nguyên từ khí hiếm Ar.
+ Hai ion được tạo thành mang điện tích ngược dấu hút nhau để hình thành liên kết ion trong phân tử muối ăn.
Bài tập 4: Vì hợp chất ion thường khó bay hơi, khó nóng chảy,... Chất cộng hoá trị thường có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
=> Chất A là chất ion; chất B là chất cộng hóa trị.
Xem toàn bộ: Đề cương ôn tập Hóa học 7 kết nối tri thức học kì 2

Bình luận