Giải bài 7 hóa học 10: Bảng tuần hoàn các nguyên tố hóa học
Bài học này trình bày nội dung: Bảng tuần hoàn các nguyên tố hóa học . Dựa vào cấu trúc SGK hóa học lớp 9, Tech12h sẽ tóm tắt lại hệ thống lý thuyết và hướng dẫn giải các bài tập 1 cách chi tiết, dễ hiểu. Hi vọng rằng, đây sẽ là tài liệu hữu ích giúp các em học tập tốt hơn.

A - Kiến thức trọng tâm
I. Nguyên tắc sắp xếp các nguyên tố hóa học
- Các nguyên tố được xếp theo chiều tăng dần của điện tích hạt nhân.
- Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng ngang (chu kì.
- Các nguyên tố có cùng số electron hóa trị (electron có khả năng tham gia vào quá trình hình thành liên kết hóa học) được xếp thành một cột (nhóm).
II. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
1. Ô nguyên tố
- Mỗi nguyên tố hóa học được xếp vào một ô của bảng gọi là ô nguyên tố. Các ô nguyên tố được đánh số thứ tự, số thứ tự chính là số điện tích Z của nguyên tố đó.
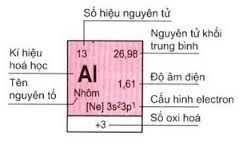
2.Chu kì
- Định nghĩa: Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tang dần.
- Số thứ tự của chu kì trùng với số lớp electron của nguyên tử của các nguyên tố trong chu kì đó.
- Có 7 chu kì
- Chu kì nhỏ: là các chu kì 1, 2, 3.
- Chu kì lớn: là các chu kì 4, 5, 6, 7.
3.Nhóm nguyên tố
- Định nghĩa: Nhóm là tập hợp các nguyên tố hóa học được xếp thành cột gồm các nguyên tố mà nguyên tử có cấu hình electron lớp ngoài cùng tương tự nhau, do đó tính chất hóa học gần giống nhau.
- Nguyên tử của các nguyên tố trong cùng một nhóm có số electron hóa trị bằng nhau và bằng số thứ tự của nhóm (trừ hai cột cuối của nhóm VIIIB)
- Các nhóm nguyên tố gồm nhóm A và nhóm B.
- Nhóm A bao gồm các nguyên tố s và nguyên tố p
- Nhóm B bao gồm các nguyên tố d và nguyên tố f

Bình luận