Dễ hiểu giải hóa học 10 kết nối bài 15: Phản ứng oxi hóa – khử
Giải dễ hiểu bài 15: Phản ứng oxi hóa – khử. Trình bày rất dễ hiểu, nên tiếp thu Hóa học 10 Kết nối dễ dàng. Học sinh nắm được kiến thức và biết suy rộng ra các bài tương tự. Thêm 1 dạng giải mới để mở rộng tư duy. Danh mục các bài giải trình bày phía dưới
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 15: PHẢN ỨNG OXI HÓA – KHỬ
MỞ ĐẦU
Trong lò luyện gang, xảy ra phản ứng oxi hóa – khử theo sơ đồ sau:
Fe2O3 + CO ![]() Fe + CO2
Fe + CO2
Về bản chất, phản ứng oxi hóa – khử là gì? Dựa vào dấu hiệu nào để nhận ra loại phản ứng đó? Làm thế nào để lập phương trình hóa học của phản ứng trên?
Giải nhanh:
- Bản chất là quá trình nhường và nhận electron
- Dựa vào sự thay đổi số oxi hóa
- Lập theo nguyên tắc: tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận.
I. SỐ OXI HÓA
Câu 1: Xác định số oxi hóa của nguyên tử Fe và S trong các chất sau:
a) Fe, FeO, Fe2O3, Fe(OH)3, Fe3O4.
b) S, H2S, SO2, SO3, H2SO4, Na2SO3.
Giải nhanh:
a) Lần lượt là 0, +2, +3, +8/3.
b) Lần lượt là 0, -2, +4, +6, +6, +4
II. CHẤT OXI HÓA, CHẤT KHỬ, PHẢN ỨNG OXI HÓA – KHỬ
Hoạt động: Xác định chất oxi hóa, chất khử
Chuẩn bị: đinh sắt, dung dịch CuSO4, dung dịch H2SO4 loãng, ống nghiệm.
Thực hiện:
Thí nghiệm 1: Cho đinh sắt vào ống nghiệm đựng dung dịch CuSO4
Thí nghiệm 2: Cho đinh sắt vào ống nghiệm đựng dung dịch H2SO4
Quan sát hiện tượng và thực hiện yêu cầu sau:
1. Viết quá trình oxi hóa, quá trình khử.
2. Xác định chất oxi hóa, chất khử trong hai phản ứng trên.
Giải nhanh:
1. - TN1: + Quá trình oxi hóa: Fe → Fe2+ + 2e
+ Quá trình khử: Cu2+ + 2e → Cu
- TN2: + Quá trình oxi hóa: Fe → Fe2+ + 2e
+ Quá trình khử: 2H2+ + 2e → H2
2. Chất khử: Fe. Chất oxi hóa: CuSO4 và H2SO4
Câu 2: Trong không khí ẩm, Fe(OH)2 màu trắng xanh chuyển dần sang Fe(OH)3 màu nâu đỏ:
Fe(OH)2 + O2 + H2O → Fe(OH)3
a) Hãy xác định các nguyên tử có sự thay đổi số oxi hóa.
b) Viết quá trình oxi hóa, quá trình khử.
c) Dùng mũi tên biểu diễn sự chuyển động electron từ chất khử sang chất oxi hóa.
Giải nhanh:
a) Fe và O.
b) Quá trình oxi hóa: Fe2+ → Fe3+ + 1e
Quá trình khử: O2 + 4e → 2O2-
c)
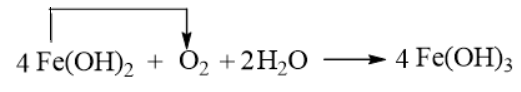
III. LẬP PHƯƠNG TRÌNH HOÁ HỌC CỦA PHẢN ỨNG OXI HOÁ – KHỬ
Câu 3: Xét các phản ứng hóa học xảy ra trong công nghiệp:
a) Al(OH)3 ![]() Al2O3 + H2O
Al2O3 + H2O
b) C + CO2 ![]() CO
CO
Phản ứng nào là phản ứng oxi hóa – khử? Lập phương trình hoá học của phản ứng oxi hóa – khử theo phương pháp thăng bằng electron.
Giải nhanh:
Phản ứng b. Chất khử: C; chất oxi hoá: CO2.
C → C+2 + 2e
C+4 + 2e → C+2
PTHH: C + CO2 ![]() 2CO
2CO
IV. PHẢN ỨNG OXI HOÁ – KHỬ TRONG THỰC TIỄN
Câu 4: Nêu một số phản ứng oxi hóa – khử có lợi và có hại trong thực tế.
Giải nhanh:
- Có lợi: đốt cháy nhiên liệu phục vụ hoạt động con người, quang hợp, hoạt động của pin điện tích trữ…
- Có hại: ăn mòn kim loại, ôi thiu thức ăn, tạo khí thải gây ô nhiễm…
Câu 5: Lập phương trình hóa học của các phản ứng trong quá trình sản xuất acid theo sơ đồ mục IV.3. Trong các phản ứng đó, phản ứng nào là phản ứng oxi hóa – khử?
Giải nhanh:
S + O2 ![]() SO2 (1)
SO2 (1)
4FeS2 + 11O2 ![]() 2Fe2O3 + 8SO2 (2)
2Fe2O3 + 8SO2 (2)
2SO2 + O2 ![]() 2SO3 (3)
2SO3 (3)
SO3 + H2O → H2SO4 (4)
Là các phản ứng (1), (2), (3).
Câu 6: Đèn xì oxygen – acetylene có cấu tạo gồm hai ống dẫn khí: một ống dẫn khí oxygen, một ống dẫn khí acetylene (Hình 15.1). Khi đèn hoạt động, hai khí này được trộn vào nhau để thực hiện phản ứng đốt cháy theo sơ đồ:
C2H2 + O2 ![]() CO2 + H2O
CO2 + H2O
Phản ứng tỏa nhiệt lớn, tạo ra ngọn lửa có nhiệt độ đạt đến 3000oC nên được dùng để hàn cắt kim loại.
Hãy xác định chất oxi hóa, chất khử và lập phương trình hóa học của phản ứng trên theo phương pháp thăng bằng electron.
Giải nhanh:
Quá trình khử: O2 + 4e → 2O2-
Quá trình oxi hoá: 2C-1 → 2C+4 + 10e
PTHH: 2C2H2 + 5O2 ![]() 4CO2 + 2H2O
4CO2 + 2H2O
Câu 7: Trong quá trình luyện gang thép từ quặng chứa Fe2O3, ban đầu không khí nóng được nén vào lò cao, đốt cháy hoàn toàn than cốc kèm theo tỏa nhiệt mạnh:
C + O2 ![]() CO2
CO2
Khi CO2 đi lên phía trên, gặp các lớp than cốc và bị khử thành CO:
CO2 + C ![]() CO
CO
Tiếp đó, khi CO khử Fe2O3 thành Fe theo phản ứng tổng quát:
Fe2O3 + CO ![]() Fe + CO2
Fe + CO2
Lập các phương trình hóa học ở trên, chỉ rõ chất oxi hóa, chất khử.
Giải nhanh:
Phản ứng 1: chất khử: C, chất oxi hoá: O2
C → C+2 + 2e
O2 + 4e → 2O2-
PTHH: 2C + O2 ![]() 2CO
2CO
Phản ứng 2: chất khử: C, chất oxi hoá: CO2
C → C+2 + 2e
C+4 + 2e → C+2
PTHH: C + CO2 ![]() 2CO
2CO
Phản ứng 3: chất khử: CO, chất oxi hoá: Fe2O3
2Fe+3 + 6e → 2Fe
C+2→ C+4 + 2e
PTHH: Fe2O3 + 3CO ![]() 2Fe + 3CO2
2Fe + 3CO2
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây

Bình luận