Dễ hiểu giải hóa học 10 kết nối bài 10: Quy tắc Octet
Giải dễ hiểu bài 10: Quy tắc Octet. Trình bày rất dễ hiểu, nên tiếp thu Hóa học 10 Kết nối dễ dàng. Học sinh nắm được kiến thức và biết suy rộng ra các bài tương tự. Thêm 1 dạng giải mới để mở rộng tư duy. Danh mục các bài giải trình bày phía dưới
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 10. QUY TẮC OCTET
MỞ ĐẦU
Khi các nguyên tử kết hợp với nhau tạo thành phân tử theo một tỉ lệ xác định, yếu tố nào quyết định tỉ lệ số nguyên tử của mỗi nguyên tố trong phân tử đó?
Giải nhanh:
Yếu tố: tỉ lệ số electron nhường, nhận hay góp chung của nguyên tử khi tham gia liên kết để hình thành phân tử.
I. KHÁI NIỆM LIÊN KẾT HÓA HỌC
Câu hỏi 1:Khi nguyên tử fluorine nhận thêm 1 electron thì ion tạo thành có cấu hình electron của nguyên tử nguyên tố nào?
Giải nhanh:
Cấu hình electron của nguyên tử Ne.
Câu hỏi 2:Để giảm năng lượng các nguyên tử kết hợp lại thành phân tử theo xu hướng nào?
Giải nhanh:
Theo xu hướng đạt tới cấu hình electron bền vững của khí hiếm.
II. QUY TẮC OCTET
Câu hỏi 3: Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử: F2, CCl4 và NF3.
Giải nhanh:
- Phân tử F2: nguyên tử fluorine có 7 electron hoá trị, mỗi nguyên tử fluorine cần thêm 1 electron để đạt cấu hình electron bão hoà theo quy tắc octet nên mỗi nguyên tử fluorine góp chung 1 electron.
Phân tử F2 được biểu diễn: ![]()
- Phân tử CCl4: nguyên tử chlorine có 7 electron hoá trị, mỗi nguyên tử chlorine cần thêm 1 electron để đạt cấu hình electron bão hoà, nguyên tử carbon có 4 electron hóa trị nên nguyên tử carbon sẽ góp chung với mỗi nguyên tử chlorine 1 electron.
Phân tử CCl4 được biểu diễn: 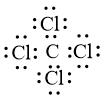
- Phân tử NF3: nguyên tử fluorine có 7 electron hoá trị, mỗi nguyên tử fluorine cần thêm 1 electron để đạt cấu hình electron bão hoà, nguyên tử nitrogen có 5 electron hóa trị nên nguyên tử nitrogen sẽ góp chung với mỗi nguyên tử fluorine 1 electron.
Phân tử NF3 được biểu diễn: 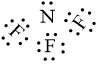
Câu hỏi 4:Phosphine là hợp chất hóa học giữa phosphorus với hydrogen, có công thức hóa học là PH3. Đây là chất khí không màu, có mùi tỏi, không bền, tự cháy trong không khí ở nhiệt độ thường và tạo thành khối phát sáng bay lơ lửng. Phosphine sinh ra khi phân hủy xác động, thực vật và thường xuyên xuất hiện trong thời tiết mưa phùn (hiện tương “ma trơi”).
Vận dụng quy tắc octet để giải thích sự tạo thành liên kết hóa học trong phosphine.
Giải nhanh:
- Nguyên tử hydrogen có 1 electron hoá trị, mỗi nguyên tử hydrogen cần thêm 1 electron để đạt cấu hình electron bão hoà. Nguyên tử phosphorus có 5 electron hóa trị còn thiếu 3 electron thì đạt octet nên nguyên tử phosphorus sẽ góp chung với mỗi nguyên hydrogen 1 electron.
- Phân tử PH3 được biểu diễn: 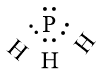
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây

Bình luận