Dạng bài tập cấu tạo nguyên tử
B. CÁC DẠNG BÀI TẬP
PHẦN NGUYÊN TỬ
Dạng 1: Cấu tạo nguyên tử
Bài tập 1: Điền từ vào chỗ trống
a) ………….. là hạt vô cùng nhỏ tạo nên các chất.
b) Nguyên tử gồm hạt nhân mang điện tích ………….. và vỏ nguyên tử mang điện tích …………...
c) Nguyên tử …………….. về điện nên tổng số hạt proton ………….. tổng số hạt electron.
Bài tập 2: Trong hạt nhân nguyên tử của aluminium có 13 proton. Em hãy xác định số electron trong nguyên tử, số lớp electron, số electron lớp ngoài cùng và vẽ sơ đồ cấu tạo nguyên tử aluminium.
Bài tập 3: Nguyên tử của một nguyên tố có tổng số các loại hạt là 58, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 18. Xác định số p, số n, số e của nguyên tử nguyên tố đó.
Bài tập 1:
a) Nguyên tử là hạt vô cùng nhỏ tạo nên các chất.
b) Nguyên tử gồm hạt nhân mang điện tích dương và vỏ nguyên tử mang điện tích âm
c) Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
Bài tập 2:
- Nguyên tử trung hòa về điện
=> số p = số e = 13
- Lớp electron trong cùng (gần hạt nhân nhất) có tối đa 2 e, các lớp electron khác chứa tối đa 8 e.
=> Số lớp electron là 3.
=> Số electron lớp ngoài cùng là: 13 - 2 - 8 = 3
Số p trong hạt nhân | số e trong nguyên tử | số lớp electron | số e lớp ngoài cùng |
13 | 13 | 3 | 3 |
Sơ đồ cấu tạo nguyên tử Aluminium:
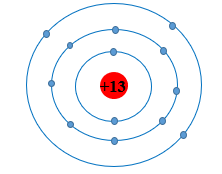
Bài tập 3:
Tổng số hạt = Số p + Số e + Số n = 58 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 18 hạt
→ Số p + Số e – Số n = 18 (2)
Trừ 2 vế (1) và (2) => Số n = 20
Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
→ Số p = Số e = $\frac{58-20}{2}$ = 19
Xem toàn bộ: Đề cương ôn tập Hóa học 7 cánh diều học kì 1

Bình luận