Slide bài giảng Hoá học 11 kết nối bài 21: Phenol
Slide điện tử bài 21: Phenol. Trình bày với các hiệu ứng hiện đại, hấp dẫn. Giúp học sinh hứng thú học bài. Học nhanh, nhớ lâu. Có tài liệu này, hiệu quả học tập của môn Hóa học 11 Kết nối tri thức sẽ khác biệt
Bạn chưa đủ điều kiện để xem được slide bài này. => Xem slide bài mẫu
Tóm lược nội dung
BÀI 21: PHENOL
HOẠT ĐỘNG KHỞI ĐỘNG
GV yêu cầu HS thảo luận và trả lời: Tìm hiểu về cách sử dụng lá trà xanh trong đời sống hàng ngày và nghiên cứu về thành phần EGCG có mặt trong lá trà xanh.
NỘI DUNG BÀI HỌC GỒM
- Tìm hiểu về khái niệm, đặc điểm cấu tạo phenol
+ Tìm hiểu khái niệm
+ Tìm hiểu đặc điểm cấu tạo của phenol
- Tìm hiểu tính chất vật lí phenol
- Luyện tập
- Vận dụng
HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
1. Tìm hiểu về khái niệm, đặc điểm cấu tạo phenol
Nhiệm vụ 1. Tìm hiểu khái niệm
GV đặt câu hỏi hướng dẫn học sinh tìm hiểu: Hãy giải thích khái niệm về phenol và đặt tên cho các hợp chất phenol với công thức cấu tạo sau:
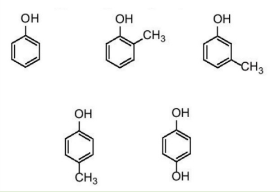
Nội dung ghi nhớ:
- Phenol là những hợp chất hữu cơ trong phân tử có chứa nhóm -OH liên kết trực tiếp với nguyên tử carbon của vòng benzene.
- Tên thông thường của một số phenol.
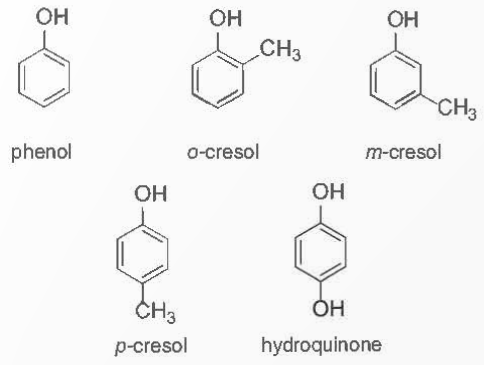
Nhiệm vụ 2. Tìm hiểu đặc điểm cấu tạo của phenol
GV đưa ra câu hỏi: Hãy mô tả cấu tạo của phenol và giải thích cách vòng benzen ảnh hưởng đến tính chất hóa học của nó. Dựa trên sự ảnh hưởng của vòng benzen, hãy dự đoán các tính chất hóa học của phenol.
Nội dung ghi nhớ:
* Mô hình phân tử:
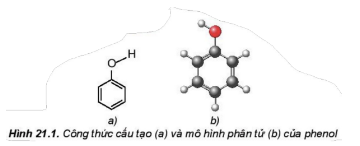
* Nhận xét tính chất của phenol:
- Trong phân tử phenol, do ảnh hưởng của vòng benzene nên liên kết O–H của phenol phân cực mạnh hơn so với alcohol
→ Phenol thể hiện tính acid yếu.
- Do có vòng benzene nên phenol có thể tham gia phản ứng thế nguyên tử hydrogen của vòng benzene.
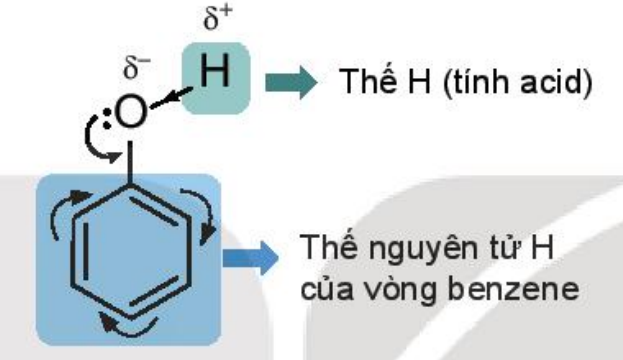
3. Tìm hiểu tính chất vật lí phenol
HS cùng thảo luận và trả lời câu hỏi:
Hãy mô tả các đặc điểm vật lý của phenol
Nội dung ghi nhớ:
- Ở điều kiện thường, phenol là chất rắn không màu, nóng chảy ở 43°C, sôi ở 181,8°C.
- Phenol ít tan trong nước ở điều kiện thường (độ tan trong nước ở 25°C: 8,42 g/100 g nước), tan nhiều khi đun nóng (tan vô hạn ở 66°C); tan tốt trong các dung môi hữu cơ như ethanol, ether và acetone.
- Phenol độc và có thể gây bỏng khi tiếp xúc với da nên phải cần thận khi sử dụng.
HOẠT ĐỘNG LUYỆN TẬP
Từ nội dung bài học,GV yêu cầu HS hoàn thành các bài tập trắc nghiệm sau:
Câu 1: Tên gọi của hợp chất có công thức cấu tạo là
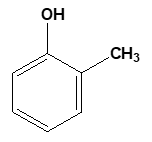
A. Phenol B. m-crezol C. o-crezol D. p-crezol
Câu 2: Cho hỗn hợp gồm 0,2 mol phenol và 0,3 mol ethylene glycol tác dụng với lượng dư potassium thu được V lít H2 ở đkc.Giá trị của V là?
A. 9,9160 B. 12,3950 C. 6,1975 D. 8,6765
Câu 3: Ảnh hưởng của nhóm OH đến vòng benzene được chứng minh bởi phản ứng nào?
A. Phản ứng của phenol với dung dịch NaOH
B. Phản ứng của phenol với nước Bromine
C. Phản ứng của phenol với Sodium
D. Phản ứng của phenol với formic aldehyde.
Câu 4: Nhận xét nào sau đây đúng?
A. Phenol có tính acid mạnh hơn ethanol
B. Phenol có tính acid yếu hơn ethanol
C. Phenol dễ tan trong nước hơn trong dung dịch NaOH
D. Phenol không có tính acid.
Câu 5: Cho 15,4 gam hỗn hợp o-crezol và ethanol tác dụng với Na dư thu được m gam muối và 2,479 lít khí H2. Giá trị của m là
A. 19,8 B. 18,9 C. 17,5 D. 15,7
HOẠT ĐỘNG VẬN DỤNG
Vận dụng kiến thức, GV yêu cầu HS hoàn thành bài tập sau:
Câu 1: Phenol đóng vai trò gì trong việc sản xuất thuốc kháng sinh và tác dụng của nó trong thuốc là gì?
Câu 2: Viết phương trình hóa học phản ứng giữa 4-methylphenol và nước bromine.
