Dạng bài tập Liên kết cộng hóa trị
Dạng 3: Liên kết cộng hóa trị
Bài tập 1: Dựa vào giá trị độ âm điện, liên kết giữa nguyên tử H và Cl thuộc loại liên kết gì?
Bài tập 2: Cho biết năng lượng liên kết của O – H là: 464 kJ mol−1. Tổng năng lượng liên kết trong phân tử H2O là bao nhiêu?
Bài tập 3: Liên kết giữa O với C trong phân tử CO2 có số cặp electron chung là
Bài tập 1:
Có χ(H) = 2,2 và χ(Cl) = 3,16
Nên x= x(Cl)−x(H)=3,16−2,2=0.96
Mà 0,4 ≤ 0,96 < 1,7 ⇒ liên kết giữa nguyên tử H và Cl thuộc loại liên kết cộng hóa trị có cực.
Bài tập 2:
Trong phân tử H2O có hai liên kết O – H nên tổng năng lượng liên kết trong phân tử H2O là: 464.2 = 928 (kJ mol−1)
Bài tập 3:
O (Z = 8): [He]2s22p4 ⇒ có 6 electron lớp ngoài cùng ⇒ xu hướng nhận 2 electron để đạt cấu hình electron bền vững ⇒ góp 2 electron.
C (Z = 6): [He]2s22p2 ⇒ có 4 electron lớp ngoài cùng ⇒ xu hướng nhận 4 electron để đạt cấu hình electron bền vững ⇒ góp 4 electron.
Công thức electron của phân tử CO2:
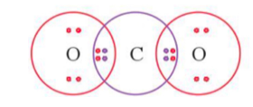
Vậy giữa 2 nguyên tử O và C có 2 cặp electron dùng chung.
Xem toàn bộ: Đề cương ôn tập Hóa học 10 cánh diều học kì 1 (P3)

Bình luận