Trắc nghiệm Hóa học 12 Cánh diều bài 11: Nguồn điện hóa học (P2)
Bộ câu hỏi và Trắc nghiệm Hóa học 12 Cánh diều bài 11: Nguồn điện hóa học (P2) có đáp án. Học sinh luyện tập bằng cách chọn đáp án của mình trong từng câu hỏi. Dưới cùng của bài trắc nghiệm, có phần xem kết quả để so sánh kết quả bài làm của mình. Kéo xuống dưới để bắt đầu.
TRẮC NGHIỆM
Câu 1: Một pin Galvani Mg-Cu có sức điện động chuẩn bằng 2,696 V. Biết
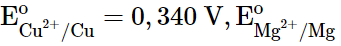 bằng
bằng
- A. 2,300 V.
- B. -2,356 V.
- C. 3,260 V.
- D. -3,260 V.
Câu 2: Cho Câu 2: Cho ![]() vvà
vvà ![]() Sức điện động chuẩn của một pin Galvani được tạo thành từ hai cặp oxi hoá – khử Zn2+/Zn và Fe2+/Fe là
Sức điện động chuẩn của một pin Galvani được tạo thành từ hai cặp oxi hoá – khử Zn2+/Zn và Fe2+/Fe là
- A. -0,323 V.
- B. -1,170 V.
C. 0,323 V.
- D. 1,170 V.
Câu 3: Trong quá trình hoạt động của pin điện Ni - Cu, quá trình xảy ra ở anode là
- A. Ni2+ + 2e → Ni.
- B. Cu → Cu2+ + 2e.
- C. Cu2+ + 2e → Cu.
D. Ni → Ni2+ + 2e.
Câu 4: Trong pin điện hoá, quá trình khử
- A. xảy ra ở cực âm.
B. xảy ra ở cực dương.
- C. xảy ra ở cực âm và cực dương.
- D. không xảy ra ở cả cực âm và cực dương.
Câu 5: Một pin Galvani được cấu tạo bởi hai cặp oxi hoá – khử sau:
(1) Ag+ + 1e → Ag = 0,799 V
(2) Ni2+ + 2e → Ni = -0,257 V
Khi pin làm việc ở điều kiện chuẩn, nhận định nào sau đây là đúng?
- A. Ag được tạo ra ở cực dương, Ni được tạo ra ở cực âm.
B. Ag được tạo ra ở cực dương, Ni2+ được tạo ra ở cực âm.
- C. Ag+ được tạo ra ở cực âm và Ni được tạo ra ở cực dương.
- D. Ag được tạo ra ở cực âm và Ni2+ được tạo ra ở cực dương.
Câu 6: Phản ứng hoá học xảy ra trong pin điện hoá Sn - Cu:
Sn + Cu2+ → Sn2+ + Cu
Trong quá trình hoạt động của pin điện hoá, nhận định nào sau đây là đúng?
- A. Khối lượng của điện cực Sn tăng.
B. Nồng độ Sn2+ trong dung dịch tăng.
- C. Khối lượng của điện cực Cu giảm.
- D. Nồng độ Cu2+ trong dung dịch tăng.
Câu 7: Trong quá trình hoạt động của pin điện Cu - Ag, điện cực đồng
- A. là điện cực dương.
- B. là cathode.
C. là điện cực bị giảm dần khối lượng.
- D. là nơi xảy ra quá trình khử.
Câu 8: Một pin điện hoá có điện cực Zn nhúng trong dung dịch ZnSO4 vả điện cực Cu nhúng trong dung dịch CuSO4. Sau một thời gian pin đó phóng điện thì
A. khối lượng điện cực Zn giảm còn khối lượng điện cực Cu tăng.
- B. khối lượng điện cực Zn tăng còn khối lượng điện cực Cu giảm.
- C. khối lượng cả hai điện cực Zn và Cu đều tăng.
- D. khối lượng cả hai điện cực Zn và Cu đều giảm.
Câu 9: Khi pin Galvani Zn – Cu hoạt động thì nồng độ
A. Cu2+ giảm, Zn2+ tăng.
- B. Cu2+ giảm, Zn2+ giảm.
- C. Cu2+ tăng, Zn2+ tăng.
- D. Cu2+ tăng, Zn2+ giảm.
Câu 10: Cho một pin điện hóa được tạo bởi các cặp oxi hóa – khử Fe2+/Fe và Ag+/Ag ở điều kiện chuẩn. Quá trình xảy ra ở cực âm khi pin hoạt động là:
A. Fe → Fe2+ + 2e
- B. Fe2+ + 2e → Fe
- C. Ag+ + 1e → Ag
- D. Ag → Ag+ + 1e
Câu 11: Trong pin Galvani, nếu rút cầu muối ra thì hiệu điện thế giữa hai điện cực của pin sẽ
A. bằng 0.
- B. không thay đổi.
- C. tăng từ từ.
- D. giảm từ từ.
Câu 12: Phát biểu nào sau đây là không đúng khi nói về pin nhiên liệu?
A. Hiệu suất chuyển hoá từ nhiên liệu sang điện năng cao hơn các pin Galvani.
- B. Pin nhiên liệu hydrogen không tạo ra các sản phẩm gây ô nhiễm môi trường.
- C. Hoạt động liên tục khi còn chất phản ứng.
- D. Giá thành thấp vì có cấu tạo đơn giản.
Câu 13: Trong pin Galvani, thành phần nào dưới đây không phải là một phần cấu tạo nhất định phải có trong pin?
- A. Điện cực dương.
- B. Điện cực âm.
- C. Cầu muối.
D. Dây dẫn điện.
Câu 14: Cho các thế điện cực chuẩn của các cặp oxi hoá- khử: E0Mg2+/Mg = -2,37V; E0Fe2+/Fe = -0,44V ; E0Fe3+/Fe2+ = + 0,77 V ; E0Cu2+/Cu = +0,34V và E0Ag+/Ag = +0,8 V. Pin điện hoá có suất điện động chuẩn lớn nhất là:
- A. Fe-Cu
B. Mg-Ag
- C. Mg-Fe
- D. Cu-Ag
Câu 15: Cho các cặp oxi hoá - khử và thế điện cực chuẩn tương ứng:
+0,34 -0,762 -0,44 +0,799
| Cặp oxi hoá-khử | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Ag +/Ag |
| Thế điện cực chuẩn (V) |
Pin có sức điện động lớn nhất là
- A. Pin Zn -Cu.
- B. Pin Fe-Cu.
- C. Pin Cu-Ag.
D. Pin Fe-Ag.
Câu 16: Tính thế điện cực chuẩn của cặp oxi hóa - khử sau:
Eo(Zn2+/Zn), biết rằng Eopin(Zn-Cu) = 1,10V và Eo(Cu2+/Cu) = +0,34V.
A. -0,76 V.
- B. 0,42 V.
- C. - 0,38.
- D. 0,24 V.
Câu 17: Sức điện động chuẩn của pin điện hoá H2–Cu (gồm hai điện cực ứng với hai cặp oxi hoá – khử là 2H+/H2 và Cu2+/Cu) đo được bằng vôn kế có điện trở vô cùng lớn là 0,340V. Từ đó, xác định được thế điện cực chuẩn của cặp Cu2+/ Cu là:
- A. -0,340V.
- B. 0,000V.
- C. 0,680 V.
D. +0,340 V.
Câu 18: Có pin điện hóa được tạo thành từ những cặp oxi hóa - khử sau: Fe2+/Fe và Ag+/Ag. Hãy tính suất điện động của mỗi pin điện hóa, biết rằng: E0Ag+/Ag = + 0,8V; E0Fe2+/Fe = -0,44V.
- A. 0,36V.
- B. -1,24V.
C. 1,24V.
- D. -0,36V.
Xem toàn bộ: Giải Hóa học 12 Cánh diều bài 11: Nguồn điện hóa học
Nội dung quan tâm khác
Giải bài tập những môn khác
Môn học lớp 12 KNTT
5 phút giải toán 12 KNTT
5 phút soạn bài văn 12 KNTT
Văn mẫu 12 KNTT
5 phút giải vật lí 12 KNTT
5 phút giải hoá học 12 KNTT
5 phút giải sinh học 12 KNTT
5 phút giải KTPL 12 KNTT
5 phút giải lịch sử 12 KNTT
5 phút giải địa lí 12 KNTT
5 phút giải CN lâm nghiệp 12 KNTT
5 phút giải CN điện - điện tử 12 KNTT
5 phút giải THUD12 KNTT
5 phút giải KHMT12 KNTT
5 phút giải HĐTN 12 KNTT
5 phút giải ANQP 12 KNTT
Môn học lớp 12 CTST
5 phút giải toán 12 CTST
5 phút soạn bài văn 12 CTST
Văn mẫu 12 CTST
5 phút giải vật lí 12 CTST
5 phút giải hoá học 12 CTST
5 phút giải sinh học 12 CTST
5 phút giải KTPL 12 CTST
5 phút giải lịch sử 12 CTST
5 phút giải địa lí 12 CTST
5 phút giải THUD 12 CTST
5 phút giải KHMT 12 CTST
5 phút giải HĐTN 12 bản 1 CTST
5 phút giải HĐTN 12 bản 2 CTST
Môn học lớp 12 cánh diều
5 phút giải toán 12 CD
5 phút soạn bài văn 12 CD
Văn mẫu 12 CD
5 phút giải vật lí 12 CD
5 phút giải hoá học 12 CD
5 phút giải sinh học 12 CD
5 phút giải KTPL 12 CD
5 phút giải lịch sử 12 CD
5 phút giải địa lí 12 CD
5 phút giải CN lâm nghiệp 12 CD
5 phút giải CN điện - điện tử 12 CD
5 phút giải THUD 12 CD
5 phút giải KHMT 12 CD
5 phút giải HĐTN 12 CD
5 phút giải ANQP 12 CD
Giải chuyên đề học tập lớp 12 kết nối tri thức
Giải chuyên đề Ngữ văn 12 Kết nối tri thức
Giải chuyên đề Toán 12 Kết nối tri thức
Giải chuyên đề Vật lí 12 Kết nối tri thức
Giải chuyên đề Hóa học 12 Kết nối tri thức
Giải chuyên đề Sinh học 12 Kết nối tri thức
Giải chuyên đề Kinh tế pháp luật 12 Kết nối tri thức
Giải chuyên đề Lịch sử 12 Kết nối tri thức
Giải chuyên đề Địa lí 12 Kết nối tri thức
Giải chuyên đề Tin học ứng dụng 12 Kết nối tri thức
Giải chuyên đề Khoa học máy tính 12 Kết nối tri thức
Giải chuyên đề Công nghệ 12 Điện - điện tử Kết nối tri thức
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Kết nối tri thức
Giải chuyên đề học tập lớp 12 chân trời sáng tạo
Giải chuyên đề Ngữ văn 12 Chân trời sáng tạo
Giải chuyên đề Toán 12 Chân trời sáng tạo
Giải chuyên đề Vật lí 12 Chân trời sáng tạo
Giải chuyên đề Hóa học 12 Chân trời sáng tạo
Giải chuyên đề Sinh học 12 Chân trời sáng tạo
Giải chuyên đề Kinh tế pháp luật 12 Chân trời sáng tạo
Giải chuyên đề Lịch sử 12 Chân trời sáng tạo
Giải chuyên đề Địa lí 12 Chân trời sáng tạo
Giải chuyên đề Tin học ứng dụng 12 Chân trời sáng tạo
Giải chuyên đề Khoa học máy tính 12 Chân trời sáng tạo
Giải chuyên đề Công nghệ 12 Điện - điện tử Chân trời sáng tạo
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Chân trời sáng tạo
Giải chuyên đề học tập lớp 12 cánh diều
Giải chuyên đề Ngữ văn 12 Cánh diều
Giải chuyên đề Toán 12 Cánh diều
Giải chuyên đề Vật lí 12 Cánh diều
Giải chuyên đề Hóa học 12 Cánh diều
Giải chuyên đề Sinh học 12 Cánh diều
Giải chuyên đề Kinh tế pháp luật 12 Cánh diều
Giải chuyên đề Lịch sử 12 Cánh diều
Giải chuyên đề Địa lí 12 Cánh diều
Giải chuyên đề Tin học ứng dụng 12 Cánh diều
Giải chuyên đề Khoa học máy tính 12 Cánh diều
Giải chuyên đề Công nghệ 12 Điện - điện tử Cánh diều
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Cánh diều

Bình luận