Đề số 1: Đề kiểm tra KHTN 8 Cánh diều bài 3 Định luật bảo toàn khối lượng. Phương trình hoá học
I. DẠNG 1 – ĐỀ KIỂM TRA TRẮC NGHIỆM
ĐỀ 1
(Chọn chữ cái trước câu trả lời đúng nhất.)
Câu 1: Giả sử có phản ứng giữa A + B tạo ra C + D. Áp dụng định luật bảo toàn khối lượng ta có:
- A. mA + mB = mC + mD.
- B. mC = mA + mB + mD.
- C. mA + mC = mB + mD.
- D. mB + mC = mA + mD.
Câu 2: “Trong phản ứng hóa học, tổng số nguyên tử mỗi nguyên tố có trong các chất tham gia phản ứng luôn … tổng số nguyên tử của nguyên tố đó trong các chất sản phẩm”
Trong dấu “…” là
- A. Lớn hơn.
B. Nhỏ hơn.
C. Bằng.
D. Tỉ lệ thuận với.
Câu 3: Nhận định nào sau đây sai
- A. Hệ số viết ngang với kí hiệu của các chất.
- B. Phải thay đổi chỉ số của các công thức hóa học đầu bài đã cho.
- C. Nếu trong phản ứng có n chất, khi biết khối lượng đã tham gia và tạo thành của (n-1) chất, ta sẽ xác định được khối lượng chất còn lại.
- D. Số nguyên tử mỗi nguyên tố ở 2 vế phương trình là bằng nhau.
Câu 4: Cho các phát biểu sau, phát biểu sai là
- A. Trong một phản ứng hóa học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng.
- B. Trong phản ứng hóa học diễn ra sự thay đổi liên kết giữa các nguyên tử.
- C. Trong phản ứng hóa học, sự thay đổi liên kết hóa học chỉ liên quan đến electron.
- D. Trong phản ứng hóa học, khối lượng sản phẩm thu được phải lớn hơn khối lượng chất tham gia.
Câu 5: Hình dưới mô tả thí nghiệm phản ứng của BaCl2 và Na2SO4. Trong cốc 1 đựng BaCl2 và cốc 2 đựng Na2SO4, lúc này cân ở trạng thái cân bằng.
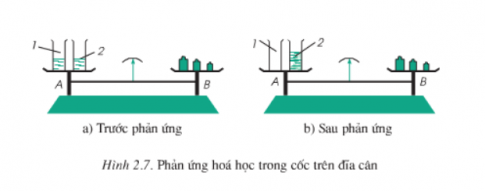
Tiếp theo ta tiến hành đổ cốc 1 vào cốc 2 thì thấy có hiện tượng xuất hiện kết tủa. Sơ đồ phản ứng: BaCl2 + Na2SO4 → NaCl + BaSO4 ↓. Sau khi phản ứng kết thúc, kim đồng hồ lệch về hướng nào?
- A. Kim sẽ lệch về phía quả cân
- B. Kim sẽ lệch về phía cốc 1 và cốc 2
- C. Kim sẽ nằm cân bằng ở giữa không lệch về bên nào
- D. Không thể xác định được.
Câu 6: Cho 13 gam Zn tác dụng với dung dịch HCl thu được 27,2 gam ZnCl2 và 0,4 gam khí H2. Tính khối lượng của HCl đã phản ứng.
- A. 12 gam
B. 14,6 gam
C. 15,2 gam
D. 16 gam
Câu 7: Khử hoàn toàn 12 gam CuO bằng 9 gam khí CO thu được 6 gam CO2 và đồng. Tính khối lượng của đồng.
A. 14 gam
B. 15 gam
C. 16 gam
D. 17 gam
Câu 8: Đốt cháy 6,4 gam sulfur trong không khí thu được 12,8 gam SO2. Tính khối lượng oxygen đã phản ứng.
- A. 6,4 gam
- B. 4,8 gam
- C. 5,2 gam
- D. 5,4 gam
Câu 9: Đá đôlômit là hỗn hợp của 2 chất CaCO3 và MgCO3. Khi nung nóng đá đôlômit sẽ tạo ra 2 chất oxit là Calci oxide (CaO) và magnessium oxide (MgO), thu được khí carbon dioxide. Nếu nung đá đôlômit, khối lượng của khí cacbon đioxit và hợp chất 2 oxit trên khi thu được lần lượt là 88kg và 104kg thì cần phải đốt bao nhiêu đá?
- A. 150 kg
- B. 162 kg
- C. 192 kg
- D. Kết quả khác
Câu 10: Cho sơ đồ phản ứng:
Fe(OH)y + H2SO4 → Fex(SO4)y + H2O.
x, y có thể lần lượt là ? (biết x ≠ y)
- A. 2 và 3
- B. 2 và 1
- C. 1 và 2
- D. 3 và 2
(Mỗi câu đúng tương ứng với 1 điểm)
Câu hỏi | Câu 1 | Câu 2 | Câu 3 | Câu 4 | Câu 5 |
Đáp án | A | C | B | D | C |
Câu hỏi | Câu 6 | Câu 7 | Câu 8 | Câu 9 | Câu 10 |
Đáp án | B | B | A | C | A |

Bình luận