Siêu nhanh giải bài 6 Khoa học tự nhiên 7 Chân trời sáng tạo
Giải siêu nhanh bài 6 Khoa học tự nhiên 7 Chân trời sáng tạo. Giải siêu nhanh Khoa học tự nhiên 7 Chân trời sáng tạo. Những phần nào có thể rút gọn, lược bỏ và tóm gọn. Đều được áp dụng vào bài giải này. Thêm cách giải mới để học sinh lựa chọn. Để tìm ra phong cách học Khoa học tự nhiên 7 Chân trời sáng tạo phù hợp với mình.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 6 GIỚI THIỆU VỀ LIÊN KẾT HOÁ HỌC
1. VỎ NGUYÊN TỬ KHÍ HIẾM
Câu 1: Trừ helium, vỏ nguyên tử của các nguyên tố còn lại ở Hình 6.1 có những điểm giống và khác nhau gì?
Trả lời:
Giống: Đều có 8 electron ở lớp ngoài cùng.
Khác: ở số lớp electron và số electron có trong mỗi lớp.
Ne: 2 lớp
Ar: 3 lớp
Kr: 4 lớp
Xe: 5 lớp
2. LIÊN KẾT ION
Câu 2: Quan sát Hình 6.2, em hãy mô tả sự tạo thành ion sodium, ion magnesium. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
Trả lời:
(1) Sự tạo thành:
Ion sodium: sodium nhường 1 electron lớp ngoài cùng và tạo thành ion dương tương ứng.
Ion magnesium: magnesium nhường 2 electron lớp ngoài cùng và tạo thành ion dương tương ứng.
(2) 8 electron.
(3) Neon (Ne).
Luyện tập: Hãy xác định vị trí của alumnium trong bảng tuần hoàn và vẽ sơ đồ tạo thành ion alumnium từ nguyên tử alumnium.
Trả lời:
Ô số 13, nhóm IIIA, chu kì 3.
Sơ đồ tạo thành ion aluminium từ nguyên tử aluminium:
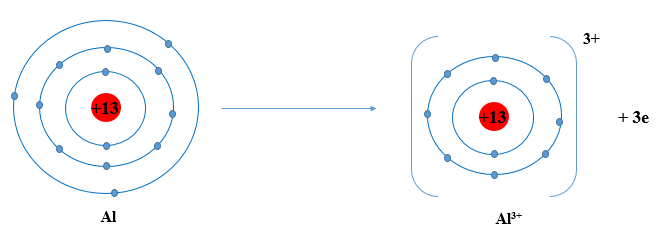
Câu 3: Quan sát Hình 6.3, em hãy mô tả sự tạo thành ion chloride, ion oxide. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
Trả lời:
(1) Sự tạo thành:
Ion chloride: chloride nhận 1 electron từ nguyên tử kim loại và tạo thành ion âm tương ứng.
Ion oxide: oxide nhận 2 electron từ nguyên tử kim loại và tạo thành ion âm tương ứng.
(2) 8 electron.
(3) Argon (Ar).
(4) Neon (Ne).
Luyện tập: Xác định vị trí của sunfur trong bảng tuần hoàn và vẽ sơ đồ tạo thành ion sunfur (S2-) từ nguyên tử sunfur.
Trả lời:
Ô số 16, nhóm VIA, chu kì 3.
Sơ đồ tạo thành ion sunfur từ nguyên tử sunfur:
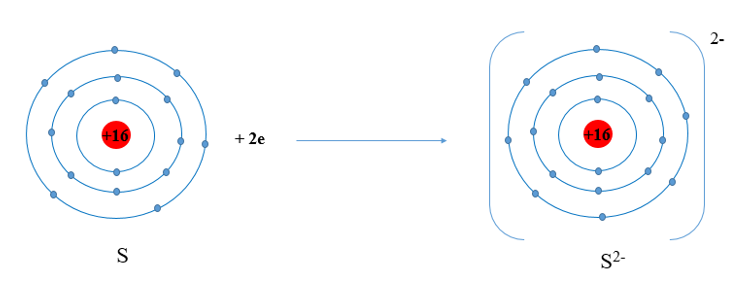
Câu 4: Quan sát Hình 6.4a, em hãy mô tả quá trình tạo thành liên kết ion trong phân tử sodium chloride. Nêu một số ứng dụng của sodium chloride trong đời sống.
Trả lời:
(1) Quá trình:
Sodium kết hợp với chlorine sẽ nhường 1 electron tạo thành ion dương, chlorine nhận 1 electron tạo thành ion âm.
Ion dương và ion âm mang điện tích trái dấu nên hút nhau, tạo thành liên kết ion trong phân tử sodium chloride.
(2) Ứng dụng:
Trong công nghiệp:
Sản xuất giấy, bột giấy, thuốc nhuộm.
Dệt may và sản xuất vải, xà phòng, chất tẩy rửa.
Là nguyên liệu ban đầu để sản xuất chlorine và xút, sử dụng trong hầu hết các ngành công nghiệp.
...
Trong nông nghiệp, chăn nuôi
Cân bằng sinh lý trong cơ thể giúp gia súc, gia cầm, giảm bệnh tật.
Phân loại hạt giống theo trọng lượng, cung cấp thêm vi lượng khi trộn với các loại phân hữu cơ để tăng hiệu quả của phân bón.
Trong thực phẩm
Là thành phần chính trong muối ăn và được sử dụng phổ biến.
Bảo quản thực phẩm: ướp thực phẩm sống như tôm, cá,…
Khử mùi thực phẩm, giữ cho trái cây không bị thâm.
Tăng hương vị, kiểm soát quá trình lên men của thực phẩm.
Trong y tế: sát trùng vết thương, cung cấp muối khoáng cho cơ thể thiếu nước, thanh lọc cơ thể, làm đẹp da, chữa viêm họng, làm trắng răng,...
Trong đời sống gia đình: rửa ống thoát, tẩy rửa các vết bẩn, vết ố,…
Luyện tập: Hãy vẽ sơ đồ mô tả quá trình tạo thành liên kết ion trong phân tử hợp chất magnesium oxide.
Trả lời:
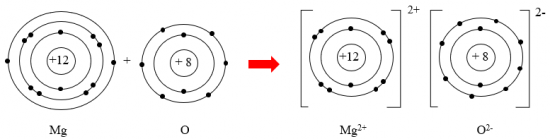
Vận dụng : Cancium chloride có nhiều ứng dụng trong đời sống. Tìm hiểu qua sách báo và internet em hãy cho biết một số ứng dụng của chất này . Vẽ sơ đồ cấu tạo trong phân tử cancium chloride
Trả lời:
Bào chế thuốc tiêm điều trị bệnh tĩnh mạch, bảo vệ cơ tim khi bị tăng kali máu, tránh các cơn đau tim cấp tính, bảo vệ và giúp tim nhanh phục hồi sau phẫu thuật
Phụ gia thực phẩm
Là chất điện giải trong một số nước uống…
3. LIÊN KẾT CỘNG HOÁ TRỊ
Câu 5: Dựa vào bảng tuần hoàn, hãy chỉ ra nguyên tố khí hiếm gần nhất của hydrogen và oxygen. Để có lớp electron ngoài cùng giống nguyên tố khí hiếm gần nhất, nguyên tử hydrogen và oxygen có xu hướng gì?
Trả lời:
(1)
Helium (He).
Neon (Ne).
(2) Góp chung electron.
Câu 6: Dựa vào các Hình 6.5, 6.6 và 6.7, em hãy cho biết số electron lớp ngoài cùng của mỗi nguyên tử trong phân tử hydrogen và oxygen là bao nhiêu? Khi đó, lớp electron ngoài cùng của nguyên tử hydrogen và nguyên tử oxygen sẽ giống với khí hiếm nào?
Trả lời:
Hydrogen: 2, giống helium (He).
Oxygen: 8, giống neon (Ne).
Câu 7: Em hãy mô tả quá trình tạo thành liên kết cộng hoá trị trong phân tử hydrogen và oxygen.
Trả lời:
Phân tử hydrogen: hai nguyên tử hydrogen có xu hướng góp chung 1 electron, hình thành liên kết cộng hoá trị.
Phân tử oxygen: hai nguyên tử oxygen có xu hướng góp chung 2 electron, hình thành liên kết cộng hoá trị.
Câu 8: Quan sát Hình 6.8, em hãy cho biết số electron dùng chung của nguyên tử H và nguyên tử O. Trong phân tử nước, số electron lớp ngoài cùng của O và H là bao nhiêu và giống với khí hiếm nào?
Trả lời:
(1)
H: 2 electron.
O: 4 electron.
(2) Helium (He).
(3) Neon (Ne).
Câu 9: Em hãy mô tả quá trình tạo thành liên kết cộng quá trị trong phân tử nước.
Trả lời:
Hai nguyên tử hydrogen gộp chung 1 electron của mỗi nguyên tử với nguyên tử oxygen để hình thành liên kết cộng hoá trị.
Cùng lúc, nguyên tử oxygen cũng gộp 2 electron cho mỗi nguyên tử hydrgen để hình thành liên kết cộng hoá trị.
Vận dụng : Khí methane là thành phần chính của khí thiên nhiên và khí mỏ dầu. Khí này còn được tạo ra từ hầm biogas. Methane là nguồn nhiên liệu quan trọng trong đời sống và có nhiều ứng dụng trong công nghiệp . Hãy vẽ sơ đồ hình thành liên kết trong phân tử methane và liệt kê một số ứng dụng của của nó thông qua tìm hiểu mạng internet, báo, đài...
Luyện tập: Vẽ sơ đồ hình thành liên kết cộng hoá trị trong các phân tử sau:
Trả lời:
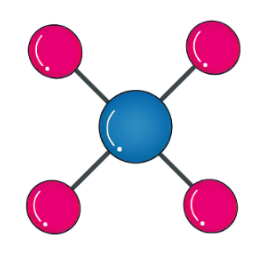
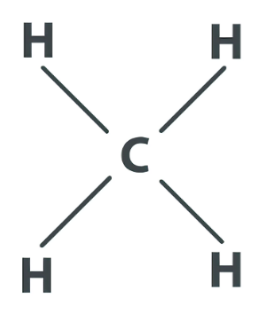
Ứng dụng methane: hóa học công nghiệp (làm nhiên liệu, khí tự nhiên, khí tự nhiên hóa lỏng) và nó được vận chuyển dưới dạng chất lỏng được làm lạnh.
Sơ đồ chlorine và ammonia:
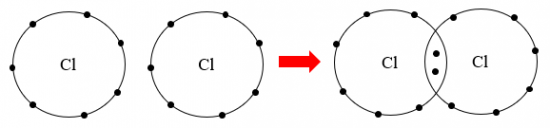
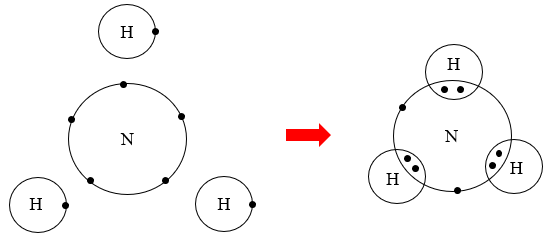
4. CHẤT ION, CHẤT CỘNG HOÁ TRỊ
Câu 10: Cho biết mỗi phân tử của chất trong Hình 6.9 được tạo bởi các ion nào? Ở điều kiện thường, các chất này ở thể gì?
Trả lời:
Sodium chloride: ion Na+ và Cl-. Ở điều kiện thường, sodium chloride ở thể rắn.
Calcium chloride: ion Ca2+ và Cl-. Ở điều kiện thường, calcium chloride ở thể rắn.
Magnesium oxide: ion Mg2+ và O2-. Ở điều kiện thường, magnesium oxide ở thể rắn
Câu 11: Quan sát và cho biết thể của các chất có trong Hình 6.10.
Trả lời:
Đường tinh luyện: rắn
Ethanol: lỏng
Carbon dioxide: khí.
Câu 12: Nếu một số ví dụ về chất cộng hoá trị và cho biết thể của chúng ở điều kiện thường.
Trả lời:
Nước: lỏng.
Chlorine, ammonia: khí.
Khói của núi lửa ngầm phun trào dưới biển có chứa một số chất như: hơi nước, sodium chloride, carbon dioxide, sulfur dioxide.
a) Hãy cho biết chất nào là hợp chất ion, chất nào là hợp chất hoá trị?
b) Nguyên tử của nguyên tố nào trong các chất trên có số electron lớp ngoài cùng nhiều nhất?
Trả lời:
a)
Ion: sodium chloride, potassium chloride.
Hoá trị: hơi nước, carbon dioxide, sulfur dioxide.
b)
Hơi nước: H có 1e, O có 6e.
Sodium chloride: Na có 1e, ử Cl có 7e.
Potassium chloride: K có 1e, Cl có 7e.
Cacbon dioxide: C có 4e, O có 6e.
Sulfur dioxide: S có 6e, O có 6e.
=> chlorine.
5. MỘT SỐ TÍNH CHẤT CỦA CHẤT ION VÀ CHẤT CỘNG HOÁ TRỊ
Câu 13: Quan sát thí nghiệm 1 (Hình 6.11, 6.12) và đánh dấu V để hoàn thành bảng sau:
Trả lời:
Tính chất | Muối | Đường |
Tan trong nước | V | V |
Dẫn điện được | V |
Câu 14: Quan sát thí nghiệm 3 (Hình 6.13), cho biết muối hay đường bền nhiệt hơn. Ở ống nghiệm nào có sự tạo thành chất mới?
Trả lời:
Muối bền nhiệt hơn.
Ở ống nghiệm của đường
Luyện tập: Kết quả thứ nghiệm tính chất của 2 chất A và B được trình bày ở bảng bên. Em hãy cho biết chất nào là chất cộng hoá trị, chất nào là chất ion?
Trả lời:
Chất A là chất ion, B là chất hoá trị
Vận dụng : Khi cơ thể bị mất nước do tiêu chảy, nôn mửa,... người ta thường cho bệnh nhân uống dung dịch oresol. Tìm hiểu qua sách báo và internet, hãy cho biết thành phần của oresol có các loại chất nào (chất ion, chất cộng hóa trị ). Trong trường hợp không có oresol, có thể thay bằng cách nào khác không ? Giải thích
Trả lời:
Muối và đường. Là các chất ion ( muối ), cộng hóa trị (đường )
Bằng cách cho uống nước chanh muối pha loãng
BÀI TẬP
Câu 1: Hãy vẽ sơ đồ và mô tả quá trình tạo thành liên kế trong phân tử sodium oxide (hình bên).
Trả lời:
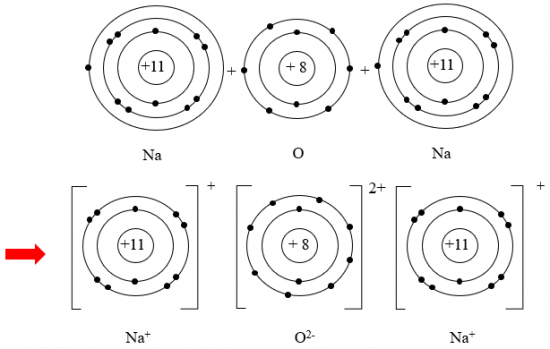
Câu 2: Cho biết vị trí trong bảng tuần hoàn, số electron lớp ngoài cùng của nguyên tử mỗi nguyên tố N, C, O và vẽ sơ đồ hình thành liên kết trong các phân tử ở hình sau:
Trả lời:
Kí hiệu hoá học | Ô nguyên tố | Chu kì | Nhóm | Số e lớp ngoài cùng |
N | 7 | 2 | VA | 5 |
C | 6 | 2 | IVA | 4 |
O | 8 | 2 | VIA | 6 |
Sơ đồ nitrogen:
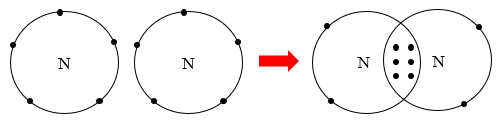
Sơ đồ carbon dioxide:
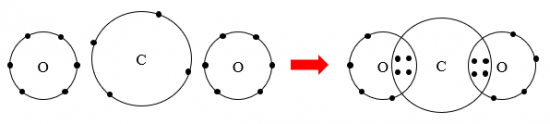
Câu 3: Potassium chloride là hợp chất có nhiều ứng dụng trong đời sống. Trong nông nghiệp, nó được dùng làm phân bón. Trong công nghiệp, potassium chloride được dùng làm nguyên liệu để sản xuất potassium hydroxide và kim loại potassium. Trong y học, potassium chloride được dùng để bào chế thuốc điều trị bệnh thiếu kali trong máu. Potassium chloride rất cần thiết cho cơ thể, trong các chức năng hoạt động của hệ tiêu hoá, tim, thận, cơ và cả hệ thần kinh. Hợp chất potassium chloride có loại liên kết gì trong phân tử? Vẽ sơ đồ hình thành liên kết có trong phân tử này.
Trả lời:
Liên kết ion.
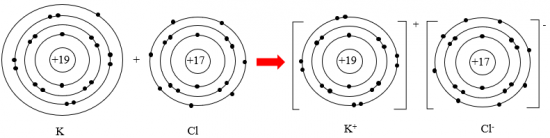
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
Giải Khoa học tự nhiên 7 Chân trời sáng tạo bài 6, Giải bài 6 Khoa học tự nhiên 7 Chân trời sáng tạo, Siêu nhanh Giải bài 6 Khoa học tự nhiên 7 Chân trời sáng tạo

Bình luận