5 phút giải Khoa học tự nhiên 9 Kết nối tri thức trang 92
5 phút giải Khoa học tự nhiên 9 Kết nối tri thức trang 92. Giúp học sinh nhanh chóng, mất ít thời gian để giải bài. Tiêu chi bài giải: nhanh, ngắn, súc tích, đủ ý. Nhằm tạo ra bài giải tốt nhất. 5 phút giải bài, bằng ngày dài học tập.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 19. DÃY HOẠT ĐỘNG HÓA HỌC
PHẦN I. HỆ THỐNG CÂU HỎI VÀ BÀI TẬP SGK
I. XÂY DỰNG DÃY HOẠT ĐỘNG HÓA HỌC
Sắp xếp mức độ hoạt động hóa học của: Na, Fe, H, Cu, Ag
Hoạt động 1: Khảo sát phản ứng của các kim loại Na, Fe, Cu với nước
Chuẩn bị: 1 mẩu kim loại natri bằng hạt dật xanh, đinh sắt và dây đồng; 2 ống nghiệm đựng nước đánh số (1), (2), chậu thủy tinh đựng nước.
Tiến hành: Cho mẩu natri vào chậu thủy tinh đựng nước, đinh sắt vào ống nghiệm (1), dây đồng vào ống nghiệm (2).
(Phản ứng của kim loại natri với nước xem Hình 18.5, Bài 18).
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
Dựa vào khả năng phản ứng với nước, có thể chia các kim loại natri, đồng và sắt thành mấy nhóm? So sánh mức độ hoạt động hóa học của các nhóm kim loại này.
Hoạt động 2: Khảo sát phản ứng của kim loại Fe, Cu với dung dịch acid
Chuẩn bị: đinh sắt, dây đồng, hai ống nghiệm đựng cùng một lượng dung dịch HCl cùng nồng độ.
Tiến hành: Cho đinh sắt, dây đồng vào từng ống nghiệm riêng biệt đựng dung dịch HCl.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:

a) Hãy cho biết kim loại nào phản ứng được với dung dịch HCl (đẩy được hydrogen ra khỏi acid).
b) So sánh mức độ hoạt động hóa học của sắt, đồng với hydrogen.
c) So sánh mức độ hoạt động hóa học của sắt với
Hoạt động 3: So sánh mức độ hoạt động hóa học của kim loại Ag và Cu
Chuẩn bị: dây đồng, dung dịch AgNO3 2%; ống nghiệm, panh.
Tiến hành: Dùng panh kẹp dây đồng đã được uốn thành hình lò xo đưa vào ống nghiệm chứa dung dịch AgNO3 2%.
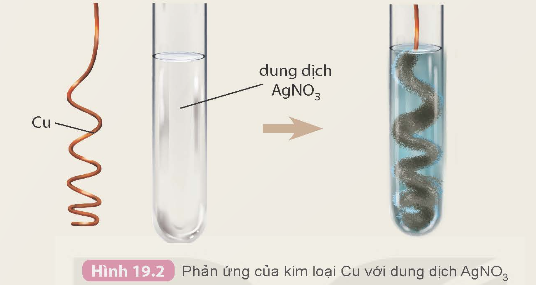
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
a) Mô tả hiện tượng và viết phương trình hóa học của phản ứng xảy ra.
b) So sánh mức độ hoạt động hóa học của đồng và bạc. Giải thích.
c) Qua ba thí nghiệm ở trên hãy sắp xếp mức độ hoạt động hóa học của các kim loại Na, Fe, Cu, Ag và H thành dãy theo chiều giảm dần.
II. Ý NGHĨA DÃY HOẠT ĐỘNG HÓA HỌC
Hoạt động 1: Kim loại hoạt động hóa học mạnh như K, Na, Ca phản ứng với nước ở điều kiện thường tạo ra sản phẩm gì?
Hoạt động 2: Kim loại đứng trước H phản ứng với dung dịch acid (H2SO4 loãng, HCl,...) tạo thành sản phẩm gì?
Hoạt động 3: Nêu khái quát về vị trí trong dãy hoạt động của:
- Kim loại hoạt động hóa học mạnh;
- Kim loại hoạt động hóa học trung bình;
- Kim loại hoạt động hóa học yếu.
Câu hỏi: Dự đoán hiện tượng xảy ra và viết phương trình hóa học của phản ứng (nếu có) trong các thí nghiệm sau:
1. Rót dung dịch H2SO4 loãng vào 3 ống nghiệm, mỗi ống khoảng 3 mL. Lần lượt cho vào mỗi ống nghiệm một mẩu kim loại trong số ba kim loại sau: Mg, Ag, Zn.
2. Cho viên kẽm vào ống nghiệm chứa dung dịch AgNO3.
3. Rót vào ba cốc thủy tinh loại 100 mL, mỗi cốc 25 mL nước cất. Cho vào mỗi cốc một mẩu kim loại trong số ba kim loại sau: Cu, Fe, Ca.
PHẦN II. 5 PHÚT GIẢI CÂU HỎI, BÀI TẬP SGK
I. XÂY DỰNG DÃY HOẠT ĐỘNG HÓA HỌC
Đáp án HĐ 1: + Tác dụng mạnh với nước: Na
![]()
+ Phản ứng ít (Fe) hoặc không phản ứng với nước (Cu):
![]()
Mức độ hoạt động: Na > Fe > Cu.
Đáp án HĐ 2: a) - Hiện tượng: dung dịch màu xanh lam và xuất hiện kết tủa trắng.
![]()
b) Cu > Ag. Vì đồng có thể đẩy bạc ra khỏi dung dịch muối.
c) Na, Fe, H, Cu, Ag.
II. Ý NGHĨA DÃY HOẠT ĐỘNG HÓA HỌC
Đáp án HĐ 1: Sản phẩm: dung dịch base và khí hydrogen.
![]()
Đáp án HĐ 2: Sản phẩm là muối và khí hydrogen.
![]()
Đáp án HĐ 3: - K, Ba, Ca, Na, Mg, Al.
- Zn, Fe, Pb.
- Cu, Ag, Au.
Đáp án CH: 1. Mg, Zn tác dụng với dung dịch H2SO4
PTHH:
![]()
![]()
Kim loại Ag không tác dụng với dung dịch H2SO4.
2. Hiện tượng: xuất hiện kết tủa trắng.
PHTT: ![]()
3. Tác dụng với nước: Na, Fe
![]()
![]()
Không phản ứng với nước: Cu.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
giải 5 phút Khoa học tự nhiên 9 Kết nối tri thức, giải Khoa học tự nhiên 9 Kết nối tri thức trang 92, giải Khoa học tự nhiên 9 KNTT trang 92
Giải bài tập những môn khác
Môn học lớp 9 KNTT
5 phút giải toán 9 KNTT
5 phút soạn bài văn 9 KNTT
Văn mẫu 9 kết nối tri thức
5 phút giải KHTN 9 KNTT
5 phút giải lịch sử 9 KNTT
5 phút giải địa lí 9 KNTT
5 phút giải hướng nghiệp 9 KNTT
5 phút giải lắp mạng điện 9 KNTT
5 phút giải trồng trọt 9 KNTT
5 phút giải CN thực phẩm 9 KNTT
5 phút giải tin học 9 KNTT
5 phút giải GDCD 9 KNTT
5 phút giải HĐTN 9 KNTT
Môn học lớp 9 CTST
5 phút giải toán 9 CTST
5 phút soạn bài văn 9 CTST
Văn mẫu 9 chân trời sáng tạo
5 phút giải KHTN 9 CTST
5 phút giải lịch sử 9 CTST
5 phút giải địa lí 9 CTST
5 phút giải hướng nghiệp 9 CTST
5 phút giải lắp mạng điện 9 CTST
5 phút giải cắt may 9 CTST
5 phút giải nông nghiệp 9 CTST
5 phút giải tin học 9 CTST
5 phút giải GDCD 9 CTST
5 phút giải HĐTN 9 bản 1 CTST
5 phút giải HĐTN 9 bản 2 CTST
Môn học lớp 9 cánh diều
5 phút giải toán 9 CD
5 phút soạn bài văn 9 CD
Văn mẫu 9 cánh diều
5 phút giải KHTN 9 CD
5 phút giải lịch sử 9 CD
5 phút giải địa lí 9 CD
5 phút giải hướng nghiệp 9 CD
5 phút giải lắp mạng điện 9 CD
5 phút giải trồng trọt 9 CD
5 phút giải CN thực phẩm 9 CD
5 phút giải tin học 9 CD
5 phút giải GDCD 9 CD
5 phút giải HĐTN 9 CD
Trắc nghiệm 9 Kết nối tri thức
Trắc nghiệm 9 Chân trời sáng tạo
Trắc nghiệm 9 Cánh diều
Tài liệu lớp 9
Văn mẫu lớp 9
Đề thi lên 10 Toán
Đề thi môn Hóa 9
Đề thi môn Địa lớp 9
Đề thi môn vật lí 9
Tập bản đồ địa lí 9
Ôn toán 9 lên 10
Ôn Ngữ văn 9 lên 10
Ôn Tiếng Anh 9 lên 10
Đề thi lên 10 chuyên Toán
Chuyên đề ôn tập Hóa 9
Chuyên đề ôn tập Sử lớp 9
Chuyên đề toán 9
Chuyên đề Địa Lý 9
Phát triển năng lực toán 9 tập 1
Bài tập phát triển năng lực toán 9

Bình luận