5 phút giải Hóa học 10 Cánh diều trang 53
5 phút giải Hóa học 10 Cánh diều trang 53. Giúp học sinh nhanh chóng, mất ít thời gian để giải bài. Tiêu chi bài giải: nhanh, ngắn, súc tích, đủ ý. Nhằm tạo ra bài giải tốt nhất. 5 phút giải bài, bằng ngày dài học tập.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 10: LIÊN KẾT ION
PHẦN I. HỆ THỐNG CÂU HỎI, BÀI TẬP TRONG SGK
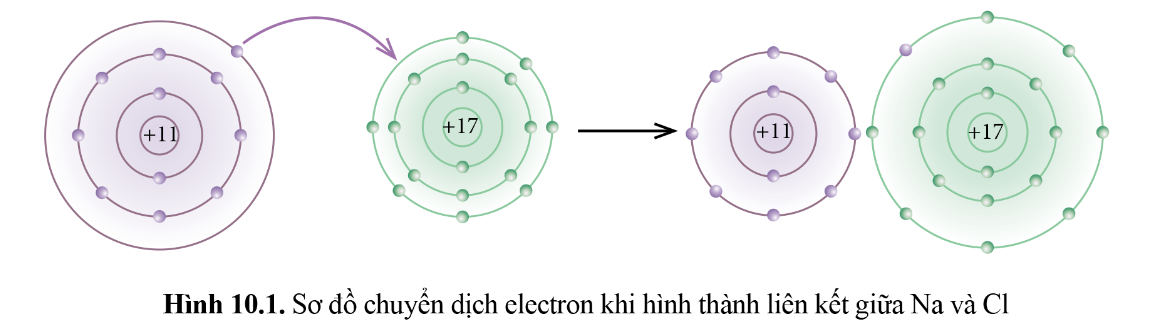
Phát biểu nào dưới đây phù hợp với sơ đồ phản ứng ở Hình 10.1?
(1) Nguyên tử Na nhường, nguyên tử Cl nhận electron để trở thành các ion.
(2) Nguyên tử Na và Cl góp chung electron để trở thành các ion.
I. KHÁI NIỆM VÀ SỰ HÌNH THÀNH LIÊN KẾT ION
Câu 1: Phát biểu nào sau đây là đúng?
a) Liên kết ion chỉ có trong đơn chất.
b) Liên kết ion chỉ có trong hợp chất.
c) Liên kết ion có trong cả đơn chất và hợp chất.
Luyện tập 1: Hãy nêu một số hợp chất ion:
a) Tạo nên bởi các ion đơn nguyên tử
b) Tạo nên bởi ion đơn nguyên tử và ion đa nguyên tử
c) Tạo nên bởi các ion đa nguyên tử
Câu 2: Viết hai giai đoạn của sự hình thành CaO từ các nguyên tử tương ứng (kèm theo cấu hình electron)
Luyện tập 2: Cho các ion: Li+, Ca2+, Al3+, F-, O2-, PO43-. Hãy viết công thức tất cả các hợp chất ion (tạo nên từ một loại cation và một loại anion) có thể được tạo thành từ các ion đã cho. Biết rằng tổng điện tích của các ion trong hợp chất bằng 0.
Luyện tập 3: Cho các chất sau: SiO2 là thành phần chính của thạch anh, CaCO3 là thành phần của đá vôi. Hãy cho biết chất nào được tạo nên bởi liên kết ion? Giải thích.
II. TINH THỂ ION
Thực hành 1: Lắp ráp mô hình tinh thể NaCl: Quan sát Hình 10.2b để lắp ráp mô hình tinh thể NaCl từ các quả cầu để minh hoạ cho ion Na+, Cl- và que nối.
Thực hành 2: Từ mô hình NaCl, hãy cho biết xung quanh mỗi ion Na+ có bao nhiêu ion Cl- (ở gần nhất với Na+)?
Vận dụng: Hãy kể tên một số hợp chất ion có xung quanh em và cho biết trong điều kiện thường, chúng tồn tại ở thể nào.
BÀI TẬP
Bài 1: Những phát biểu nào sau đây là đúng?
Hợp chất tạo nên bởi ion Al3+ và O2- là hợp chất
(a) cộng hóa trị (b) ion
(c) có công thức Al2O3 (d) có công thức Al3O2
Bài 2: Những tính chất nào sau đây là tính chất điển hình của hợp chất ion?
(a) Tồn tại ở thể khí trong điều kiện thường
(b) Có nhiệt độ nóng chảy và nhiệt độ sôi cao
(c) Thường tồn tại ở thể rắn trong điều kiện thường
(d) Có nhiệt độ nóng chảy và nhiệt độ sôi thấp
Bài 3: a) Giải thích vì sao bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng.
b) Vì sao cả Na2O và MgO đều là chất rắn ở nhiệt độ thường?
c) Vì sao nhiệt độ nóng chảy của MgO (2852 oC) cao hơn rất nhiều so với Na2O (1132 oC)?
PHẦN II. 5 PHÚT TRẢ LỜI CÂU HỎI, BÀI TẬP TRONG SGK
Phát biểu (1).
I. KHÁI NIỆM VÀ SỰ HÌNH THÀNH LIÊN KẾT ION
Câu 1:
c.
Luyện tập 1:
a) NaCl, KBr, MgCl…
b) KNO3, NH4Cl, Na2SO4…
c) NH4NO3, (NH4)2CO3,...
Câu 2:
- GĐ1: Hình thành ion
Ca → Ca2+ + 2e; O + 2e → O2-
- GĐ2: Các ion trái dấu kết hợp.
Ca2+ + O2- → CaO
Luyện tập 2:
LiF, Li2O, Li3PO4, CaF2, CaO, Ca3(PO4)2, Al2O3, AlPO4, AlF3
Luyện tập 3:
CaCO3 vì Si và O không tạo được ion trái dấu.
II. TINH THỂ ION
Thực hành 1:
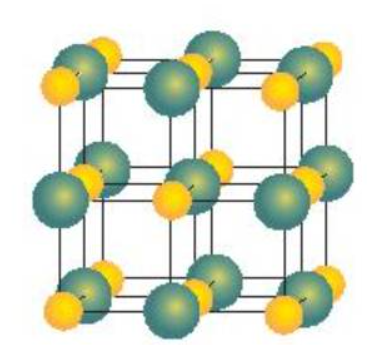
Thực hành 2:
6.
Vận dụng:
NaCl (muối ăn), CaO (vôi sống), CaCO3 (đá vôi): thể rắn.
BÀI TẬP
Bài 1:
b và c.
Bài 2:
b và c.
Bài 3:
a) - Ion Na+ chỉ có 2 lớp electron nên bán kính Na+ nhỏ hơn
- Ion Mg2+ chỉ có 2 lớp electron nên bán kính Mg2+ nhỏ hơn.
b) Nguyên tử Na, Mg nhường electron, nguyên tử O nhận tạo hợp chất ion.
c) Vì bán kính Na+ > bán kính Mg2+. Mà năng lượng phân li TLN với Rion.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
giải 5 phút Hóa học 10 Cánh diều, giải Hóa học 10 Cánh diều trang 53, giải Hóa học 10 CD trang 53

Bình luận