Giáo án hóa học 11 mới năm 2023 cánh diều
Bộ giáo án 11 cánh diều. Đây lhóa họcà giáo án sách lớp 11 mới năm học 2023-2024. Giáo án có đầy đủ các bài kì 1 + kì 2. Với cách trình bày khoa học, chi tiết. Giáo viên chỉ việc tải về và sử dụng. Cách tải đơn giản. Giáo án hóa học 11 cánh diều là giáo án bản word, dễ dàng chỉnh sửa
Click vào ảnh dưới đây để xem giáo án rõ







Xem video về:Giáo án hóa học 11 mới năm 2023 cánh diều
Đầy đủ Giáo án hóa học THPT cánh diều
- Bài giảng điện tử Hóa học 12 cánh diều
- Bài giảng điện tử Hoá học 12 cánh diều
- Giáo án chuyên đề Hoá học 12 mới năm 2024 cánh diều
- Giáo án Hoá học 12 mới năm 2024 cánh diều
- Giáo án chuyên đề hóa học 11 mới năm 2023 cánh diều
- Bài giảng điện tử hóa học 11 cánh diều
- Giáo án hóa học 11 mới năm 2023 cánh diều
- Bài giảng Powerpoint hóa học 10 cánh diều
- Tải GA word hóa học 10 cánh diều
Ngày soạn:…/…/…
Ngày dạy:…/…/…
CHƯƠNG 1. CÂN BẰNG HÓA HỌC
BÀI 1: KHÁI NIỆM VỀ CÂN BẰNG HÓA HỌC
- MỤC TIÊU
- Kiến thức
Sau bài học này, HS sẽ:
- Trình bày được khái niệm phản ứng thuận nghịch và trạng thái cân bằng của một phản ứng thuận nghịch
- Viết được biểu thức hằng số cân bằng (KC) của một phản ứng thuận nghịch
- Thực hiện được thí nghiệm nghiên cứu ảnh hưởng của nhiệt độ tới chuyển dịch cân bằng.
- Vận dụng được nguyên lí chuyển dịch cân bằng Le Chatelier để giải thích ảnh hưởng của nhiệt độ, nồng độ, áp suất đến cân bằng hóa học.
- Năng lực
Năng lực chung:
- Năng lực tự chủ và tự học: Chủ động, tích cực tìm hiểu được khái niệm phản ứng thuận nghịch và trạng thái cân bằng của một phản ứng thuận nghịch
- Năng lực giao tiếp và hợp tác: Sử dụng ngôn ngữ khoa học để mô tả các khái niệm, hiện tượng. Hoạt động nhóm một cách hiệu quả theo đúng yêu cầu của GV, tích cực tham gia các hoạt động trong lớp.
- Giải quyết vấn đề và sáng tạo: Thảo luận với các thành viên trong nhóm nhằm giải quyết các vấn đề trong bài học để hoàn thành nhiệm vụ học tập.
Năng lực khoa học tự nhiên:
- Nhận thức khoa học tự nhiên: Nêu được khái niệm phản ứng thuận nghịch và trạng thái cân bằng của một phản ứng thuận nghịch.
- Tìm hiểu tự nhiên: Thông qua các hoạt động thảo luận, quan sát các hiện tượng thí nghiệm rút ra được nhận xét về phản ứng thuận nghịch và cân bằng hóa học, dự đoán được chiều chuyển dịch cân bằng hóa học trong những điều kiện cụ thể.
- Vận dụng kiến thức, kĩ năng đã học: Vận dụng được các yếu tố ảnh hưởng đến cân bằng hóa học, đề xuất cách tăng hiệu suất phản ứng trong trường hợp cụ thể.
- Phẩm chất
- Tham gia tích cực hoạt động nhóm phù hợp với khả năng của bản thân.
- Cẩn thận, trung thực và thực hiện các yêu cầu trong bài học.
- Có niềm say mê, hứng thú với việc khám phá và học tập khoa học tự nhiên.
- THIẾT BỊ DẠY HỌC
- Đối với giáo viên
- SGK, SGV, SBT.
- Tranh ảnh, video thí nghiệm liên quan đến bài học (nếu cần).
- Dụng cụ hóa chất để thực hiện các thí nghiệm trong SGK.
- Đối với học sinh
- SGK, SBT.
- Tranh ảnh, tư liệu sưu tầm liên quan đến bài học và dụng cụ học tập (nếu cần) theo yêu cầu của GV.
III. TIẾN TRÌNH DẠY HỌC
- HOẠT ĐỘNG KHỞI ĐỘNG
- Mục tiêu: Tạo tâm thế hứng thú cho học sinh và từng bước làm quen bài học.
- Nội dung: GV trình bày vấn đề, HS suy nghĩ và trả lời câu hỏi.
- Sản phẩm học tập: HS trả lời được câu hỏi theo ý kiến cá nhân.
- Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ:
- GV đặt vấn đề:
Khí NO2 (màu nâu đỏ) liên tục chuyển hóa thành khí N2O4 (không màu) và ngược lại, tại một điều kiện xác định. Tại điều kiện này, khí NO2 cũng như khí N2O4 trong các bình riêng biệt (Hình 1.1), sau một thời gian đều chuyển thành hỗn hợp khí có thành phần như nhau và không đổi theo thời gian
Tại thời điểm hỗn hợp khí trong hai bình có thành phần như nhau, có phản ứng diễn ra trong hai bình này hay không?
Bước 2: Thực hiện nhiệm vụ
- HS lắng nghe câu hỏi, suy nghĩ, thảo luận trả lời câu hỏi phần khởi động.
Bước 3: Báo cáo kết quả hoạt động và thảo luận
- HS đưa ra những nhận định ban đầu.
Bước 4: Kết luận, nhận định
- GV đánh giá câu trả lời của HS, trên cơ sở đó dẫn dắt HS vào bài học – Bài 1: Mở đầu về cân bằng hóa học.
SOẠN HÓA HỌC 10 CÁNH DIỀU SOẠN CHI TIẾT:
- Tải GA word hóa học 10 cánh diều
- Bài giảng Powerpoint hóa học 10 cánh diều
- Giáo án word chuyên đề hoá học 10 cánh diều cả năm
HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC
Hoạt động 1: Tìm hiểu khái niệm phản ứng thuận nghịch và trạng thái cân bằng
- Mục tiêu: Thông qua hoạt động, HS trình bày được khái niệm phản ứng một chiều, phản ứng thuận nghịch, trạng thái cân bằng của phản ứng thuận nghịch.
- Nội dung: GV trình bày vấn đề; HS lắng nghe, đọc hiểu Ví dụ 1, 2, thảo luận và trả lời Câu hỏi 1 – 4 SGK trang 7, 8.
- Sản phẩm học tập: HS phân biệt được phản ứng một chiều và phản ứng thuận nghịch, trạng thái cân bằng của phản ứng thuận nghịch, lấy được ví dụ, câu trả lời cho Câu hỏi 1 – 4 SGK trang 7, 8.
- Tổ chức hoạt động:
HOẠT ĐỘNG CỦA GIÁO VIÊN - HỌC SINH | DỰ KIẾN SẢN PHẨM |
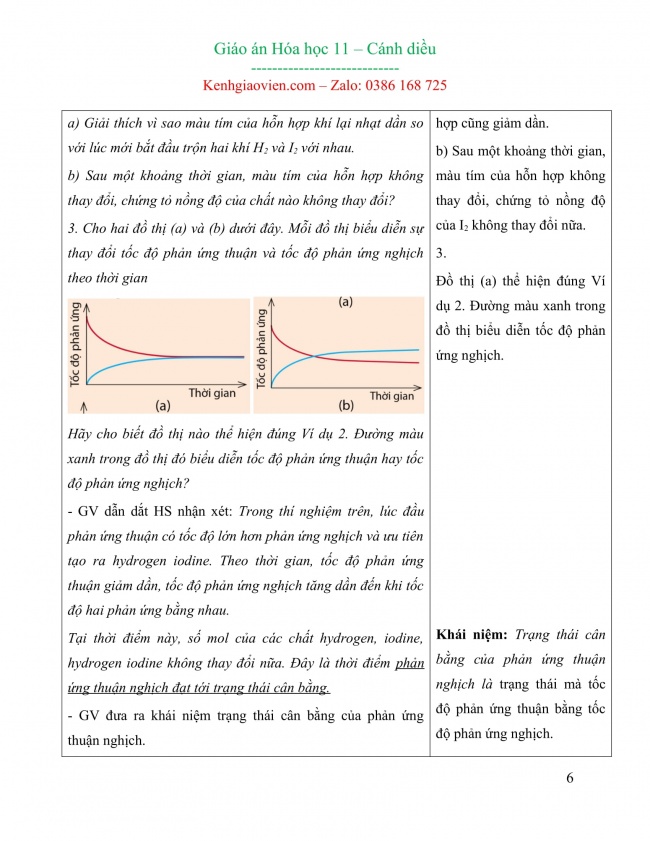
Bước 1: Chuyển giao nhiệm vụ * Phản ứng một chiều - GV viết phương trình hóa học : Fe(s) + 2HCl(aq) FeCl2(aq) + H2(g) (1) - GV nêu đặc điểm của phản ứng (1): + Trong cùng điều kiện, FeCl2(aq) và H2(g) không thể biến đổi lại thành Fe(s) và HCl(aq) được. + Phản ứng có đặc điểm như vậy được gọi là phản ứng một chiều. - GV chốt lại đặc điểm của phản ứng một chiều: Các chất sản phẩm không phản ứng lại được với nhau tạo thành chất đầu. - GV đặt câu hỏi: Vậy có phản ứng nào mà các chất sản phẩm lại phản ứng được với nhau để tạo thành chất đầu không? * Phản ứng thuận nghịch - GV: Trong thực tế, nhiều phản ứng không chỉ diễn ra theo một chiều mà đồng thời theo cả hai chiều, chiều thuận và chiều nghịch. - GV yêu cầu HS thảo luận cặp đôi tìm hiểu Ví dụ 1 SGK trang 7 và trả lời câu hỏi: N2(g) + 3H2(g) 2NH3(g) (1) + Chiều các chất ban đầu tạo thành sản phẩm được gọi là chiều gì? (chiều thuận) + Chiều các chất sản phẩm tạo thành chất ban đầu được gọi là chiều gì? (chiều nghịch) + Phản ứng thuận nghịch là gì? - GV kết luận: Phản ứng (1) được gọi là phản ứng thuận nghịch. - GV yêu cầu HS trả lời Câu hỏi 1 SGK trang 7: 1. Hãy nêu một số ví dụ về phản ứng thuận nghịch mà em biết. * Trạng thái cân bằng - GV chia lớp thành các nhóm, thảo luận nghiên cứu về trạng thái cân bằng hóa học thông qua Ví dụ 2 SGK trang 7, 8: H2(g) + I2(g) 2HI (g) - GV yêu cầu các nhóm trả lời Câu hỏi 2, 3 SGK trang 7: 2. Xét Ví dụ 2: a) Giải thích vì sao màu tím của hỗn hợp khí lại nhạt dần so với lúc mới bắt đầu trộn hai khí H2 và I2 với nhau. b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi, chứng tỏ nồng độ của chất nào không thay đổi? 3. Cho hai đồ thị (a) và (b) dưới đây. Mỗi đồ thị biểu diễn sự thay đổi tốc độ phản ứng thuận và tốc độ phản ứng nghịch theo thời gian
Hãy cho biết đồ thị nào thể hiện đúng Ví dụ 2. Đường màu xanh trong đồ thị đó biểu diễn tốc độ phản ứng thuận hay tốc độ phản ứng nghịch? - GV dẫn dắt HS nhận xét: Trong thí nghiệm trên, lúc đầu phản ứng thuận có tốc độ lớn hơn phản ứng nghịch và ưu tiên tạo ra hydrogen iodine. Theo thời gian, tốc độ phản ứng thuận giảm dần, tốc độ phản ứng nghịch tăng dần đến khi tốc độ hai phản ứng bằng nhau. Tại thời điểm này, số mol của các chất hydrogen, iodine, hydrogen iodine không thay đổi nữa. Đây là thời điểm phản ứng thuận nghịch đạt tới trạng thái cân bằng. - GV đưa ra khái niệm trạng thái cân bằng của phản ứng thuận nghịch. - GV nhấn mạnh với HS đặc điểm của cân bằng hóa học: Cân bằng hóa học là một cân bằng động, ở trạng thái cân bằng phản ứng thuận và phản ứng nghịch vẫn tiếp diễn với tốc độ bằng nhau nhưng nồng độ của một chất bất kì trong phản ứng không đổi là do lượng mất đi và lượng sinh ra chất đó bằng nhau.
- GV yêu cầu HS thảo luận trả lời Câu hỏi 4 SGK trang 8: 4. Vì sao giá trị là một hằng số ở nhiệt độ xác định? Bước 2: Thực hiện nhiệm vụ - HS suy nghĩ trả lời câu hỏi của GV, Câu hỏi 1 – 4 SGK trang 7, 8. - GV hướng dẫn, theo dõi, hỗ trợ HS nếu cần thiết. Bước 3: Báo cáo kết quả hoạt động và thảo luận - Đại diện HS trả lời câu hỏi của GV, Câu hỏi 1 – 4 SGK trang 7, 8. - GV mời HS khác nhận xét, bổ sung. Bước 4: Kết luận, nhận định GV đánh giá, nhận xét, tổng kết các đặc điểm của phản ứng một chiều và phản ứng thuận nghịch, trạng thái cân bằng của phản ứng thuận nghịch. | I. Khái niệm phản ứng thuận nghịch và trạng thái cân bằng - Phản ứng một chiều là phản ứng chỉ xảy ra theo chiều chất phản ứng biến đổi thành chất sản phẩm, ví dụ : Fe(s) + 2HCl(aq) FeCl2(aq) + H2(g).
Ví dụ 1 (SGK trang 7) - Phản ứng thuận nghịch là phản ứng trong đó ở cùng điều kiện, xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng. Trả lời câu hỏi 1 SGK trang 7: Một số ví dụ về phản ứng thuận nghịch: 2SO2 + O2 2SO3 CH3COOH + C2H5OH CH3COOC2H5 + H2O Ví dụ 2 (SGK trang 7, 8) Trả lời Câu hỏi 2, 3 SGK trang 7: 2. a) Sau khi trộn hai khí, phản ứng thuận diễn ra, nồng độ H2 và I2 giảm dần nên giảm dần, màu tím của hỗn hợp cũng giảm dần. b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi, chứng tỏ nồng độ của I2 không thay đổi nữa. 3. Đồ thị (a) thể hiện đúng Ví dụ 2. Đường màu xanh trong đồ thị biểu diễn tốc độ phản ứng nghịch.
Khái niệm: Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái mà tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. Đặc điểm: + Cân bằng hóa học là một cân bằng động + Ở trạng thái cân bằng, phản ứng thuận và phản ứng nghịch vẫn tiếp diễn với tốc độ bằng nhau. + Ở trạng thái cân bằng, nồng độ của một chất bất kì trong phản ứng không đổi. Trả lời Câu hỏi 4 SGK trang 8: Ta có: Vì ở trạng thái cân bằng nồng độ của một chất bất kì trong phản ứng không đổi nên giá trị là một hằng số ở nhiệt độ xác định. |
SOẠN HÓA HỌC 11 CÁNH DIỀU CHUẨN KHÁC:
Hoạt động 2: Tìm hiểu biểu thức hằng số cân bằng và ý nghĩa
- Mục tiêu: Thông qua hoạt động, HS viết được biểu thức hằng số cân bằng (KC) của một phản ứng thuận nghịch, nêu được ý nghĩa của biểu thức hằng số cân bằng.
- Nội dung: GV trình bày vấn đề; HS lắng nghe, đọc hiểu Ví dụ 3, 4, thảo luận và trả lời Câu hỏi 5 – 7 SGK trang 9, 10.
- Sản phẩm học tập: HS viết vào vở biểu thức và ý nghĩa hằng số cân bằng, câu trả lời Câu hỏi 5 – 7 SGK trang 9, 10.
- Tổ chức hoạt động:
HOẠT ĐỘNG CỦA GIÁO VIÊN - HỌC SINH | DỰ KIẾN SẢN PHẨM |
Bước 1: Chuyển giao nhiệm vụ * Biểu thức hằng số cân bằng - GV giới thiệu biểu thức tính tính hằng số cân bằng của phản ứng thuận nghịch tổng quát. aA + bB mM + nN - GV lưu ý HS: + Hằng số cân bằng KC của một phản ứng thuận nghịch, chỉ phụ thuộc nhiệt độ và bản chất của phản ứng, không phụ thuộc nồng độ ban đầu của các chất. + Nồng độ của chất rắn được coi bằng 1 và không có mặt trong biểu thức tính hằng số cân bằng. - GV lấy ví dụ về phản ứng thuận nghịch có mặt của chất rắn và hướng dẫn HS viết biểu thức hằng số cân bằng của phản ứng: C(s) + CO2(g) 2CO(g) - GV yêu cầu HS thảo luận trả lời Câu hỏi 5, 6 SGK trang 9: 5. Viết biểu thức hằng số cân bằng KC cho phản ứng thuận nghịch: a) N2(g) + 3H2(g) 2NH3(g) b) CaCO3(s) CaO(s) + CO2(g) 6. Viết biểu thức hằng số cân bằng KC cho phản ứng (*), (**) dưới đây. H2(g) + I2(g) 2HI(g) (*) H2(g) + I2(g) HI(g) (**) Theo em, giá trị hai hằng số cân bằng này có bằng nhau không? * Ý nghĩa của hằng số cân bằng - GV yêu cầu HS hoạt động nhóm tìm hiểu ý nghĩa biểu thức hằng số cân bằng qua các Ví dụ 3, 4 SGK trang 9, 10. - GV: Như vậy, dựa vào độ lớn của hằng số cân bằng có thể biết được nồng độ của chất tham gia hay chất sản phẩm là chiếm ưu thế ở trạng thái cân bằng, cũng như phản ứng thuận có xảy ra thuận lợi hay không. - GV yêu cầu HS rút ra các kết luận về ý nghĩa của biểu thức hằng số cân bằng: + Nếu phản ứng thuận nghịch có KC rất lớn so với 1 thì phản ứng thuận diễn ra như thế nào? Các chất ở trạng thái cân bằng chủ yếu là chất nào? + Nếu phản ứng thuận nghịch có KC rất nhỏ so với 1 thì phản ứng thuận diễn ra như thế nào? Các chất ở trạng thái cân bằng chủ yếu là chất nào? - GV cho HS đọc mục Em có biết SGK trang 10, GV lưu ý HS: Hằng số cân bằng lớn (hay nhỏ) chỉ cho biết phản ứng thuận diễn ra thuận lợi hay không thuận lợi mà không cho biết thời gian đạt đến trạng thái cân bằng là nhanh hay chậm. - GV yêu cầu HS trả lời Câu hỏi 7 SGK trang 10: 7. Hai acid HA và HB cùng nồng độ ban đầu là 0,5 M, phân li trong nước theo các cân bằng: HA H+ + A- HB H++ B- Với các hằng số cân bằng (hay gọi là hằng số phân li acid) tương ứng là KC(HA) = 0,2 và KC(HB) = 0,1. Tính nồng độ H+ của mỗi dung dịch acid. Rút ra kết luận về mối liên hệ giữa độ mạnh của acid với độ lớn của hằng số phân li acid. Biết rằng acid càng mạnh khi càng dễ tạo ra H+ Bước 2: Thực hiện nhiệm vụ - HS thảo luận theo cặp đôi, đọc hiểu Ví dụ 3, 4 và trả lời Câu hỏi 5, 6, 7 SGK trang 9, 10 - GV hướng dẫn, theo dõi, hỗ trợ HS nếu cần thiết. Bước 3: Báo cáo kết quả hoạt động và thảo luận - Đại diện HS trả lời Câu hỏi 5, 6, 7 SGK trang 9, 10 - GV mời HS khác nhận xét, bổ sung. Bước 4: Kết luận, nhận định GV đánh giá, nhận xét, chuẩn kiến thức về biểu thức hằng số cân bằng và ý nghĩa, chuyển sang nội dung mới. | II. Biểu thức hằng số cân bằng và ý nghĩa 1. Biểu thức hằng số cân bằng - Xét phản ứng thuận nghịch tổng quát: aA + bB mM + nN - Ở trạng thái cân bằng, hằng số cân bằng (KC) của phản ứng được xác định theo biểu thức: - Trong đó: [M], [N], [A], [B] là nồng độ mol của các chất M, N, A, B ở trạng thái cân bằng; m, n, a, b là hệ số tỉ lượng của các chất trong phương trình hóa học của phản ứng. Trả lời Câu hỏi 5, 6 SGK trang 9: 5. a) b) 6. (*): (**): Hai giá trị hằng số cân bằng này không bằng nhau.
2. Ý nghĩa của biểu thức hằng số cân bằng Ví dụ 3, 4 (SGK trang 9, 10)
- KC phụ thuộc vào bản chất của phản ứng và nhiệt độ. - KC rất lớn so với 1 thì phản ứng thuận càng chiếm ưu thế hơn, các chất ở trạng thái cân bằng chủ yếu là chất sản phẩm - Ngược lại, KC rất nhỏ so với 1 thì phản ứng nghịch càng chiếm ưu thế hơn, các chất ở trạng thái cân bằng chủ yếu là chất ban đầu.
Trả lời Câu hỏi 7 SGK trang 10: HA H+ + A- Co 0,5 [ ] 0,5 – a a a KC(HA) = = = 0,2 a = 0,232 HB H++ B- Co 0,5 [ ] 0,5 – b b b KC(HB) = = = 0,1 b = 0,179 Ta có: a > b; KC(HA) > KC(HB) nên hằng số phân li acid càng lớn, acid càng mạnh. |
SOẠN GIÁO ÁN TẤT CẢ CÁC MÔN LỚP 11 MỚI:
- Giáo án tất cả các môn lớp 11 chân trời sáng tạo
- Giáo án tất cả các môn lớp 11 cánh diều
- Giáo án tất cả các môn lớp 11 kết nối tri thức
Hoạt động 3: Tìm hiểu về ảnh hưởng của nhiệt độ, nồng độ và áp suất đến cân bằng hóa học
- Mục tiêu: Thông qua hoạt động, HS thực hiện được thí nghiệm nghiên cứu ảnh hưởng của nhiệt độ tới chuyển dịch cân bằng, vận dụng được nguyên lí chuyển dịch cân bằng Le Chatelier để giải thích ảnh hưởng của nhiệt độ, nồng độ, áp suất đến cân bằng hóa học.
- Nội dung: GV trình bày vấn đề; HS lắng nghe, thực hiện thí nghiệm 1, 2; đọc hiểu các Ví dụ 5 – 8; trả lời Câu hỏi 8, 9 SGK trang 11 – 13.
- Sản phẩm học tập: Kết quả thực hiện được thí nghiệm 1, 2; câu trả lời cho Câu hỏi 8, 9 SGK trang 11 – 13
- Tổ chức hoạt động:
HOẠT ĐỘNG CỦA GIÁO VIÊN - HỌC SINH | DỰ KIẾN SẢN PHẨM | |||||||||||||||||||||||||||
Bước 1: Chuyển giao nhiệm vụ * Ảnh hưởng của nhiệt độ tới cân bằng hóa học - GV chia lớp thành các nhóm, thực hiện thí nghiệm nghiên cứu ảnh hưởng của nhiệt độ tới chuyển dịch cân bằng thông qua các thí nghiệm: Thí nghiệm 1: 2NO2(g) N2O4(g) < 0 (8) (màu nâu đỏ) (không màu) - GV phát cho các nhóm: Ba ống nghiệm (1), (2), (3) chứa NO2 (có màu giống nhau), một cốc nước nóng (70 – 80 oC) và một cốc nước đá. - GV hướng dẫn HS cách tiến hành: + Ống nghiệm thứ nhất (1) được để ở nhiệt độ phòng (khoảng 25oC). + Ống nghiệm thứ (2) được nhúng vào cốc nước nóng + Ống nghiệm thứ ba (3) được nhúng vào cốc nước đá. - GV lưu ý HS: NO2 là khí độc, chú ý nút kín ống nghiệm, làm trong tủ hút. - GV yêu cầu HS quan sát hiện tượng và giải thích. - GV cho HS thảo luận trả lời Câu hỏi 8 SGK trang 11: 8. Từ Thí nghiệm 1, hãy cho biết: a) Dựa vào dấu hiệu nào để biết trạng thái cân bằng của phản ứng (8) bị chuyển dịch khi thay đổi nhiệt độ b*) Khi tăng nhiệt độ hoặc giảm nhiệt độ, cân bằng chuyển dịch theo chiều thu nhiệt hay tỏa nhiệt?
Thí nghiệm 2: CH3COO- + H2O CH3COOH + OH- > 0 - GV phát hóa chất và dụng cụ thí nghiệm cho các nhóm: CH3COONa tinh thể; ống nghiệm, cốc thủy tinh. - GV hướng dẫn HS cách tiến hành: + Cho 1 thìa tinh thể CH3COONa vào ống nghiệm A chứa khoảng 5 ml nước cất, lắc đều. + Thêm 2 – 3 giọt chất chỉ thị phenolphthalein. + Rót khoảng một nửa dung dịch từ ống nghiệm A sang B, đặt ống nghiệm B vào cốc nước nóng (khoảng 70 oC – 80 oC). + Sau 2p, quan sát và so sánh màu sắc của dung dịch trong hai ống nghiệm - GV yêu cầu các nhóm thảo luận về chiều chuyển dịch cân bằng khi nhiệt độ tăng lên. - GV kết luận về ảnh hưởng của nhiệt độ đến sự chuyển dịch cân bằng hóa học: Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều làm giảm nhiệt độ, tức là chiều phản ứng thu nhiệt (> 0), nghĩa là chiều làm giảm tác động của việc tăng nhiệt độ và ngược lại. * Nguyên lí chuyển dịch cân bằng Le Chatelier - GV giới thiệu HS nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
- GV yêu cầu HS áp dụng nguyên lí trên để trả lời Câu hỏi 9 SGK trang 12: 9. Cân bằng 2NO2(g) N2O4(g) chuyển dịch theo chiều nào khi tăng áp suất của hỗn hợp (bằng cách nén hỗn hợp) ở điều kiện nhiệt độ không đổi. Biết rằng áp suất tỉ lệ với số mol chất khí. - GV yêu cầu HS thảo luận nhóm, tìm hiểu và trình bày lại Ví dụ 6 – 8 SGK trang 13. Bước 2: Thực hiện nhiệm vụ - HS đọc hiểu các Ví dụ 5 – 8; thực hiện thí nghiệm 1, 2; trả lời Câu hỏi 8, 9 SGK trang 11 – 13. - GV hướng dẫn, theo dõi, hỗ trợ HS nếu cần thiết. Bước 3: Báo cáo kết quả hoạt động và thảo luận - Đại diện HS báo cáo kết quả thực hiện thí nghiệm 1,2; Câu hỏi 8, 9 SGK trang 11 – 12. - GV mời HS khác nhận xét, bổ sung. Bước 4: Kết luận, nhận định GV đánh giá, nhận xét, chuẩn kiến thức về ảnh hưởng của nhiệt độ đến sự chuyển dịch cân bằng hóa học và nguyên lí chuyển dịch cân bằng Le Chatelier. | III. Ảnh hưởng của nhiệt độ, nồng độ và áp suất đến cân bằng hóa học 1. Ảnh hưởng của nhiệt độ tới cân bằng hóa học Thí nghiệm 1 (SGK trang 11) 2NO2(g) N2O4(g) - 58 kJ (8) (màu nâu đỏ) (không màu) - Hiện tượng thí nghiệm và giải thích:
Trả lời Câu hỏi 8 SGK trang 11: a) Dựa sự thay đổi màu khí trong ống nghiệm. b)
Thí nghiệm 2 (SGK trang 12) CH3COO- + H2O CH3COOH + OH- - Hiện tượng và chiều chuyển dịch cân bằng:
2. Nguyên lí chuyển dịch cân bằng Le Chatelier Ví dụ 5 (SGK trang 12) - Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó. Trả lời Câu hỏi 9 SGK trang 12: Cân bằng dịch chuyển theo chiều thuận
Ví dụ 6 – 8 (SGK trang 13) |
- HOẠT ĐỘNG LUYỆN TẬP
- Mục tiêu: Củng cố lại kiến thức đã học thông qua trả lời câu hỏi dưới dạng trắc nghiệm.
- Nội dung: HS sử dụng SGK, kiến thức đã học, GV hướng dẫn (nếu cần thiết) để trả lời câu hỏi.
- Sản phẩm học tập: HS hoàn thành được bài tập trắc nghiệm
- Tổ chức thực hiện:
....CÒN TIẾP
Nâng cấp lên tài khoản VIP để tải tài liệu và dùng thêm được nhiều tiện ích khác
