Đề số 5: Đề kiểm tra hóa học 11 Kết nối bài 7 Sulfur và sulfur dioxide
III. DẠNG 3 – ĐỀ TRẮC NGHIỆM VÀ TỰ LUẬN
ĐỀ SỐ 5
I. Phần trắc nghiệm (4 điểm)
(Chọn chữ cái trước câu trả lời đúng nhất.)
Câu 1. Trong phương trình phản ứng sau, SO2 đóng vai trò gì
SO2 + 2H2S → 3S + 2H2O
- A. Vừa là chất oxi hóa, vừa là chất khử
- B. Là chất khử
- C. Là chất oxi hóa
- D. Không là chất oxi hóa cũng không là chất khử
Câu 2. So sánh tính chất cơ bản của oxigen và sulfur ta có
- A. tính oxi hóa của oxi < sulfur
- B. tính khử của sulfur > oxi
- C. tính oxi hóa của oxi = tính oxi hóa của S
- D. tính khử của oxi = tính khử của S
Câu 3: Để phân biệt SO2 và CO2 chỉ cần dùng thuốc thử là
- A. dung dịch Ba(OH)2
- B. CaO
- C. dung dịch NaOH
- D. nước bromine
Câu 4. Để loại bỏ các khí HCl, CO2 và SO2 có lẫn trong khí N2, người ta sử dụng lượng dư dung dịch
- A. NaCl.
- B. CuCl2.
- C. Ca(OH)2.
- D. H2SO4.
II. Phần tự luận (6 điểm)
Câu 1(4 điểm): Hoàn thành các phản ứng sau, xác định sự thay đổi số oxi hóa của các chất và cho biết trong các phản ứng đó, SO2 thể hiện tính oxi hóa hay tính khử.
(1) SO2 + 2H2S ⟶
(2) SO2 + Br2 + H2O ⟶
Câu 2 (2 điểm): Cho 11 gam hỗn hợp bột aluminium và bột iron tác dụng hoàn toàn với bột sulfur trong điều kiện không có không khí, thì thấy lượng sulfur tham gia phản ứng là 12,8g. Tính khối lượng sắt có trong hỗn hợp đầu.
Trắc nghiệm: (Mỗi câu đúng tương ứng với 1 điểm)
Câu hỏi | Câu 1 | Câu 2 | Câu 3 | Câu 4 |
Đáp án | C | B | D | C |
Tự luận:
Câu 1 (4 điểm) |
|
Câu 2 (2 điểm) | nS = Bảo toàn electron: 2nFe + 3nAl = 2nS 56nFe + 27nAl = 11; 2nFe + 3nAl = 2.0,4 nFe = 0,1nAl = 0,2 ⟹ mFe = 0,1.56 = 5,6 (gam) |
Giải những bài tập khác
Giải bài tập những môn khác
Giải sgk lớp 11 KNTT
Giải sgk lớp 11 CTST
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều

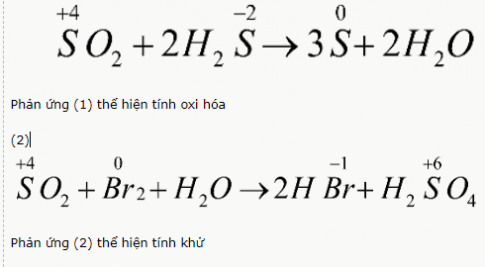
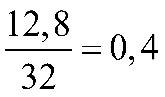 mol mhh = mFe + mAl
mol mhh = mFe + mAl
Bình luận