Đề thi cuối kì 1 Hóa học 11 KNTT: Đề tham khảo số 3
Trọn bộ đề thi cuối kì 1 Hóa học 11 KNTT: Đề tham khảo số 3 bộ sách mới Kết nối tri thức gồm nhiều câu hỏi ôn tập hay, các dạng bài tập phong phú giúp các em củng cố ôn luyện lại kiến thức thật tốt chuẩn bị tốt cho kì thi sắp tới. Tài liệu có kèm theo đáp án và lời giải chi tiết. Hi vọng đây sẽ là tài liệu hữu ích giúp các em đạt điểm cao. Thầy cô và các em kéo xuống để tham khảo ôn luyện
PHÒNG GD & ĐT ………………. | Chữ kí GT1: ........................... |
TRƯỜNG THPT………………. | Chữ kí GT2: ........................... |
ĐỀ KIỂM TRA HỌC KÌ 1
HÓA HỌC 11 – KẾT NỐI TRI THỨC
NĂM HỌC: 2023 - 2024
Thời gian làm bài: 45 phút (Không kể thời gian phát đề)
Họ và tên: …………………………………… Lớp: ……………….. Số báo danh: …………………………….……Phòng KT:………….. | Mã phách |
Điểm bằng số
| Điểm bằng chữ | Chữ ký của GK1 | Chữ ký của GK2 | Mã phách |
A. PHẦN TRẮC NGHIỆM (7 điểm)
Khoanh tròn vào chữ cái đứng trước câu trả lời đúng:
Câu 1. Chọn phát biểu sai?
A. Sulfur tan nhiều trong alcohol
B. Sulfur không tan trong nước
C. Sulfur có hai dạng thù hình
D. Sulfur tan nhiều trong carbon disulfide
Câu 2. Nhận xét nào sau đây đúng?
A. Khi bỏng do sulfuric acid, có thể dùng kem đánh răng bôi lên vết bỏng.
B. Tính acid của sulfuric acid loãng là tính acid yếu.
C. Sulfuric acid đặc, nóng có tính oxi hóa mạnh.
D. Sulfuric acid là chất lỏng sánh, màu vàng nhạt.
Câu 3. Nhận xét nào dưới đây không đúng?
A. Hợp chất hữu cơ có ở xung quanh ta
B. Hợp chất hữu cơ là hợp chất của carbon
C. Khi đốt cháy các hợp chất hữu cơ đều thấy tạo ra CO2
D. Đốt cháy hợp chất hữu cơ luôn thu được CO2 và H2O
Câu 4. Chọn ý đúng khi nói về tính chất vật lý của sulfur?
A. Là chất rắn, màu vàng, không tan trong nước
B. Tan tốn trong ethanol, không tan trong dầu hỏa
C. Tan ít trong ethanol, không tan trong benzene
D. Hóa hơi ở nhiệt độ khoảng 150 oC, dễ chảy lỏng ở nhiệt độ khoảng 70 oC
Câu 5. Chọn phát biểu sai về cách sơ cứu khi bị bỏng acid
A. Nhanh chóng rửa ngay với nước lạnh nhiều lần để làm giảm lượng acid bám trên da
B. Nếu acid đã bắn vào mắt thì úp mặt vào chậu nước sạch, mở mắt và chớp nhiều lần
C. Sau khi ngâm rửa bằng nước, tiến hành trung hòa acid bằng dung dịch NaHCO3 loãng
D. Nếu bị bỏng ở vùng mặt nhưng acid chưa bắn vào mắt thì mở mắt khi ngâm rửa
Câu 6. Muối sulfate nào dưới đây được dùng để sản xuất phân đạm?
A. Barium sulfate
B. Ammonium sulfate
C. Calcium sulfate
D. Magnesium sulfate
Câu 7. Câu nào sau đây diễn tả đúng tính chất hóa học của sulfur?
A. Sulfur có cả tính oxi hóa và tính khử
B. Sulfur không có tính oxi hóa và cả tính khử
C. Sulfur chỉ có tính khử
D. Sulfur chỉ có tính oxi hóa
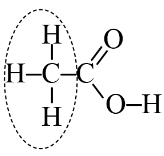
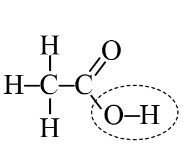
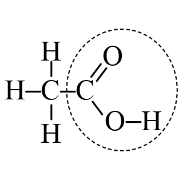
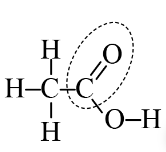
Câu 8. Trường hợp nào dưới đây khoanh đúng nhóm chức carboxylic acid của ethanoic acid?
A. | B. | C. | D. |
Câu 9. Phương pháp tách biệt nào được thể hiện trong hình dưới đây?
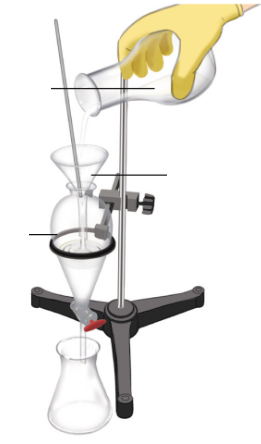
A. Phương pháp chiết
B. Phương pháp chưng cất
C. Phương pháp kết tinh
D. Phương pháp sắc kí
Câu 10. Biện pháp giảm thải sulfur dioxide ra khí quyển nào sau đây là đúng?
A. Thay thế nhiên liệu tái tạo bằng nhiên liệu thiên nhiên, nhiên liệu hóa thạch.
B. Xử lý khí thải nhà máy bằng các acid mạnh như H2SO4 đặc, HCl đặc.
C. Chuyển hóa sulfur dioxide thành chất ít gây ô nhiễm bằng đá vôi nghiền.
D. Dùng giấm ăn để biến đổi sulfur dioxide thành chất khác.
Câu 11. Phương pháp sắc kí bao gồm
A. Pha lỏng và pha rắn
B. Pha hấp phụ và pha dung môi
C. Phá chất tan và pha dung dịch
D. Pha tĩnh và pha động
Câu 12. Phân tử khối một chất có thể xác định dựa trên
A. công thức thực nghiệm
B. phổ khối lượng
C. phân tích nguyên tử
D. thành phần nguyên tố
Câu 13. Công thức đơn giản nhất của hợp chất C10H14N2 là
A. C5H7N2
B. CH7N
C. C3H7N2
D. C5H7N
Câu 14. Phổ MS của chất Y cho thây Y có phân tử khối bằng 60. Công thức phân tử nào dưới đây không phù hợp với Y?
A. C3H8O
B. C2H4O2
C. C3H7F
D. C2H8N2
Câu 15. Hiện tượng các chất có cấu tạo và tính chất hoá học tương tự nhau, chúng chỉ hơn kém nhau một hay nhiều nhóm metylen (–CH2–) được gọi là hiện tượng
A. Đồng phân
B. Đồng vị
C. Đồng khối
D. Đồng đẳng
Câu 16. Cặp chất nào sau đây là đồng đẳng của nhau?
A. C6H5Cl và C6H5CH2Cl
B. CH3C6H4Cl và C6H5Cl
C. CH3CH2OH và CH3OCH3
D. C6H5OH và C6H5CH2OH
Câu 17. Chọn câu đúng trong các câu sau
A. Tính chất của các hợp chất chỉ phụ thuộc vào loại nguyên tử trong phân tử và thứ tự các liên kết mà không phụ thuộc vào số lượng các nguyên tử.
B. Trong một phân tử hợp chất hữu cơ, thứ tự liên kết giữa các nguyên tử thay đổi nhưng vẫn đảm bảo hóa trị của các nguyên tử không đổi nên tính chất hóa học không đổi.
C. Các hợp chất hữu cơ có cùng số lượng nguyên tử các nguyên tố đều có tính chất hóa học tương tự nhau.
D. Cùng công thức phân tử, các nguyên tử liên kết với nhau theo đúng hóa trị nhưng thứ tự liên kết giữa các nguyên tử khác nhau sẽ tạo ra hợp chất khác nhau.
Câu 18. Công thức phân tử của chất có công thức cấu tạo đầy đủ như sau là ?
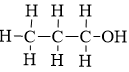
A. C3H6O
B. C3H8O
C. C3H10O
D. C3H8O2
Câu 19. Methadone là một loại thuốc dùng trong cai nghiện ma túy, nó thực chất cũng là một loại chất gây nghiện nhưng “nhẹ” hơn các loại ma túy thông thường và dễ kiểm soát hơn. Công thức cấu tạo của nó như hình dưới.
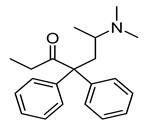
A. C21H27NO
B. C17H27NO
C. C21H29NO
D. C17H22NO
Câu 20. Nhóm chất nào sau đây gồm các chất đều tác dụng với dung dịch H2SO4 loãng?
A. Cu, Cu(OH)2
B. S, Mg
C. C, Mg(OH)2
D. Fe, Fe(OH)3
Câu 21. Cho 20 gam hỗn hợp Cu và Al phản ứng với dung dịch H2SO4 loãng, dư thấy thu được 13,44 lít khí (đktc). % theo khối lượng Al và Cu trong hỗn hợp lần lượt là
A. 44% và 66%.
B. 54% và 46%.
C. 50% và 50%.
D. 94% và 16%.
Câu 22. Chọn phát biểu sai về phân loại hợp chất hữu cơ
A. Hydrocarbon và dẫn xuất của hydrocarbon.
B. Hydrocarbon và hợp chất hữu cơ có nhóm chức.
C. Hydrocarbon thơm và hydrocarbon không thơm.
D. Hydrocarbon no, không no, thơm và dẫn xuất của hydrocarbon.
Câu 23. Chọn phát biểu đúng khi nói về thành phần các nguyên tố trong phân tử các hợp chất hữu cơ
A. Tất cả các nguyên tố trong tự nhiên đều có thể được tìm thấy trong thành phần hợp chất hữu cơ.
B. Một vài nguyên tố ít gặp hơn oxygen và nitrogen trong thành phần hợp chất hữu cơ là phosphorus, các halogen.
C. Oxygen, nitrogen, sulfur là những thành phần nguyên tố thường gặp.
D. Số lượng các nguyên tố thường gặp là nhiều.
Câu 24. Đốt cháy hoàn toàn chất A tạo thành CO2 và H2O. Trên phổ IR của A thầy có hấp thụ ở 1 720 cm-1 chứng tỏ trong phân tử chất A không thể có nhóm chức nào dưới đây?
A. Amine
B. Carboxylic acid
C. Ester
D. Aldehyde
Câu 25. Hỗn hợp X gồm các alkane: pentane (ts = 36,1oC), heptane (ts = 98,4oC), octane (ts = 125,7oC) và nonane (ts = 150,8oC). Có thể tách riêng các chất đó một cách thuận lợi bằng phương pháp nào sau đây?
A. Phương pháp kết tinh
B. Phương pháp chưng cất
C. Phương pháp sắc kí
D. Phương pháp chiết
Câu 26. Ngâm củ nghệ với ethanol nóng, sau đó lọc bỏ phần bã, lấy dung dịch đem cô để làm bay hơi bớt dung môi. Phần dung dịch còn lại sau khi cô được làm lạnh, để yên một thời gian rồi lọc lấy kết tủa curcumin màu vàng. Từ mô tả ở trên, hãy cho biết, người ta đã sử dụng các kĩ thuật tinh chế nào để lấy được curcumin từ củ nghệ.
A. Chiết, chưng cất và kết tinh.
B. Chưng cất và kết tinh
C. Chưng cất, kết tinh và sắc kí
D. Chiết và kết tinh
Câu 27. Glyoxal có thành phần phần trăm khối lượng các nguyên tố là: 41,4% C; 3,4% H và 55,2% O. Công thức nào dưới đây phù hợp với công thức thực nghiệm của glyoxal?Câu 28. Hình sau đây là phổ khối lượng của phân tử acetone. Hãy xác định phân tử khối của acetone. Biết phân tử khối của hợp chất này được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất
A. CHO
B. CH2O
C. CH2O2
D. C2H6O
Câu 28. Phân tích chất hữu cơ X chứa C, H, O ta có: nC : nH : nO = 1 : 3 : 1. Công thức đơn giản nhất của X là:
A. C6H12O4
B. C3H6O2
C. CH3O
D. C3H6O
B. PHẦN TỰ LUẬN (3 điểm)
Câu 1. (1 điểm) Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10% thu được 2,479 lít khí H2 (ở đkc). Tính khối lượng dung dịch thu được sau phản ứng.
Câu 2. (1 điểm) Lindane hay hexachlorane là chất có tác dụng trừ sâu mạnh, từng được sử dụng phổ biến trong nông nghiệp và làm dược phẩm (trị ghẻ, diệt chấy,…). Tuy nhiên, do là chất độc phân huỷ rất chậm trong tự nhiên nên vào năm 2009, hexachlorane đã bị đưa vào phụ lục cấm sản xuất và sử dụng của Công ước Stockholm về các chất ô nhiễm hữu cơ khó phân huỷ và bị cấm sử dụng tại 169 quốc gia trên thế giới. Thành phần phần trăm khối lượng của các nguyên tố có trong hexachlorane là: 24,78% C; 2,08% H và 73,14% Cl. Dựa vào phổ MS, xác định được phân tử khối của hexachlorane là 288 (ứng với 35Cl) hoặc 300 (ứng với 37Cl). Trong tự nhiên, 35Cl chiếm 75,77% số lượng nguyên tử còn 37Cl chiếm 24,23% số lượng nguyên tử.
a) Xác định công thức thực nghiệm của hexachlorane.
b) Xác định công thức phân tử của hexachlorane.
Câu 3 (1 điểm) a. Carboxylic acid Z là đồng phân cấu tạo của methyl acetate (CH3COOCH3). Viết công thức cấu tạo của Z.
b. X, Y là các chất đồng đẳng của Z. Viết công thức cấu tạo của X, Y biết rằng số nguyên tử carbon có trong phân tử mỗi chất X, Y đều nhỏ hơn số nguyên tử carbon có trong phân tử Z.
BÀI LÀM
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
BÀI LÀM
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
……….…………………………………………………………………………………………
TRƯỜNG THPT .............
HƯỚNG DẪN CHẤM KIỂM TRA HỌC KÌ 1 (2023 – 2024)
MÔN: HÓA HỌC 11 – CÁNH DIỀU
A. PHẦN TRẮC NGHIỆM: (7,0 điểm)
Mỗi câu trả lời đúng được 0,25 điểm.
1. A | 2. C | 3. D | 4. A | 5. D | 6. B | 7. A |
8. C | 9. A | 10. C | 11. D | 12. B | 13. D | 14. C |
15. D | 16. B | 17. D | 18. B | 19. A | 20. D | 21. B |
22. C | 23. B | 24. A | 25. B | 26. D | 27. A | 28. C |
B. PHẦN TỰ LUẬN: (3,0 điểm)
Câu | Nội dung đáp án | Biểu điểm |
Câu 1 (1 điểm) | Ta có: nFe = 0,1 mol Ta có: → Áp dụng định luật bảo toàn khối lượng: mhỗn hợp KL + → mdd sau phản ứng = mhỗn hợp KL + = 3,68 + 98 – 0,1 × 2 = 101,48g
|
0,25đ
0,25đ 0,25đ 0,25đ |
Câu 2 (1 điểm) | Nguyên tử khối trung bình của chlorine là:
a) Tỉ lệ về số nguyên tử carbon : hydrogen : chlorine có trong phân tử hexachlorane là: nC : nH : nCl = Vậy công thức thực nghiệm của X là CHCl. b) Tính với 35Cl, hexachlorane có phân tử khối 288: (CHCl)n = 288 hay 48n = 288, từ đó suy ra n = 6. Tương tự, với 37Cl, hexachlorane có phân tử khối 300: (CHCl)n = 300 hay 50n = 300, từ đó cũng suy ra n = 6. Vậy công thức phân tử của hexaclorane là C6H6Cl6. |
0,25
0,25 0,5
|
Câu 3 (1 điểm) | a. Công thức cấu tạo của Z: CH3CH2COOH b. X, Y là HCOOH và CH3COOH. | 0,5đ 0,5đ |
TRƯỜNG THPT .............
MA TRẬN ĐỀ KIỂM TRA HỌC KÌ 1 (2023 – 2024)
MÔN: HÓA HỌC 11 – KẾT NỐI TRI THỨC
CHỦ ĐỀ |
NỘI DUNG KIẾN THỨC | MỨC ĐỘ | Tổng số câu |
Điểm số | ||||||||
Nhận biết | Thông hiểu | Vận dụng | VD cao | |||||||||
TN | TL | TN | TL | TN | TL | TN | TL | TN | TL | |||
Nitrogen và sulfur
| Bài 7. Sulfur và sulfur dioxide | 2 |
| 2 |
|
|
|
|
| 4 | 0 | 1đ |
Bài 8. Sulfuric acid và muối sulfate | 2 |
| 3 |
|
| 1 |
|
| 5 | 1 | 2,25đ | |
Đại cương về hóa học hữu cơ | Bài 10. Hợp chất hữu cơ và hóa học hữu cơ | 2 |
| 3 |
|
|
|
|
| 5 | 0 | 1,25đ |
Bài 11. Phương pháp tách biệt và tinh chế hợp chất hữu cơ | 2 |
| 2 |
|
|
|
|
| 3 | 0 | 0,75đ | |
Bài 12. Công thức phân tử học chất hữu cơ | 1 |
| 4 |
|
|
|
| 1 | 5 | 1 | 2,25đ | |
Bài 13. Cấu tạo hóa học của hợp chất hữu cơ | 2 |
| 3 |
|
| 1 |
|
| 6 | 1 | 2,5đ | |
Tổng số câu TN/TL | 12 | 0 | 16 | 0 | 0 | 2 | 0 | 1 | 28 | 3 |
10 điểm | |
Điểm số | 3đ | 0đ | 4đ | 0đ | 0đ | 2đ | 0đ | 1đ | 7đ | 3đ | ||
Tổng số điểm | 3 điểm 30% | 4 điểm 30% | 2 điểm 20% | 1 điểm 10% | 10 điểm 100 % | |||||||
TRƯỜNG THPT .............
BẢN ĐẶC TẢ KĨ THUẬT ĐỀ KIỂM TRA HỌC KÌ 1 (2023 – 2024)
MÔN: HÓA HỌC 11 – KẾT NỐI TRI THỨC
Nội dung |
Đơn vị kiến thức |
Mức độ, yêu cầu cần đạt | Số ý TL/ Số câu hỏi TN | Câu hỏi | ||
TL | TN | TL | TN | |||
Nitrogen và sulfur
| Bài 7. Sulfur và sulfur dioxide | Nhận biết: - Nêu được trạng thái tự nhiên, tính chất vật lí của nguyên tố sulfur. |
|
2 |
|
Câu 1
Câu 4 |
Thông hiểu: - Trình bày được cấu tạo, tính chất hóa học cơ bản và ứng dụng của sulfur đơn chất và sulfur dioxide - Trình bày được sự hình thành sulfur dioxide do tác động của con người, tự nhiên, tác hại của sulfur dioxide và một số biện pháp làm giảm thiểu lượng sulfur dioxide thải vào không khí |
| 1
1 |
| Câu 7
Câu 10 | ||
Bài 8. Sulfuric acid và muối sulfate | Nhận biết: - Nêu được tính chất vật lí, cách bảo quản, sử dụng và nguyên tắc xử lí sơ bộ khi bỏng acid - Nêu được ứng dụng của một số muối sulfate quan trọng và nhận biết được ion S |
|
1 1
|
|
Câu 5 Câu 6
| |
Thông hiểu: - Trình bày được tính chất hóa học của dung dịch sulfuric acid |
| 3
|
|
Câu 20 Câu 2 Câu 21 | ||
Vận dụng: - Vận dụng kiến thức về sulfuric acid và muối sulfate để giải quyết bài tập liên quan. | 1 |
| Câu 1 |
| ||
Đại cương về hóa học hữu cơ
| Bài 10. Hợp chất hữu cơ và hóa học hữu cơ | Nhận biết: - Nêu được khái niệm chất hữu cơ và hóa học hữu cơ - Nêu được khái niệm nhóm chức và một số loại nhóm chức cơ bản |
|
1
1
|
|
Câu 3 Câu 8
|
Thông hiểu: - Phân loại được hợp chất hữu cơ, trình bày đặc điểm chung của các hợp chất hữu cơ - Sử dụng được bảng tín hiệu phổ hồng ngoại (IR) để xác định một số nhóm chức cơ bản |
| 2 1 |
| Câu 22 Câu 23 Câu 24 | ||
Bài 11. Phương pháp tách biệt và tính chế hợp chất hữu cơ | Nhận biết: - Nhận biết được các phương pháp tách biệt và tinh chế hợp chất hữu cơ |
|
2 |
|
Câu 9 Câu 11 | |
Thông hiểu: - Trình bày được nguyên tắc cách thức tiến hành các phương pháp tách biệt và tinh chế hợp chất hữu cơ.
|
|
2
|
| Câu 25 Câu 26 | ||
Bài 12. Công thức phân tử hợp chất hữu cơ | Nhận biết: - Nêu được khái niệm về công thức đơn giản nhất của hợp chất hữu cơ. |
2
|
|
Câu 12 Câu 13
| ||
Thông hiểu: - Sử dụng được kết quả phổ khối lượng (MS) để xác định phân tử khối của hợp chất hữu cơ - Lập được công thức phân tử hợp chất hữu cơ từ dữ liệu phân tích nguyên tố và phân tử khối |
|
1
2
|
|
Câu 14 Câu 27 Câu 28
| ||
Vận dụng cao: - Vận dụng phổ MS, thành phần phần trăm khối lượng, xác định công thức phân tử của chất |
1 |
Câu 2 |
| |||
Bài 13. Cấu tạo hóa học của hợp chất hữu cơ | Nhận biết: - Nêu được khái niệm chất đồng đẳng và dãy đồng đẳng; chất đồng đẳng, chất đồng phân dựa vào công thức cấu tạo cụ thể của các hợp chất hữu cơ |
| 2 |
|
Câu 15 Câu 16
| |
Thông hiểu: - Trình bày được nội dung thuyết cấu tạo hóa học trong hóa học hữu cơ - Xác định được công thức cấu tạo của một số hợp chất hữu cơ đơn giản (công thức cấu tạo đầy đủ, công thức cấu tạo thu gọn) |
| 1
2 |
| Câu 17 Câu 18 Câu 19 | ||
Vận dụng cao: - Vận dụng kiến thức về đồng đẳng, đồng phân để viết công thức cấu tạo của chất | 1 | Câu 3 |
| |||
Thêm kiến thức môn học
Đề thi Hóa học 11 kết nối tri thức, trọn bộ đề thi Hóa học 11 kết nối, đề thi cuối kì 1 Hóa học 11 KNTT: Đề
Giải bài tập những môn khác
Giải sgk lớp 11 KNTT
Giải sgk lớp 11 CTST
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều

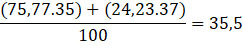
Bình luận