Đề cương ôn tập Hóa học 10 chân trời sáng tạo học kì 1 (P3)
Đề cương ôn tập môn Hóa học lớp 10 bộ sách Chân trời sáng tạo mới là tài liệu giúp các em ôn tập củng cố lại toàn bộ kiến thức được của môn Hóa học 10. Tài liệu bao gồm các kiến thức trọng tâm, giúp các bạn ôn tập lại lý thuyết và luyện tập các dạng bài khác nhau để chuẩn bị tốt cho kì thi cuối kì 1 sắp tới. Sau đây mời các em tham khảo đề cương chi tiết
A. KIẾN THỨC TRỌNG TÂM
CHỦ ĐỀ 3: LIÊN KẾT HÓA HỌC
1. Quy tắc octet
- Quy tắc Octet (bát tử): Trong quá trình hình thành liên kết hoá học, nguyên tử của các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có 8 electron tương ứng với khí hiếm gần nhất (hoặc 2 electron với khí hiếm helium).
Ví dụ: Vận dụng quy tắc octet trong sự tạo thành ion potassium (K+).
Nguyên tử potassium có 1 electron ở lớp ngoài cùng. Nếu mất đi 1 electron nguyên tử potassium sẽ đạt được cấu hình electron bền vững, giống với khí hiếm gần nhất là Ar.
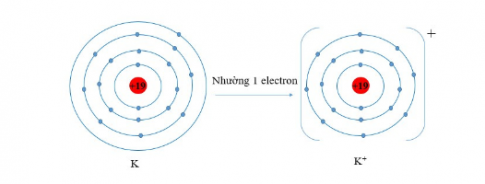
Viết gọn: K → K+ + 1e
2. Liên kết ion
- Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
- Liên kết ion thường được hình thành khi kim loại điển hình tác dụng với phi kim điển hình.
Ví dụ: Sự hình thành liên kết ion trong phân từ sodium chloride:
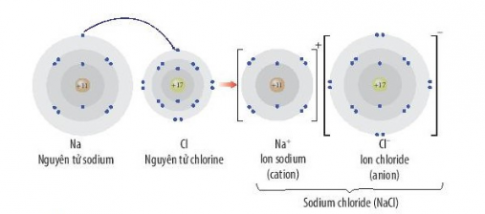
- Trong điều kiện thưởng, các hợp chất ion thường tồn tại ở trạng thái rắn, khó nóng chảy, khó bay hơi và không dẫn điện ở trạng thái rắn. Hợp chất ion thường dễ tan trong nước, tạo thành dung dịch có khả năng dẫn điện.
3. Liên kết cộng hóa trị
- Liên kết cộng hóa trị là liên kết được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron chung
+ Liên kết cộng hóa trị không phân cực là liên kết cộng hoá trị trong đó cặp electron chung không lệch về phía nguyên tử nào.
+ Liên kết cộng hóa trị phân cực là liên kết cộng hoá trị trong đó cặp electron chung lệch về phía nguyên tử có độ âm điện lớn hơn.
- Liên kết cho – nhận là một trường hợp đặc biệt của liên kết cộng hóa trị, trong đó cặp electron chung chỉ do một nguyên tử đóng góp.
Ví dụ: Sự tạo thành liên kết cho - nhận trong ion NH4+
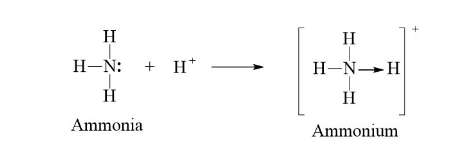
- Phân biệt liên kết cộng hóa trị phân cực và không phân cực
+ Liên kết cộng hóa trị không phân cực là liên kết cộng hóa trị trong đó cặp electron chung không lệch về phía nguyên tử nào.
Ví dụ: Liên kết cộng hóa trị trong các phân tử H2, Br2 là liên kết cộng hóa trị không phân cực.
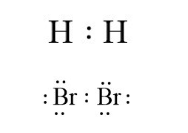
+ Liên kết cộng hóa trị phân cực là liên kết cộng hóa trị trong đó cặp electron chung lệch về phía nguyên tử có độ âm điện lớn hơn.
Ví dụ: Liên kết cộng hóa trị trong các phân tử HBr, H2O là liên kết cộng hóa trị phân cực.
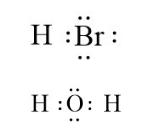
- Phân biệt loại liên kết trong phân tử dựa trên giá trị hiệu độ âm điện: Có thể dựa vào hiệu độ âm điện (∆χ) giữa hai nguyên tử tham gia liên kết để dự đoán loại liên kết giữa chúng.
- Liên kết ,
và năng lượng liên kết
+ Liên kết là loại liên kết cộng hóa trị được hình thành do sự xen phủ trục của hai orbital. Vùng xen phủ nằm trên đường nối tâm hai nguyên tử.
+ Liên kết là loại liên kết cộng hóa trị được hình thành do sự xen phủ bên của hai orbital. Vùng xen phủ năm hai bên đường nội tâm hai nguyên tử.
4. Liên kết hydrogen và tương tác van der waals
- Liên kết hydrogen
+ Liên kết hydrogen là một loại liên kết yếu, được hình thánh giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cập electron hóa trị chưa tham gia liên kết.
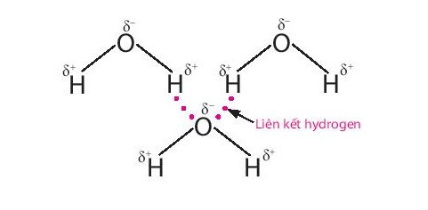
+ Liên kết hydrogen làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của nước.
- Tương tác Van der Waals
+ Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực được hình thành giữa các phân tử hay nguyên tử.
+ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.

Bình luận