Đề cương ôn tập Hóa học 10 chân trời sáng tạo học kì 1 (P1)
Đề cương ôn tập môn Hóa học lớp 10 bộ sách Chân trời sáng tạo mới là tài liệu giúp các em ôn tập củng cố lại toàn bộ kiến thức được của môn Hóa học 10. Tài liệu bao gồm các kiến thức trọng tâm, giúp các bạn ôn tập lại lý thuyết và luyện tập các dạng bài khác nhau để chuẩn bị tốt cho kì thi cuối kì 1 sắp tới. Sau đây mời các em tham khảo đề cương chi tiết
A. KIẾN THỨC TRỌNG TÂM
CHỦ ĐỀ 1: CẤU TẠO NGUYÊN TỬ
1. Thành phần của nguyên tử
- Nguyên tử có cấu tạo rỗng, gồm hạt nhân ở trung tâm và lớp vỏ là các electron chuyển động xung quanh hạt nhân. Khối lượng của nguyên tử gần bằng khối lượng hạt nhân.
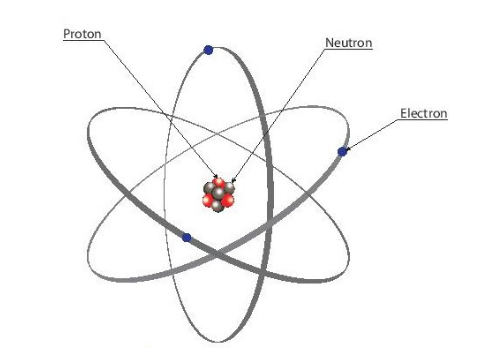
- Hạt nhân nguyên tử gồm 2 loại hạt có khối lượng gần bằng nhau:
+ Proton (p): Mang điện tích dương (+1)
+ Neutron (n): Không mang điện
- Electron (e) có khối lượng và mang điện tích âm
qe = - 1,602 × 10-19 C (coulomb). Dùng làm điện tích đơn vị, được quy ước là -1
me = 9,11 × 10-28g.
2. Nguyên tố hóa học
- Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số electron (E).
- Số khối (A) = số proton (P) + số neutron (N)
- Nguyên tố hóa học là tập hợp những nguyên tử cùng điện tích hạt nhân, mỗi nguyên tố hóa học có một số hiệu nguyên tử.
- Kí hiệu nguyên tử:
- Các đồng vị của một nguyên tố hóa học là những nguyên tử có cùng số proton (P), cùng số hiệu nguyên tử (Z), nhưng khác nhau về số neutron (N). Do đó, số khối (A) của chúng khác nhau.
- Nguyên tử khối là khối lượng tương đối của nguyên tử. Nguyên tử khối của một nguyên tử cho biết khối lượng của nguyên tử đó nặng gấp bao nhiêu lần đơn vị khối lượng nguyên tử (1 amu).
- Công thức tính nguyên tử khối trung bình của nguyên tố X:
Trong đó: là nguyên tử khối trung bình của X
Ai là nguyên tử khối đồng vị thứ i
ai là tỉ lệ % số nguyên tử đồng vị thứ i
3. Cấu trúc lớp vỏ electron của nguyên tử:
- Một số AO (Orbital nguyên tử) thường gặp: s, p, d, f. Các AO có hình dạng khác nhau: AO s có dạng hình cầu, AO p có dạng hình số tám nổi, AO d và f có hình dạng phức tạp.
- Trong nguyên tử, các electron được sắp xếp thành từng lớp (kí hiệu K, L, M, N, O, P, Q) từ gần đến xa hạt nhân, theo thứ tự từ lớp n = 1 đến n = 7.
- Mỗi lớp electron phân chia thành các phân lớp, được kí hiệu bằng các chữ cái viết thường: s, p, d, f. Các electron thuộc các phân lớp s, p, d và f được gọi tương ứng là các electron s, p, d và f. Các phân lớp s, p, d và f lần lượt có các số AO tương ứng 1, 3, 5 và 7.
- Nguyên lí vững bền: Ở trạng thái cơ bản, các electron trong nguyên tử chiếm lần lượt những orbital có mức năng lượng từ thấp đến cao: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p …
- Nguyên lí Pauli: Mỗi orbital chỉ chứa tối đa 2 electron và có chiều tự quay ngược nhau. Dựa vào nguyên lí Pauli, ta dễ dàng xác định được số AO và số electron tối đa trong mỗi lớp và phân lớp:
+ Số AO tối đa trong lớp n là n2 (n ≤ 4).
+ Số electron tối đa trong lớp n là 2n2 (n ≤ 4).
- Quy tắc Hund: Trong cùng một phân lớp chưa bão hòa, các electron sẽ phân bố vào các orbital sao cho số electron độc thân là tối đa.
- Cách viết cấu hình electron:
+ Bước 1: Xác định số electron của nguyên tử.
+ Bước 2: Các electron được phân bố theo thứ tự các AO có mức năng lượng tăng dần, theo các nguyên lí và quy tắc phân bố electron trong nguyên tử.
+ Bước 3: Viết cấu hình electron theo thứ tự các phân lớp trong một lớp và theo thứ tự của các lớp electron.
Ví dụ: K (Z = 19): Thứ tự mức năng lượng orbital: 1s22s22p63s23p64s1.
Cấu hình electron: 1s22s22p63s23p64s1 hoặc viết gọn là: [Ar]4s1.

Bình luận