Đáp án Hóa học 10 Kết nối bài 14 Ôn tập chương 3
Đáp án bài 14 Ôn tập chương 3. Bài giải được trình bày ngắn gọn, chính xác giúp các em học Hóa học 10 Kết nối tri thức dễ dàng. Từ đó, hiểu bài và vận dụng vào các bài tập khác. Đáp án chuẩn chỉnh, rõ ý, dễ tiếp thu. Kéo xuống dưới để xem chi tiết
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 14. ÔN TẬP CHƯƠNG 3
I. HỆ THỐNG HÓA KIẾN THỨC
Hoàn thành sơ đồ hệ thống hoá kiến thức sau:
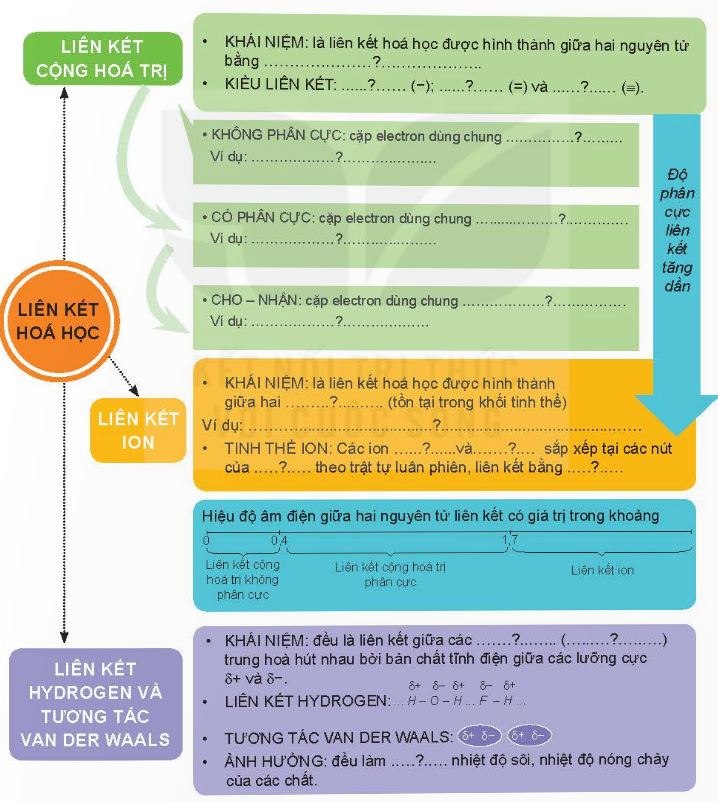
Giải nhanh:
(1) một hay nhiều cặp e dùng chung; (2) liên kết đơn; (3) liên kết đôi; (4) liên kết ba.
(5) nằm chính giữa 2 nguyên tử; (6) Cl2, Br2,…
(7) lệch về nguyên tử có ĐÂĐ lớn hơn; (8) H2O, CO, NH3,…
(9) do một nguyên tử đóng góp; (10) SO2, HNO3,…
(11) tinh thể ion; (12) NaCl
(13) ion mang điện tích trái dấu; (14) NaCl, NaF, CaCl2.
(15) âm; (16) dương; (17) mạng tinh thể; (18) lực hút tĩnh điện của chúng
(19) phân tử (hay nguyên tử)
(20) tăng
II. LUYỆN TẬP
Câu 1: Dãy các chất nào dưới đây mà tất cả các phân tử đều có liên kết ion?
A. Cl2, Br2, I2, HCl. B. Na2O, KCl, BaCl2, Al2O3.
C. HCl, H2O, NaCl, N2O D. MgO, H2SO4, H3PO4, HCl.
Giải nhanh:
B.
Câu 2: Dãy các chất nào dưới đây mà tất cả các phân tử đều có liên kết cộng hóa trị không phân cực?
A. N2, CO2, Cl2, H2 B. N2, Cl2, H2, HCl
C. N2, HI, Cl2, CH4 D. Cl2, O2, N2, F2.
Giải nhanh:
D.
Câu 3: Viết công thức cấu tạo và công thức Lewis của các phân tử sau: PH3, H2O, C2H6. Trong phân tử nào có liên kết phân cực mạnh nhất?
Giải nhanh:
- CTCT:
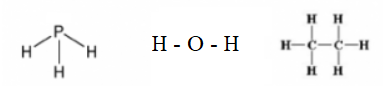
- CT Lewis:
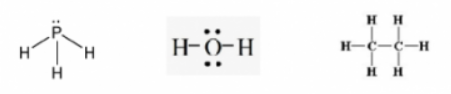
Câu 4:Dựa vào giá trị độ âm điện của các nguyên tử trong Bảng 6.2, xác định loại liên kết trong phân tử các chất: CH4, CaCl2, HBr, NH3.
Giải nhanh:
- CH4, NH3: liên kết CHT không phân cực
- CaCl2: liên kết ion
- HBr: liên kết CHT phân cực
Câu 5: Cho dãy các oxide sau: Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7.
a) Độ phân cực của các liên kết trong dãy các oxide trên thay đổi thế nào?
b) Dựa vào giá trị độ âm điện của các nguyên tố trong Bảng 6.2, cho biết loại liên kết (ion, cộng hóa trị phân cực, cộng hóa trị không phân cực) trong từng phân tử oxide.
Giải nhanh:
a) Tăng dần.
b) Na2O, MgO, Al2O3: liên kết ion
SiO2, P2O5: liên kết CHT phân cực.
SO3, Cl2O7: liên kết CHT không phân cực.
Câu 6: a) Cho dãy các phân tử: C2H6, CH3OH, NH3. Phân tử nào trong dãy có thể tạo liên kết hydrogen? Vì sao?
b) Vẽ sơ đồ biểu diễn liên kết hydrogen giữa các phân tử đó.
Giải nhanh:
a) CH3OH, NH3. Vì chứa O và N có độ âm điện lớn và cặp e chưa liên kết.
b)
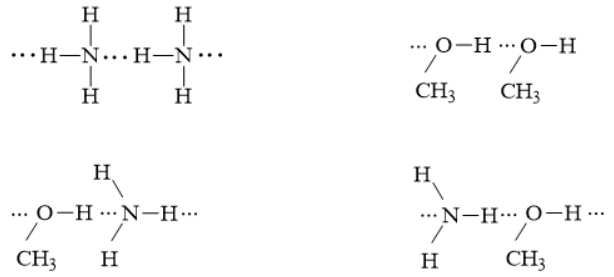
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây

Bình luận