5 phút giải Hóa học 11 Chân trời sáng tạo trang 99
5 phút giải Hóa học 11 Chân trời sáng tạo trang 99. Giúp học sinh nhanh chóng, mất ít thời gian để giải bài. Tiêu chi bài giải: nhanh, ngắn, súc tích, đủ ý. Nhằm tạo ra bài giải tốt nhất. 5 phút giải bài, bằng ngày dài học tập.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
CHƯƠNG 5. DẪN XUẤT HALOGEN - ALCOHOL - PHENOL
BÀI 16: ALCOHOL
PHẦN I. HỆ THỐNG CÂU HỎI, BÀI TẬP TRONG SGK
Một số loài thực vật như tràm, bạc hà, hoa hồng,... thường có mùi thơm dễ chịu và đặc trưng, vì trong thành phần hóa học chứa hợp chất menthol, terpinen - 4 - ol hoặc geraniol,...là các alcohol. Alcohol là gì?Alcohol có tính chất vật lí, hóa học nào và được ứng dụng trong lĩnh vực gì?
1. KHÁI NIỆM VÀ CẤU TRÚC
Bài 1: Quan sát hình 16.1 cho biết trong các hợp chất hữu cơ đã nêu có nhóm chức đặc trưng nào?
Bài 2: Quan sát hình 16.1 và hình 16.2 cho biết nguyên tử carcbon liên kết với nhóm chức hydroxy có đặc điểm gì? Cách xác định bậc alcohol như thế nào?
Bài 3: Quan sát hình 16.3, Nêu đặc điểm liên kết trong phân tử methanol, ethanol
2. ĐỒNG PHÂN VÀ DANH PHÁP
Bài 1: Quan sát bảng 16.1 cho biết cách xác định mạch carbon chính và thứ tự của các nguyên tử carbon trong phân tử alcohol
Bài 2: Viết công thức cấu tạo và gọi tên các đồng phân alcohol có công thức phân tử C5H12O
Bài 3: Viết công thức cấu tạo và gọi tên các đồng phân alcohol có công thức phân tử C5H12O
3. TÍNH CHẤT VẬT LÝ
Bài 1: Biết nhiệt độ sôi của ethanol là 78,3oC, propane là -42,1oC và dimethyl ether là -24,8oC. Giải thích sự khác biệt đó.
Bài 2: Từ thông tin bảng 16.2 và hình 16.4 cho biết khả năng hòa tan trong nước của alcohol. Độ tan và nhiệt độ sôi của alcohol thay đổi như thế nào theo chiều tăng khối lượng phân tử
4. TÍNH CHẤT HOÁ HỌC
Bài 1: Dựa vào độ âm điện, nêu nguyên nhân sự gây ra sự phân cực về phía nguyên tử oxygen của hai liên kết C - O và O - H
Bài 2: Trong phản ứng với sodium liên kết nào trong phân tử alcohol bị phân cắt?
Bài 3: Viết phương trình hóa học của phản ứng: CH3CH2CH2OH + K →
Bài 4: Hỗn hợp methanol và ethanol có thể cấu tạo bao nhiêu ether nhờ xúc tác dung dịch H2SO4 đặc. đun nóng?
Bài 5: Viết phương trình hóa học của phản ứng tạo thành alkene từ propan - 1 - ol ở điều kiện thích hợp.
Bài 6: Tiến hành thí nghiệm 1 quan sát hiện tượng.
Bài 7: Viết phương trình hóa học của phản ứng oxi hóa propan - 1 - ol bằng CuO tạo thành aldehyde
Bài 8: Tiến hành thí nghiệm 2, quan sát hiện tượng ở hai ống nghiệm (1) và (2) viết phương trình hóa học của phản ứng xảy ra ở bước 2
Bài 9: Trình bày phương pháp hóa học nhận biết hai chất methyl alcohol và ethylene glycol.
5. ỨNG DỤNG VÀ ĐIỀU CHẾ
Bài 1: Đọc thông tin về những ứng dụng của alcohol, nhận xét vai trò của alcohol trong đời sống, sản xuất.
Bài 2: Nêu ý kiến của em về thực trạng xã hội trong cách sử dụng rượu bia hiện nay. Làm thế nào để bảo vệ sức khỏe bản thân, gia đình, cộng đồng liên quan đến đồ uống có cồn.
Bài 3: Dựa trên tính chất nào để sử dụng methanol và ethanol làm nhiên liệu thay thế cho động cơ đốt trong
Bài 4: Có những phương pháp phổ biến nào để điều chế ethanol
Bài 5: Trong nhiều gia đình, thường ngâm các loại thảo dược như củ đinh lăng, tỏi, gừng, nhân sâm, trái nhàu,... với rượu để sử dụng. Phương pháp trên ứng dụng tính chất nào của ethanol vào đời sống?
BÀI TẬP
Bài 1: Viết phương trình hóa học của các phản ứng xảy ra theo sơ đồ sau:
Bài 2: Khi chưng cất rượu gạo theo phương pháp nấu rượu truyền thống, tại sao không nên đun sôi quá mạnh?
Bài 3: Theo hướng dẫn của Tổ chức Y tế Thế giới (WHO) về cách pha chế nước rửa tay khô bằng alcohol, nguyên liệu cần có: isopropyl alcohol 99,8% hoặc ethyl alcohol 96o, bộ hydrogen peroxide 3%, glycerol 98% và nước cất. Thành phần % theo thể tích các chất như sau:
- Isopropyl alcohol 75,15% hoặc ethyl alcohol 83,33% có tác dụng khử trùng
- Glycerol 1,45% giữ ẩm da tay
- Hydrogen peroxide 4,17%, loại bỏ các bào vi khuẩn nhiễm có trong dung dịch
- Thành phần còn lại là nước cất hoặc nước đun sôi để nguội
Mô tả cách thực hiện và pha chế 5 lít nước rửa tay khô từ nguyên liệu trên (có thể thêm một ít hương liệu hoặc tinh dầu để giảm bớt mùi alcohol và tạo cảm giác dễ chịu)
Một số loài thực vật như tràm, bạc hà, hoa hồng,... thường có mùi thơm dễ chịu và đặc trưng, vì trong thành phần hóa học chứa hợp chất menthol, terpinen - 4 - ol hoặc geraniol,...là các alcohol. Alcohol là gì?Alcohol có tính chất vật lí, hóa học nào và được ứng dụng trong lĩnh vực gì?
PHẦN II. 5 PHÚT TRẢ LỜI CÂU HỎI, BÀI TẬP TRONG SGK
1. KHÁI NIỆM VÀ CẤU TRÚC
Bài 1:
(-OH)
Bài 2:
Đặc điểm: nguyên tử carbon no
Bậc của alcohol = bậc của nguyên tử C liên kết với nhóm -OH.
Bài 3:
Menthol là bậc 2
Terpinen - 4 - ol là bậc 3
Geraniol là bậc 1
2. ĐỒNG PHÂN VÀ DANH PHÁP
Bài 1:
Mạch chính là mạch carbon dài nhất có chứa nhóm -OH
Đánh số thứ tự nguyên tử C mạch chính bắt đầu từ phía gần nhóm -OH hơn
Bài 2:
Đồng phân | Tên gọi |
CH3 -CH2-CH2-CH2-CH2-OH | n-Pentane – 1- ol |
| 3 – metyl butan – 1 – ol |
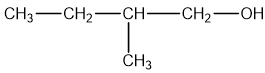
| 2 –metylbutan – 1 – ol |
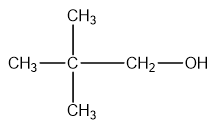
| 2,2 – đimetylpropan – 1- ol |
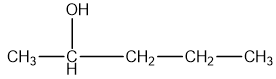
| pentan – 2 – ol |
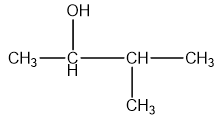
| 3 – metylbutan – 2- ol |
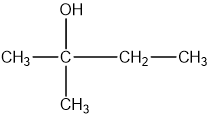
| 2 – metyl butan – 2- ol |
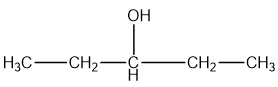
| pentan – 3 – ol |
Bài 3:
Đồng phân | Tên gọi |
CH3 -CH2-CH2-CH2-CH2-OH | Pentan-1-ol |
| 2-Methylbutan-1-ol |
| 3-Methylbutan-1-ol |
| 2,2-Dimethylpropan-1-ol |
| pentan – 2 – ol |
| 3-Methylbutan-2-ol |
| 2-Methylbutan-2-ol |
| pentan – 3 – ol |
3. TÍNH CHẤT VẬT LÝ
Bài 1:
Do ethanol tạo được liên kết hydro giữa các phân tử ethanol với nhau và giữa các phân tử ethanol với nước.
Bài 2:
Các alcohol từ C1 đến C3 tan vô hạn trong nước.
Nhiệt độ sôi tăng khi phân tử khối tăng
Độ tan giảm khi số Carbon tăng (phân tử khối tăng)
4. TÍNH CHẤT HOÁ HỌC
Bài 1:
Do độ âm điện của O > độ âm điện của C, H --> cặp electron dùng chung lệch về phía O --> liên kết C - O và O - H phân cực về phía nguyên tử O
Bài 2
liên kết O - H
Bài 3:
2CH3CH2CH2OH + 2K → 2CH3CH2CH2OK + H2
Bài 4:
3 ether.
Bài 5:
C3H7OH →H2SO4đ,170o C3H6 + H2O
Bài 6:
Hiện tượng: ngọn lửa màu xanh, toả nhiều nhiệt
PTHH: C2H5OH + 3O2 →to 2CO2 + 3H2O
Bài 7:
CH3CH2CH2OH + CuO →to CH3CH2CHO + Cu + H2O
Bài 8:
Hiện tượng: tủa xanh lam nhạt (Cu(OH)2)
PTHH: CuSO4 + 2NaOH → Cu(OH)2↓(xanh) + Na2SO4 (PTHH ở bước 2)
- gylycerol vào ống 1: Kết tủa tan tạo thành phức màu xanh lam
PTHH: 2C3H5(OH)3 + Cu(OH)2→ [C3H5(OH)2O]2Cu + 2H2O
- ethanol vào ống 2: không có hiện tượng, kết tủa không tan.
Bài 9:
Cho hai mẫu thử tác dụng với dd Cu(OH)2, mẫu thử nào làm kết tủa tan dần thành dung dịch màu xanh thì chính là C2H4(OH)2
5. ỨNG DỤNG VÀ ĐIỀU CHẾ
Bài 1:
- Dùng làm rượu, nước giải khát.
- Methanol: sản xuất formaldehyde và phụ gia nhiên liệu.
- Ethanol: đồ uống có cồn, phụ gia nhiên liệu, dung môi.
- Isopropyl alcohol làm dung môi cho sơn và các quá trình hóa học.
- propan - 1 - ol, butan - 1 - ol và isobutyl alcohol để sử dụng làm cồn tẩy rửa cho da
- Ethylene glycol thường được dùng làm chất chống đông cho ô tô và là một thành phần trong chất lỏng thủy lực, mực in và dung môi sơn.
Bài 2:
Thực trạng.
- Việt Nam đứng thứ 2 khu vực, 10 Châu Á và thứ 29 thế giới về việc sử dụng rượu.
- Hầu như trên mỗi bàn tiệc, mỗi buổi liên hoan, mỗi cuộc gặp gỡ đều có sử dụng rượu.
- Hiện tượng uống rượu bia có ở nữ giới
- Ở các dân tộc miền núi, hiện tượng uống rượu càng phổ biến
- Hiện tượng uống rượu xuât hiện cả trong môi trường học đường
Biện pháp
- Tuyên truyền, giáo dục mọi người biết sử dụng rượu đúng cách, đúng mức, có nhận thức đúng đắn về tác hại của rượu.
- Có biện pháp cai nghiện đúng
- Nâng cao hiểu biết và nhận thức của giới trẻ trong việc sử dụng rượu
Bài 3:
Do phản ứng toả nhiều nhiệt, sản phẩm sinh ra ít gây ảnh hưởng xấu đến môi trường
Bài 4:
Phương pháp tổng hợp
Phương pháp sinh hóa
Bài 5:
Khả năng hoà tan nhiều chất hữu
BÀI TẬP
Bài 1:
(1) C6H12O6 → C2H5OH + CO2 (enzyme)
(2) C2H5OH + 3O2 → 2CO2 + 3H2O (t0)
(3) CH2=CH2 + H2O → C2H5OH (H2SO4,to)
(4) C2H5OH + CuO → CH3CHO + Cu + H2O(to)
(5) C2H5OH → CH2=CH2 + H2O (H2SO4,to)
Bài 2:
Vì khi đun ở nhiệt độ cao, thì nước cũng bay hơi --> Hơi nước lẫn hơi rượu --> nồng độ rượu thấp
Bài 3:
- Isopropyl alcohol 3,7525 lít hoặc ethyl alcohol 4,1665 lít
- Glycerol 0,0725 lít
- Hydrogen peroxide 0,2085 lít
- Nước cất hoặc nước đun sôi để nguội.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
giải 5 phút Hóa học 11 Chân trời sáng tạo, giải Hóa học 11 Chân trời sáng tạo trang 99, giải Hóa học 11 CTST trang 99
Giải bài tập những môn khác
Giải sgk lớp 11 KNTT
Giải sgk lớp 11 CTST
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều


Bình luận