5 phút giải Hóa học 11 Chân trời sáng tạo trang 74
5 phút giải Hóa học 11 Chân trời sáng tạo trang 74. Giúp học sinh nhanh chóng, mất ít thời gian để giải bài. Tiêu chi bài giải: nhanh, ngắn, súc tích, đủ ý. Nhằm tạo ra bài giải tốt nhất. 5 phút giải bài, bằng ngày dài học tập.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
CHƯƠNG 4. HYDROCACBON
BÀI 13: HYDROCARBON KHÔNG NO
PHẦN I. HỆ THỐNG CÂU HỎI, BÀI TẬP TRONG SGK
Trái cây chín sinh ra ethylene và ethylene sinh ra tiếp tục kích thích trái cây xung quanh nhanh chín. Do vậy để những trái xang bên cạnh các trái chín cũng là cách để các trái xanh nhanh chín hơn.
Ethylene là một trong các hydrocarbon không no. Hydrocarbon không no là gì? Chúng có cấu tạo, tính chất và ứng dụng trong những lĩnh vực nào?
1. KHÁI NIỆM VỀ ALKENE VÀ ALKYNE
Bài 1: So sánh đặc điểm cấu tạo của các phân tử alkene, alkyne và alkane.
Bài 2: Giải thích tại sao trong các phân tử alkene, alkyne và alkane có cùng số nguyên tử carbon thì số nguyên từ hydrogen lại giảm dần
2. DANH PHÁP ALKENE VÀ ALKYNE
Bài 1: Viết công thức cấu tạo các alkene và alkyne sau
a) but - 2 - ene
b) 2-methylpropene
c) pent - 2- yne
Bài 2: Hãy nhận xét cách đánh số nguyên tử Carbon trên mạch chính của phân tử alkene và alkyne.
3. ĐỒNG PHÂN HÌNH HỌC
Bài 1: Vì sao các alkyne không có đồng phân hình học?
Bài 2: Nêu điều kiện để một alkene có đồng phân hình học
Bài 3: Viết công thức các đồng phân hình học của pent - 2 - ene và gọi tên các đồng phân hình học
4. TÍNH CHẤT VẬT LÝ
Bài 1: Vì sao nhiệt độ nóng chảy và nhiệt độ sôi của các alkene, alkyne tăng dần khi số nguyên tử carbon trong phân tử tăng
5. TÍNH CHẤT HOÁ HỌC
Bài 1: Khi tham gia phản ứng cộng hydrogen liên kết nào trong phân tử alkene, alkyne bị phá vỡ. Giải thích
Bài 2: Tại sao phải dẫn khí đi qua ống nghiệm có nhánh đựng dung dịch NaOH trong thí nghiệm 1 (hình 13.5)
Bài 3: Viết phương trình hóa học của phản ứng điều chế và thử tính chất C2H4 trong thí nghiệm 1
Bài 4: Viết phương trình hóa học của phản ứng điều chế C2H2 trong phòng thí nghiệm 2
Bài 5: Nhận xét và giải thích sự biến đổi màu sắc của nước bromine trong 2 thí nghiệm
Bài 6: Bên cạnh sản phẩm chính 1,1 - dibromoethane phản ứng giữa bromoethane và HBr còn tạo sản phẩm phụ nào?
Bài 7: Propyne phản ứng với nước trong điều kiện tương tự như acetylene. Viết phương trình phản ứng minh họa.
Bài 8: Nhận xét sự biến đổi màu sắc của dung dịch KMnO4 trong hai thí nghiệm. Ống nghiệm nào thu được dung dịch trong suốt sau thí nghiệm. Giải thích
Bài 9: Propylene cũng bị oxi hóa bởi dung dịch thuốc tím tương tự như ethylene. Viết phương trình hóa học của phản ứng
Bài 10: Hãy so sánh lượng nhiệt tỏa ra nếu đốt cháy C2H4 và C2H2 với cùng số mol bằng nhau
Bài 11: Viết phương trình hóa học của phản ứng giữa alkyne có nguyên tử hydrogen linh động, phân tử chứa 4 nguyên tử Carbon với dung dịch AgNO3 trong ammonia
Bài 12: Trình bày bài phương pháp hóa học để phân biệt but - 1 - yne và but - 2 - yne
6. ỨNG DỤNG VÀ CÁCH ĐIỀU CHẾ ALKENE, ALKYNE
Bài 1: Tại sao acetylene được dùng làm nhiên liệu trong đèn xì oxy - acetylene mà không dùng ethylene
Bài 2: Vì sao không được dùng nước dập tắt đám cháy có mặt đất đèn (có thành phần chính là CaC2)
BÀI TẬP
Bài 1: Viết công thức cấu tạo và gọi tên các alkene, alkyne có 4 nguyên tử Carbon. Trong phân tử alkene nào có đồng phân hình học? Gọi tên các đồng phân hình học đó.
Bài 2: Viết công thức phân tử của
a) propene
b) 2 - methylbut - 1 - ene
c) but - 1 - yne
d) cis - but - 2 - ene
Bài 3: Viết công thức cấu tạo sản phẩm chính của các phản ứng sau:
a) 2 - methylbut - 2 - en tác dụng với hydrogen chloride.
b) but - 1 - yne tác dụng với nước có xúc tác Hg2+ ở 80oC
PHẦN II. 5 PHÚT TRẢ LỜI CÂU HỎI, BÀI TẬP TRONG SGK
Hydrocarbon không no là những hydrocarbon trong phân tử có liên kết đôi C=C hoặc liên kết ba C≡C hoặc cả hai loại liên kết đó.
Tính chất: phản ứng cộng
Ứng dụng: dùng vào hàn xì (acetylen) hay tổng hợp các dẫn xuất của hydrocarbon
1. KHÁI NIỆM VỀ ALKENE VÀ ALKYNE
Bài 1:
| alkene | alkyne | alkane |
Đặc điểm cấu tạo | C=C | C≡C | C - H, C - C |
Bài 2:
Do carbon có hóa trị 4 nên khi hình thành liên kết C=C, C≡C thì số lượng nguyên tử H liên kết với C giảm
2. DANH PHÁP ALKENE VÀ ALKYNE
Bài 1:
a) CH3-CH=CH-CH3
b) 2 (CH3)2C=CH2
c) CH3–C≡ C – CH2–CH3
Bài 2:
Số chỉ vị trí liên kết bội mang số nhỏ nhất
3. ĐỒNG PHÂN HÌNH HỌC
Bài 1:
Do không có nối đôi
Bài 2:
Mỗi nguyên tử carbon của liên kết đôi đều phải liên kết với hai nguyên tử hoặc nhóm nguyên tử khác nhau.
Bài 3:
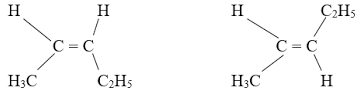
Cis - pent - 2 - ene ; trans - pent - 2 - ene
4. TÍNH CHẤT VẬT LÝ
Bài 1:
Vì số carbon tăng thì phân tử khối tăng → lực Van der Waals tăng
5. TÍNH CHẤT HOÁ HỌC
Bài 1:
Liên kết π vì kém bền
Bài 2:
Vì NaOH có vai trò giữ lại SO2 đảm bảo C2H4 thu được không bị lẫn SO2
Bài 3:
C2H5OH → C2H4 + H2O (Xúc tác: H2SO4 đặc, nhiệt độ 170 độ C)
C2H4 + Br2 → C2H4Br2
Vàng cam không màu
Bài 4:
CaC2 + 2H2O → C2H2 + Ca(OH)2
Bài 5:
Hiện tượng: mất màu dung dịch. Do liên kết π ở nối đôi, nối ba của alkene, alkyne kém bền vững.
Bài 6:
CH2Br - CHBr
Bài 7:
CH3 - C ≡ C- H + HOH →HgSO4,to [CH3 - C(OH) = CH2] → CH3−CO−CH3
(Kém bền)
Bài 8:
TN 3: dung dịch trong suốt
TN 4: dung dịch trong suốt
Do KMnO4 là chất oxi hoá mạnh, alkene, alkyne có liên kết bội kém bền nên có khả năng tham gia phản ứng oxi hoá - khử
Bài 9:
3CH2=CH–CH3 + 4H2O + 2KMnO4 →to 3OH-CH2–CH(OH)– CH3 + 2MnO2 + 2KOH
Bài 10:
Lượng nhiệt tỏa ra từ ethylene nhiều hơn acetylene
Bài 11:
CH≡C−CH2−CH3 + [Ag(NH3)2]OH → CAg≡C−CH2−CH3 + NH4NO3
Bài 12:
Thuốc thử | CH≡C-CH2-CH3 | CH3-C≡C-CH3 |
AgNO3/NH3 | Kết tủa vàng | không hiện tượng |
6. ỨNG DỤNG VÀ CÁCH ĐIỀU CHẾ ALKENE, ALKYNE
Bài 1:
Nhiệt lượng toả ra khi đốt cháy acetylene gần gấp đôi so ethylene
Bài 2:
Do CaC2 tác dụng được với nước tạo thành C2H2, C2H2 cháy được trong không khí ở nhiệt độ cao và toả nhiều nhiệt
BÀI TẬP
Bài 1:
Đồng phân | Tên gọi |
CH2 = CH – CH2 – CH3 | but – 1 – ene |
CH3 – CH = CH – CH3 | but – 2 – ene |
CH2=C(CH3)−CH3 | 2−methylprop−1−ene |
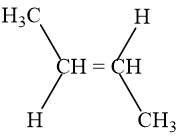
Trong đó but – 2 – ene có đồng phân hình học:
Đồng phân | Tên gọi |
| Cis – but – 2 - ene |
| Trans – but – 2 – ene |
Bài 2:
a) CH2=CH−CH3
b)

c) CH≡C−CH2−CH2−CH3
d)

Bài 3
a) CH3-CCl(CH3)-CH2-CH3(sản phẩm chính)
b) CH3–CO-CH2– CH3
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
giải 5 phút Hóa học 11 Chân trời sáng tạo, giải Hóa học 11 Chân trời sáng tạo trang 74, giải Hóa học 11 CTST trang 74
Giải bài tập những môn khác
Giải sgk lớp 11 KNTT
Giải sgk lớp 11 CTST
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều


Bình luận