5 phút giải Hóa học 10 Chân trời sáng tạo trang 55
5 phút giải Hóa học 10 Chân trời sáng tạo trang 55. Giúp học sinh nhanh chóng, mất ít thời gian để giải bài. Tiêu chi bài giải: nhanh, ngắn, súc tích, đủ ý. Nhằm tạo ra bài giải tốt nhất. 5 phút giải bài, bằng ngày dài học tập.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 9. LIÊN KẾT ION
PHẦN I. HỆ THỐNG CÂU HỎI, BÀI TẬP TRONG SGK
Hơn 50% dược phẩm sử dụng trong y tế được sản xuất dưới dạng muối với mục đích thúc đẩy sự hấp thu các dược chất vào máu, tăng cường hiệu quả điều trị. Trong đó, thường gặp nhất là các muối hydrochloride, sodium hoặc sulfate.
Muối thường là các hợp chất chứa liên kết ion. Liên kết ion là gì?
1. ION VÀ SỰ HÌNH THÀNH LIÊN KẾT ION
Thảo luận 1: Quan sát hình 9.1 nhận xét số electron trên lớp vỏ với số proton trong hạt nhân của mỗi ion tạo thành.
Thảo luận 2: Trình bày cách tính điện tích của các ion thu được khi nguyên tử nhường hoặc nhận thêm electron ở hình 9.1.
Thảo luận 3: Ion Na + và O 2- thu được có bền vững về mặt hóa học không? Chúng có cấu hình electron giống cấu hình electron nguyên tử của nguyên tố nào.
Thảo luận 4: Trong các nguyên tố kim loại và phi kim, nguyên tử của những nguyên tố nào có xu hướng tạo thành cation hoặc anion? Giải thích.
Thảo luận 5: Quan sát hình 9.2, hãy trình bày sự hình thành liên kết ion trong phân tử NaCl khi sodium tác dụng với chlorine.
Thảo luận 6: Các ion Na + và Cl - có cấu hình electron nguyên tử của các khí hiếm tương ứng nào?
Luyện tập: Trình bày sự hình thành liên kết ion trong phân tử MgO khi magnesium tác dụng với oxygen.
2. TINH THỂ ION
Thảo luận 7: Quan sát hình 9.3 cho biết:
a) Tinh thể NaCl có cấu trúc của hình khối nào
b) Các ion Na + và Cl - phân bố trong tinh thể như thế nào?
c) Xung quanh mỗi loại ion có bao nhiêu ion ngược dấu gần nhất.
Thảo luận 8: Em hiểu thế nào về tinh thể ion?
Thảo luận 9: Quan sát các bước trong hình 9.4 cho biết cần bao nhiêu thanh nối và khối cầu mỗi loại lắp ráp thành mô hình một ô mạng tinh thể NaCl.
Vận dụng: Ion Na+ đóng vai trò rất quan trọng trong việc điều hòa huyết áp của cơ thể. Tuy nhiên, nếu cơ thể hấp thụ một lượng lớn ion này sẽ dẫn đến các vấn đề về tim mạch và thận. Các nhà khoa học khuyến cáo lượng ion Na+ nạp vào cơ thể nên thấp hơn 2300 mg, nhưng không ít hơn 500 mg mỗi ngày đối với một người lớn để đảm bảo sức khỏe.
Giả sử, nếu một người sử dụng 5,0 g muối ăn mỗi ngày thì lượng ion Na+ mà người ấy nạp vào cơ thể có vượt mức giới hạn cho phép không?
BÀI TẬP
Câu 1: Ion Mg 2+ có cấu hình eletron giống cấu hình electron của khí hiếm nào
A. Helium B. Neon C. Argon D. Krypton
Câu 2: Cho các ion sau: Ca2+, F-, Al3+ và N3-. Số ion có cấu hình electron của khí hiếm neon là
A. 4 B. 2 C. 1 D. 3
Câu 3: Potasssium và magnesium là các nguyên tố thiết yếu đối với cơ thể sinh vật sống
a) Viết cấu hình electron của các ion được tạo thành từ nguyên tử của các nguyên tố này. Chúng có cấu hình electron của những nguyên tử khí hiếm nào?
b) Có hợp chất ion nào chỉ tạo bởi các ion trên với nhau không? Vì sao?
Câu 4: Hoàn thành những thông tin còn thiếu trong bảng sau:

Câu 5: Sodium oxide (Na2O ) có trong thành phần thủy tinh và các sản phẩm gốm sứ. Trình bày sự hình thành liên kết ion trong phân tử sodium oxide.
PHẦN II. 5 PHÚT TRẢ LỜI CÂU HỎI, BÀI TẬP TRONG SGK
Được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
1. ION VÀ SỰ HÌNH THÀNH LIÊN KẾT ION
Thảo luận 1:
- Ion sodium: electron ở lớp vỏ ít hơn số proton trong hạt nhân.
- Ion oxide: electron ở lớp vỏ nhiều hơn số proton trong hạt nhân.
Thảo luận 2:
Điện tích ion = số đơn vị điện tích hạt nhân – số electron của ion
Thảo luận 3:
Bền vững về mặt hóa học và có cấu hình giống với Ne.
Thảo luận 4:
- Kim loại dễ nhường electron ⇒ Tạo thành cation.
- Phi kim dễ nhận electron ⇒ Tạo thành anion.
Thảo luận 5:
- Na nhường đi 1 electron để trở thành ion mang điện tích dương và Cl nhận 1 electron từ nguyên tử Na trở thành ion mang điện tích âm.
- Các ion Na+ và Cl- hút nhau tạo thành liên kết trong phân tử NaCl.
- PTHH: 2Na + Cl2 → 2NaCl.
Thảo luận 6:
- Ion Na+ giống cấu hình Ne.
- Ion Cl- giống cấu hình Ar.
Luyện tập:
- Mg có xu hướng nhường 2 electron để đạt cấu hình electron của khí hiếm.
- O có xu hướng nhận 2 electron để đạt cấu hình electron của khí hiếm.
- Hai ion là Mg2+ và O2- liên kết với nhau tạo thành phân tử MgO
2. TINH THỂ ION
Thảo luận 7:
a) Hình khối lập phương dạng rỗng.
b) Được phân bố luân phiên đều đặn trên các đỉnh của các hình lập phương.
c) - Một ion Na + được bao phủ bởi 6 ion Cl -
- Một ion Cl - được bao phủ bởi 6 ion Na +
Thảo luận 8:
Chúng là chất rắn gồm các ion liên kết với nhau bằng lực hút tĩnh điện thành một mạng tinh thể đều đặn.
Thảo luận 9
48 và 27.
Vận dụng:
Không vượt mức giới hạn cho phép.
BÀI TẬP
Câu 1
B.
Câu 2:
D.
Câu 3:
a) - K: 1s22s22p63s23p64s1 và ion tạo thành có cấu hình giống với Ar.
- Mg: 1s22s22p63s2 và ion tạo thành có cấu hình giống với Ne.
b) Không có hợp chất ion vì hai ion này cùng mang điện tích dương.
Câu 4:
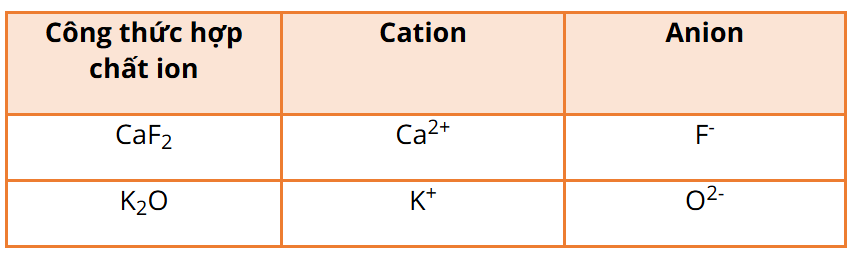
Câu 5:
- Na có xu hướng nhường 1 electron để tạo thành ion Na+
- O có xu hướng nhận 2 electron để tạo thành ion O2-
- Hai ion Na+ và 1 ion O2- liên kết với nhau tạo thành phân tử Na2O.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
giải 5 phút Hóa học 10 Chân trời sáng tạo, giải Hóa học 10 Chân trời sáng tạo trang 55, giải Hóa học 10 CTST trang 55

Bình luận