Lý thuyết trọng tâm Hóa học 12 Chân trời bài 6: Amine
Tổng hợp kiến thức trọng tâm Hóa học 12 chân trời sáng tạo bài 6: Amine. Tài liệu nhằm củng cố, ôn tập lại nội dung kiến thức bài học cho học sinh dễ nhớ, dễ ôn luyện. Kéo xuống để tham khảo
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 6. AMINE
A. MỤC TIÊU CẦN ĐẠT CỦA BÀI HỌC
- Nêu được khái niệm amine và phân loại amine (theo bậc của amine và bản chất gốc hydrocarbon).
- Viết được công thức cấu tạo và gọi được tên một số amine theo danh pháp thay thế, danh pháp gốc – chức (số nguyên tử carbon trong phân tử ≤ 5), tên thông thường của một số amine hay gặp.
- Nêu được đặc điểm về tính chất vật lí của amine (trạng thái, nhiệt độ sôi, nhiệt độ nóng chảy, khả năng hoà tan).
- Trình bày được đặc điểm cấu tạo phân tử và hình dạng phân tử methylamine và aniline.
- Trình bày được tính chất hoá học đặc trưng của amine: tính chất của nhóm –NH2 (tính base với quỳ tím, với HCl, với FeCl3), phản ứng với nitrous acid, phản ứng thế ở nhân thơm (với nước bromine) của aniline, phản ứng tạo phức của methylamine (hoặc ethylamine) với Cu(OH)2.
- Trình bày được ứng dụng của amine (diamine và aniline); các phương pháp điều chế amine (khử hợp chất nitro và thế nguyên tử hydrogen trong phân tử ammonia).
B. NHỮNG NỘI DUNG CẦN GHI NHỚ TRONG BÀI HỌC
1. Khái niệm và cấu trúc
Khái niệm và cách phân loại amine
- Khái niệm: Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen trong phân tử ammonia được thay thế bằng gốc hydrocarbon.
- Phân loại: Amine được phân loại theo bậc của amine và bản chất gốc hydrocarbon.
+ Theo bậc amine:
Cách xác định: Bậc của amine được xác định bằng số gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen.
Phân loại: Amine bậc một (CH3NH2,…), amine bậc hai (CH3NHCH3,…), amine bậc ba ((CH3)3N,…).
+ Theo bản chất gốc hydrocarbon:
Gốc hydrocarbon | Alkyl | Aryl |
Phân loại amine | Alkylamine | Arylamine |
Ví dụ | CH3NH2 | 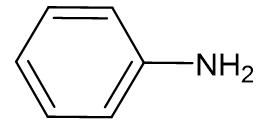 |
Đặc điểm cấu tạo, hình dạng phân tử methylamine và aniline
- Methylamine có cặp electron chưa liên kết trên nguyên tử nitrogen, hướng về đỉnh của một hình chóp tam giác, 2 nguyên tử hydrogen và nhóm -CH3 trên cùng mặt phẳng tam giác hướng về 3 đỉnh còn lại của hình chóp. Đối với nguyên tử carbon, 3 nguyên tử hydrogen và nhóm -NH2 hướng về 4 đỉnh của tứ diện. Vì vậy, methylamine có cấu trúc hình chóp tam giác đối với nguyên tử nitrogen và tứ diện đối với nguyên tử carbon. Cặp electron trên nguyên tử nitrogen của aniline liên hợp với hệ thống electron của vòng benzene, dẫn đến aniline có cấu trúc phẳng.
2. Đồng phân và danh pháp
- Đồng phân: Amine có đồng phân mạch carbon (phân nhánh không phân nhánh), vị trí nhóm chức và bậc amine (bậc I, bậc II, bậc III).
- Danh pháp:
+ Danh pháp gốc - chức:
Tên gốc alkyl + amine.
Sử dụng tiền tố di, tri,… để mô tả 2,3,… gốc alkyl giống nhau như diethyl, trimethyl; hoặc có 2,3,.. nhóm amine, như methylenediamine (NH2CH2NH2).
+ Danh pháp thay thế:
Amine bậc I:
Chọn mạch carbon dài nhất có chứa nguyên tử nitrogen làm mạch chính, số thứ tự bắt đầu từ nguyên tử carbon dầu mạch gần N nhất.
Đối với amine đơn chức: lược bỏ kí tự -e tận cùng của tên hydrocarbon + amine. Amine có từ 3 nguyên tử carbon thêm vị trí của nguyên tử nitrogen trước amine. Đối với amine đa chức, thêm di, tri,… + amine.
Amine bậc II và bậc III:
Cách gọi tên như amine bậc I và thêm tiền tố N- hoặc N,N- trước một hoặc hai nhóm thế liên kết với nguyên tử nitrogen. Sử dụng di, tri để mô tả 2, 3 nhóm thế giống nhau.
3. Tính chất vật lí
- Ở điều kiện thường, amine có thể tồn tại ở thể khí, lỏng hoặc rắn.
- Amine có nhiệt độ nóng chảy thấp.
- Nhiệt độ sôi của các amine cùng bậc tăng khi khối lượng phân tử tăng. Amine bậc I và bậc II có nhiệt độ sôi cao hơn amine bậc III có khối lượng phân tử tương đương.
- Amine có số nguyên tử carbon ![]() 4 tan nhều trong nước.
4 tan nhều trong nước.
4. Tính chất hóa học
Tính base của nhóm NH2
- Trong dung dịch, amine phản ứng với H2O tạo ion ammonium và ion hydroxide:
RNH2 + H2O ![]() RNH3+ + OH-
RNH3+ + OH-
⇒ Dung dịch alkylamine làm quỳ tím hóa xanh, dung dịch aniline không làm quỳ tím đổi màu.
- Amine tác dụng với acid tạo thành muối:
CH3NH2 + HCl → CH3NH3Cl
- Amine có khả năng tác dụng với dung dịch muối của một số kim loại tạo kết tủa hydroxide: 3CH3NH2 + FeCl3 + 3H2O → Fe(OH)3 + 3CH3NH3Cl
Phản ứng với nitrous acid
- Amine phản ứng với nitrous acid, sản phẩm phụ thuộc vào bậc amine, bản chất gốc hydrocarbon, điều kiện tiến hành,…
- Alkylamine bậc một tác dụng với nitrous acid (nhiệt độ thường) tạo alcohol và nitrogen ⇒ Nhận biết alkylamine bậc một.
- Aniline tác dụng với nitrous acid (0-5oC) tạo muối diazonium.
Phản ứng của aniline với nước bromine
- Do ảnh hưởng của -NH2, aniline dễ tham gia phản ứng thế nguyên tử H của vòng benzene hơn so với benzene, ưu tiên thế vào vị trí 2, 4, 6
Phản ứng tạo phức của methylamine
- Amine (methylamine, ethylamine) có khả năng tạo phức chất màu xanh lam với Cu2+:
CuSO4 + 2CH3NH2 + 2H2O → Cu(OH)2 + (CH3NH3)2SO4
4CH3NH2 + Cu(OH)2 → [Cu(CH3NH2)4](OH)2
5. Ứng dụng và điều chế
Giới thiệu ứng dụng của amine
- Amine: tổng hợp polyamide, dược phẩm, hóa chất sử dụng trong nông nghiệp và các vật liệu khác.
- Aniline: nguyên liệu sản xuất phẩm nhuộm, dược phẩm.
Điều chế
Khử hợp chất nitro
- Arylamine được điều chế bằng cách khử hợp chất có nhóm nitro bởi kim loại (Zn, Fe,…) trong môi trường acid.
Ví dụ: C6H5NO2 + 6[H] ![]() C C6H5NH2 + 2H2O
C C6H5NH2 + 2H2O
Alkyl hóa ammonia
- Alkylamine được điều chế từ ammonia và dẫn xuất halogen.
Ví dụ: NH3 ![]() CH3NH2
CH3NH2 ![]() (CH3)2NH
(CH3)2NH ![]() (CH3)3N
(CH3)3N
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
Tóm tắt kiến thức Hóa học 12 CTST bài 6: Amine, kiến thức trọng tâm Hóa học 12 chân trời sáng tạo bài 6: Amine, Ôn tập Hóa học 12 chân trời sáng tạo bài 6: Amine
Giải bài tập những môn khác
Môn học lớp 12 KNTT
5 phút giải toán 12 KNTT
5 phút soạn bài văn 12 KNTT
Văn mẫu 12 KNTT
5 phút giải vật lí 12 KNTT
5 phút giải hoá học 12 KNTT
5 phút giải sinh học 12 KNTT
5 phút giải KTPL 12 KNTT
5 phút giải lịch sử 12 KNTT
5 phút giải địa lí 12 KNTT
5 phút giải CN lâm nghiệp 12 KNTT
5 phút giải CN điện - điện tử 12 KNTT
5 phút giải THUD12 KNTT
5 phút giải KHMT12 KNTT
5 phút giải HĐTN 12 KNTT
5 phút giải ANQP 12 KNTT
Môn học lớp 12 CTST
5 phút giải toán 12 CTST
5 phút soạn bài văn 12 CTST
Văn mẫu 12 CTST
5 phút giải vật lí 12 CTST
5 phút giải hoá học 12 CTST
5 phút giải sinh học 12 CTST
5 phút giải KTPL 12 CTST
5 phút giải lịch sử 12 CTST
5 phút giải địa lí 12 CTST
5 phút giải THUD 12 CTST
5 phút giải KHMT 12 CTST
5 phút giải HĐTN 12 bản 1 CTST
5 phút giải HĐTN 12 bản 2 CTST
Môn học lớp 12 cánh diều
5 phút giải toán 12 CD
5 phút soạn bài văn 12 CD
Văn mẫu 12 CD
5 phút giải vật lí 12 CD
5 phút giải hoá học 12 CD
5 phút giải sinh học 12 CD
5 phút giải KTPL 12 CD
5 phút giải lịch sử 12 CD
5 phút giải địa lí 12 CD
5 phút giải CN lâm nghiệp 12 CD
5 phút giải CN điện - điện tử 12 CD
5 phút giải THUD 12 CD
5 phút giải KHMT 12 CD
5 phút giải HĐTN 12 CD
5 phút giải ANQP 12 CD
Giải chuyên đề học tập lớp 12 kết nối tri thức
Giải chuyên đề Ngữ văn 12 Kết nối tri thức
Giải chuyên đề Toán 12 Kết nối tri thức
Giải chuyên đề Vật lí 12 Kết nối tri thức
Giải chuyên đề Hóa học 12 Kết nối tri thức
Giải chuyên đề Sinh học 12 Kết nối tri thức
Giải chuyên đề Kinh tế pháp luật 12 Kết nối tri thức
Giải chuyên đề Lịch sử 12 Kết nối tri thức
Giải chuyên đề Địa lí 12 Kết nối tri thức
Giải chuyên đề Tin học ứng dụng 12 Kết nối tri thức
Giải chuyên đề Khoa học máy tính 12 Kết nối tri thức
Giải chuyên đề Công nghệ 12 Điện - điện tử Kết nối tri thức
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Kết nối tri thức
Giải chuyên đề học tập lớp 12 chân trời sáng tạo
Giải chuyên đề Ngữ văn 12 Chân trời sáng tạo
Giải chuyên đề Toán 12 Chân trời sáng tạo
Giải chuyên đề Vật lí 12 Chân trời sáng tạo
Giải chuyên đề Hóa học 12 Chân trời sáng tạo
Giải chuyên đề Sinh học 12 Chân trời sáng tạo
Giải chuyên đề Kinh tế pháp luật 12 Chân trời sáng tạo
Giải chuyên đề Lịch sử 12 Chân trời sáng tạo
Giải chuyên đề Địa lí 12 Chân trời sáng tạo
Giải chuyên đề Tin học ứng dụng 12 Chân trời sáng tạo
Giải chuyên đề Khoa học máy tính 12 Chân trời sáng tạo
Giải chuyên đề Công nghệ 12 Điện - điện tử Chân trời sáng tạo
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Chân trời sáng tạo
Giải chuyên đề học tập lớp 12 cánh diều
Giải chuyên đề Ngữ văn 12 Cánh diều
Giải chuyên đề Toán 12 Cánh diều
Giải chuyên đề Vật lí 12 Cánh diều
Giải chuyên đề Hóa học 12 Cánh diều
Giải chuyên đề Sinh học 12 Cánh diều
Giải chuyên đề Kinh tế pháp luật 12 Cánh diều
Giải chuyên đề Lịch sử 12 Cánh diều
Giải chuyên đề Địa lí 12 Cánh diều
Giải chuyên đề Tin học ứng dụng 12 Cánh diều
Giải chuyên đề Khoa học máy tính 12 Cánh diều
Giải chuyên đề Công nghệ 12 Điện - điện tử Cánh diều
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Cánh diều

Bình luận