Đề thi giữa kì 1 KHTN 7 CTST: Đề tham khảo số 4
Đề tham khảo số 4 giữa kì 1 KHTN 7 Chân trời sáng tạo gồm nhiều câu hỏi ôn tập hay, các dạng bài tập phong phú giúp các em củng cố ôn luyện lại kiến thức thật tốt chuẩn bị tốt cho kì thi sắp tới. Tài liệu có kèm theo đáp án và lời giải chi tiết. Hi vọng đây sẽ là tài liệu hữu ích giúp các em đạt điểm cao. Thầy cô và các em kéo xuống để tham khảo ôn luyện
ĐỀ THI GIỮA HỌC KÌ 1
MÔN: KHOA HỌC TỰ NHIÊN 7 – CHÂN TRỜI SÁNG TẠO
TRẮC NGHIỆM (4,0 điểm).
Chọn chỉ một phương án trả lời đúng trong các phương án A, B, C, D D rồi ghi vào giấy kiểm tra
Câu 1. Khối lượng phân tử sulfur dioxide (SO2) là?
A. 32 amu B. 48 amu C. 64 amu D. 80 amu
Câu 2. Dãy chất nào sau đây chỉ gồm công thức hóa học của các hợp chất?
A. Na2CO3, NaOH,Cu B. NH3, NaCl, H2O
C. NaCl, H2O, H2 D. HCl, NaCl, O2
Câu 3. Hai nguyên tử hydrogen liên kết với nhau tạo thành 1 phân tử hydrogen bởi?
A.Liên kết cộng hóa trị C. Liên kết hidro
B.Liên kết ion D. Liên kết ion và liên kết CHT.
Câu 4. Liên kết được hình thành bởi sự dùng chung electron giữa hai nguyên tử là liên kết nào?
A. Liên kết hydrogen. B. Liên kết kim loại.
C. Liên kết ion. D. Liên kết cộng hóa trị.
Câu 5. Fe có hóa trị III trong công thức nào?
A. FeO B. Fe2O3 C. FeSO4 D. FeCl2.
Câu 6. Chọn câu sai
A. Hóa tri là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố kia
B. Hoá trị của một nguyên tố được xác định theo hóa trị của H chọn làm đơn vị và hóa trị của oxi là 2 đơn vị
C. Quy tắc hóa trị : x.a=y.b
D. Photpho chỉ có hóa trị IV
Câu 7. Phát biểu nào sau đây không mô tả đúng mô hình nguyên tử của
Rơ-dơ-pho - Bo?
A. Nguyên tử có cấu tạo rỗng, gồm hạt nhân ở tâm nguyên tử và các electron ở vỏ nguyên tử
B. Nguyên tử có cấu tạo đặc khít, gồm hạt nhân nguyên tử và các electron.
C. Electron chuyển động xung quanh hạt nhân theo những quỹ đạo xác định tạo thành các lớp electron.
D. Hạt nhân nguyên tử mang điện tích dương, electron mang điện tích âm.
Câu 8. Kí hiệu hoá học của nguyên tố carbon là
A. Fe. B. Cu. C. C. D. Al.
Câu9. Sulfur là tên nguyên tố hóa học được kí hiệu là:
A. S B. Cl C. Si D. Ca
Câu 10. Cho mô hình cấu tạo nguyên tử aluminium:
Nguyên tử aluminium có bao nhiêu lớp electron và có bao nhiêu electron ở lớp ngoài cùng? A. Có 3 lớp electron và có 6 electron ở lớp ngoài ngoài cùng. B. Có 3 lớp electron và có 3 electron ở lớp ngoài ngoài cùng. C. Có 3 lớp electron và có 2 electron ở lớp ngoài ngoài cùng. D. Có 4 lớp electron và có 3 electron ở lớp ngoài ngoài cùng. | 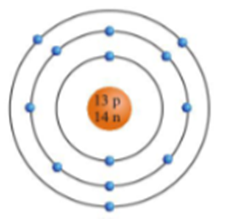 |
Câu 11. Bảng tuần hoàn các nguyên tố hoá học được cấu tạo từ
A. Ô nguyên tố, chu kì, nhóm.
B. Chu kì, nhóm.
C. Ô nguyên tố.
D. Chu kì.
Câu 12. Phát biểu nào sau đây là đúng?
A. Bảng tuần hoàn gồm 116 nguyên tố hoá học.
B. Bảng tuần hoàn gồm 6 chu kì.
C. Bảng tuần hoàn gồm 8 nhóm A và 8 nhóm B.
D. Các nguyên tố trong bảng tuần hoàn được xếp theo chiều tăng dần khối
lượng nguyên tử.
Câu 13. Kí hiệu hóa học của các nguyên tố sau: Sodium, Auminium, Nitrogen lần lượt là các KHHH nào ?
A. Na, Al, H. B. Na, Al, N. C. Al, Ba, N D. Ba, Al, H
Câu 14. Kí hiệu hóa học N là của nguyên tố hóa học nào?
A. Sodium. B. Nitrogen. C. Auminium. D. Oxygen.
Câu 15. Nhóm A là tập hợp các nguyên tố mà nguyên tử
A. Có số electron lớp ngoài cùng bằng nhau.
B. Có số lớp electron bằng nhau.
C. Có điện tích hạt nhân bằng nhau.
D. Có số hạt trong nguyên tử bằng nhau.
Câu 16. Phát biểu nào sau đây không đúng?
A. Bảng tuần hoàn gồm 3 chu kì nhỏ và 4 chu kì lớn.
B. Số thứ tự của chu kì bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố thuộc chu kì đó.
C. Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố
thuộc chu kì đó.
D. Các nguyên tố trong cùng chu kì được sắp xếp theo chiều điện tích hạt
nhân tăng dần.
II. TỰ LUẬN (6,0 điểm).
Câu 17 (1,5 điểm). Trình bày phương pháp tìm hiểu tự nhiên?
Câu 18 (1,5 điểm). a, Viết tên và kí hiệu của nguyên tố hóa học, hoàn thành bảng sau
STT | Tên nguyên tố hóa học | Kí hiệu hóa học | STT | Tên nguyên tố hóa học | Kí hiệu hóa học |
| 1 | H | 6 | chlorine | ||
| 2 | Ar | 7 | magnesium | ||
| 3 | F | 8 | potassium | ||
| 4 | Li | 9 | phosphorus | ||
| 5 | Si | 10 | oxygen |
b, Mô tả cấu tạo bảng tuần hoàn nguyên tố hóa học: ô, nhóm, chu kì
Câu 19 (1,0 điểm).
Quan sát ô nguyên tố và trả lời các câu hỏi sau: a) Em biết được thông tin gì trong ô nguyên tố calcium? b) Nguyên tố calcium này nằm ở vị trí nào (ô, nhóm, chu kì) trong bảng tuần hoàn các nguyên tố hóa học |  |
Câu 20 (1,0 điểm). Em tính khối lượng của chất theo đơn vị amu: Cl2, H2O, FeO, Al. Hợp chất NaCl thuộc loại liên kết hóa học nào?
Câu 21 (1,0 điểm). Copper (II) sulfate có trong thành phần của một số thuốc diệt nấm, trừ sâu và diệt cỏ cho cây trồng. Copper (II) sulfate được tạo thành từ Cu, S và O và có khối lượng phân tử là 160 amu. Phần trăm khối lượng của các nguyên tố Cu, S và O trong Copper (II) sulfate lần lượt là: 40%, 20% và 40%. Hãy xác định công thức hoá học của Copper (II) sulfate.
HẾT -
ĐÁP ÁN ĐỀ THI
I.TRẮC NGHIỆM (4,0 điểm)
Mỗi câu chọn đúng 0,25 điểm
Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
Chọn | C | B | A | D | B | D | B | C | A | C | A | C | B | B | A | B |
II. TỰ LUẬN(6,0 điểm )
Câu | Nội dung | Điểm | ||||||||||
17 | Phương pháp tìm hiểu tự nhiên gồm 5 bước - Đề xuất vấn đề cùng tìm hiểu - Đưa ra dự đoán khoa học để giải quyết vấn đề - Lập kế hoạch kiểm tra dự án - Thực hiện kế hoạch kiểm tra dự án - Viết báo cáo, thảo luận và trình bày báo cáo khi được yêu cầu. | 1,5 | ||||||||||
18 |
| 1,0 | ||||||||||
Cấu tạo bảng tuần hoàn hóa học - Ô nguyên tố: cho biết kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử. - Chu kì: cho biết số lớp electron, xếp theo chiều điện tích hạt nhân tăng dần đi từ trái sang phải. gồm 7 chu kì. - Nhóm: Gồm 8 nhóm A, 8 nhóm B, cho biết số electron lớp ngoài cùng | 0,5 | |||||||||||
19 | a.Từ ô nguyên tố của calcium, ta biết được + Số thứ tự của ô: 20. + Kí hiệu nguyên tố: Ca. + Tên nguyên tố: calcium. + Khối lượng nguyên tử: 40. | 0,5 | ||||||||||
| b) Vị trí của nguyên tố calcium + Ô: 20. + Nhóm: IIA. + Chu kì: 3. | 0,5 | ||||||||||
20 | Tính khối lượng của chất theo đơn vị amu: + H2O: 16+ 1.2= 18amu + FeO: 56+ 16= 72amu + Cl2: 35,5 . 2= 71amu + Al: 27amu | 0,5 | ||||||||||
NaCl thuộc loại liên kết ion. | 0,5 | |||||||||||
21 | Gọi công thức của Copper (II) sulfate là Cux SyOz. Vậy ta có: ( 64x:160 ) x 100% = 40% → x = 1 (32y : 160 ) x 100% = 20% → y = 1 (16z : 160 ) x 100% = 40% → z = 4 Vậy công thức của Copper (II) sulfate là: CuSO4 | 0,25 0,25 0,25 0,25 |
HẾT -
Thêm kiến thức môn học
Đề thi giữa kì 1 KHTN 7 Chân trời Đề tham khảo số 4, đề thi giữa kì 1 KHTN 7 CTST, đề thi KHTN 7 giữa kì 1 Chân trời sáng tạo Đề tham khảo số 4

Bình luận