Slide bài giảng Khoa học tự nhiên 9 Chân trời bài 22: Alkene
Slide điện tử bài 22: Alkene. Kiến thức bài học được hình ảnh hóa, sinh động hóa. Trình bày với các hiệu ứng hiện đại, hấp dẫn. Giúp học sinh hứng thú học bài. Học nhanh, nhớ lâu. Có tài liệu này, hiệu quả học tập của học môn Khoa học tự nhiên 9 Chân trời sáng tạo sẽ khác biệt
Bạn chưa đủ điều kiện để xem được slide bài này. => Xem slide bài mẫu
Tóm lược nội dung
BÀI 22. ALKENE
Mở đầu: Nhiều vật dụng như: bao tay, hộp nhựa, … được sản xuất từ hạt nhựa PE, PP. Các loại hạt nhựa này được tổng hợp từ các alkene tương ứng là ethylene, propylene.
Alkene là gì? Alkene đơn giản nhất (ethylene) có tính chất và ứng dụng gì?
Trả lời rút gọn:
Alkene là hydrocarbon mạch hở, chứa các liên kết đơn và có một liên kết đôi C=C trong phân tử.
Về tính chất vật lý, ethylene là chất khí, không màu, không mùi, rất ít tan trong nước, nhẹ hơn không khí. Về tính chất hóa học, ethylene có thể cháy trong không khí, khi cháy tạo sản phẩm chủ yếu gồm khí carbon dioxide và hơi nước, phản ứng tỏa nhiều nhiệt.
Ứng dụng của ethylene: được dùng để tổng hợp polyethylene trong công nghiệp. Polyethylene (PE) có nhiều ứng dụng trong đời sống như làm màng bọc thực phẩm, các loại bao đựng…
1. KHÁI NIỆM ALKENE
Câu 1: Hãy viết công thức phân tử và công thức cấu tạo thu gọn của các alkene ở Hình 22.1

Trả lời rút gọn:
Công thức phân tử: C2H4:
Công thức cấu tạo thu gọn: CH2=CH2
Công thức phân tử: C3H6
Công thức cấu tạo thu gọn: CH2=CH-CH3
Câu 2: Bằng cách nào để biết được ethylene nhẹ hơn không khí?
Trả lời rút gọn:
Khối lượng mol của ethylen C2H4 bằng 28, trong khi đó khối lượng mol của không khí bằng 29.
Tỉ khối dC2H4/không khí = 28/29 <1, vậy nên ethylen nhẹ hơn không khí.
2. TÍNH CHẤT HÓA HỌC CỦA ETHYLENE
Câu 3: Nêu hiện tượng và viết phương trình hóa học của phản ứng xảy ra ở Thí nghiệm 1
Trả lời rút gọn:
Hiện tượng: Khí ethylen cháy trong không khí, ngọn lửa tỏa nhiều nhiệt.
C2H4 + 3O2 —> 2CO2 + 2H2O (có nhiệt độ)
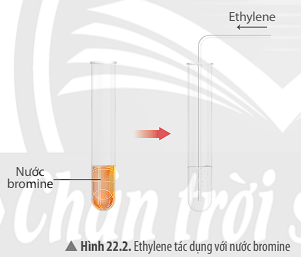
Câu 4: Nêu hiện tượng của Thí nghiệm 2 ở Hình 22.2. Dùng công thức cấu tạo thu gọn, viết phương trình hóa học của phản ứng xảy ra
Trả lời rút gọn:
Nước bromine trong ống nghiệm ban đầu có màu vàng nâu; sau khi sục khí ethylen vào ống nghiệm, màu vàng nâu của nước bromine nhạt dần rồi mất màu, sản phẩm thu được không màu.
CH2=CH2 + Br-Br —> Br-CH2-CH2-Br
Luyện tập: Cho các hợp chất hữu cơ sau: CH3-CH3, CH2=CH-CH3, CH2=CHCl, CH3-CH2-CH3. Trong các chất trên, chất nào có phản ứng trùng hợp tạo polymer và chất nào có khả năng làm mất màu nước bromine? Giải thích
Trả lời rút gọn:
Các chất có phản ứng trùng hợp tạo polymer và có khả năng làm mất màu nước bromine: CH2=CH-CH3, CH2=CHCl. Bởi vì trong phân tử hai chất này chứa liên kết đôi C=C kém bền, dễ bị đứt ra để tham gia phản ứng (phản ứng cộng với Br2 hoặc phản ứng cộng nhiều phân tử với nhau thành những phân tử mạch rất dài và có khối lượng phân tử rất lớn - phản ứng trùng hợp)
Vận dụng: PE được tạo ra từ ethylene, có nhiều ứng dụng trong đời sống như làm màng bọc thực phẩm, các loại bao đựng,…
Hãy cho biết thêm một số ứng dụng của polyethylene
Trả lời rút gọn:
Nhựa PE có thể được sử dụng trong in tem nhãn, dùng trong sản xuất các sản phẩm đóng gói, sản xuất ống và phụ kiện; vì cách điện tốt nên PE còn có thể sử dụng để cách điện có cáp đồng trục và vỏ cáp; ngoài ra còn có thể ứng dụng trong y tế (sử dụng làm khớp nhân tạo thay khớp gối và khớp háng)...
3. MỘT SỐ ỨNG DỤNG CỦA ETHYLENE
Vận dụng: Tìm hiểu và trình bày một số ứng dụng của ethylene trong đời sống
Trả lời rút gọn:
Một số ứng dụng của ethylene trong đời sống Ethylene là nguyên liệu quan trọng của công nghiệp tổng hợp polymer và các hóa chất hữu cơ khác.; chuyển hóa ethylene thành các monomer khác để tổng hợp ra hàng loạt polymer đáp ứng nhu cầu phong phú của đời sống và kỹ thuật (như nhựa PVC).
