Slide bài giảng Khoa học tự nhiên 9 Chân trời bài 21: Alkane
Slide điện tử bài 21: Alkane. Kiến thức bài học được hình ảnh hóa, sinh động hóa. Trình bày với các hiệu ứng hiện đại, hấp dẫn. Giúp học sinh hứng thú học bài. Học nhanh, nhớ lâu. Có tài liệu này, hiệu quả học tập của học môn Khoa học tự nhiên 9 Chân trời sáng tạo sẽ khác biệt
Bạn chưa đủ điều kiện để xem được slide bài này. => Xem slide bài mẫu
Tóm lược nội dung
BÀI 21. ALKANE
Mở đầu: Khí tự nhiên, khí mỏ dầu đều có thành phần chính là alkane và một số hydrocarbon khác. Alkane là gì? Alkane có những tính chất vật lý, hóa học nào?
Trả lời rút gọn:
Alkane là hydrocarbon mạch hở, chỉ chứa liên kết đơn (C-C, C-H) trong phân tử.
Tính chất vật lý của alkane: ở điều kiện thường, các alkane từ C1 đến C4 ở trạng thái khí, từ C5 đến khoảng C18 ở trạng thái lỏng, từ khoảng C18 trở đi ở trạng thái rắn.
Alkane không tan trong nước. Alkane là những dung môi phân cực và đều là những chất không màu.
Tính chất hóa học: trong phân tử Alkane chỉ có các liên kết C-C và C-H bền, nên alkane tương đối trơ về mặt hóa học. Dưới tác dụng của ánh sáng, xúc tác và nhiệt độ, alkane tham gia các phản ứng thế, phản ứng tách và phản ứng oxy hóa.
1. KHÁI NIỆM HYDROCARBON, ALKANE
Câu 1: Vì sao methane, ethylene được gọi là hydrocarbon?
Trả lời rút gọn:
Methane, ethylene được gọi là hydrocarbon. Vì trong thành phần nguyên tố của 02 hợp chất này chỉ gồm nguyên tố carbon và hydrogen
Câu 2: Hãy viết công thức phân tử, công thức cấu tạo thu gọn và cho biết đặc điểm cấu tạo các alkane ở Hình 21.1.
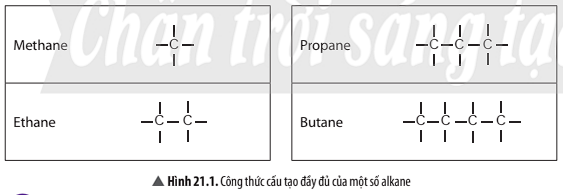
Trả lời rút gọn:
Công thức phân tử:
Methane: CH4; propane: C3H8; ethane: C2H6; butane: C4H10
Công thức cấu tạo thu gọn:
Methane: CH4; propane: CH3-CH2-CH3; ethane: CH3-CH3;
butane: CH3-CH2-CH2-CH3
Đặc điểm cấu tạo của các alkane: có mạch hở, chỉ chứa các liên kết đơn (C-C, C-H) trong phân tử.
2. THÍ NGHIỆM ĐỐT CHÁY BUTANE
Câu 3: Gas dùng đun nấu có chứa alkane chủ yếu nào? Viết phương trình hóa học biểu diễn phản ứng cháy của chúng
Trả lời rút gọn:
Gas dùng để đun nấu có chứa các alkane chủ yếu gồm propane C3H8 và butane C4H10.
Phương trình hóa học biểu diễn phản ứng cháy:
C3H8 + 5O2 —> 3CO2 + 4H2O (có nhiệt độ)
2C4H10 + 13O2 —> 8CO2 + 10H2O (có nhiệt độ)
Vận dụng: Vì sao ở các trạm xăng dầu người ta thường treo bảng cấm như ở hình bên dưới?

Trả lời rút gọn:
Các trạm xăng dầu người ta thường treo bảng cấm. Vì trong xăng dầu có nhiều alkane. Các alkane đầu dãy đồng đẳng có trong xăng dầu rất dễ cháy (dưới những tác nhân như ngọn lửa, điếu thuốc cháy dở, sóng điện thoại, tia lửa xuất hiện trong động cơ xe…), khi cháy alkane tỏa nhiều nhiệt. Khí CO2, hơi nước và nhiệt tạo ra nhanh nên có thể gây nổ, rất nguy hiểm.
3. ỨNG DỤNG LÀM NHIÊN LIỆU CỦA ALKANE TRONG THỰC TIỄN
Câu 4: Vì sao một số alkane (methane, propane, butane,…) được sử dụng làm nhiên liệu?
Trả lời rút gọn:
Một số alkane (methane, propane, butane,…) được sử dụng làm nhiên liệu do các alkane này đều cháy trong không khí tạo sản phẩm chủ yếu gồm carbon dioxide và nước, khi cháy tỏa nhiều nhiệt.
Luyện tập: Methane, propane thường được dùng làm nhiên liệu. Khi đốt cùng một khối lượng mỗi chất trên thì nhiệt lượng tỏa ra của chất nào lớn hơn? Biết rằng nhiệt tỏa ra khi cháy của methane và propane lần lượt là 890 kJ/mol và 2219 kJ/mol.
Trả lời rút gọn:
Giả sử có cùng khối lượng methane và propane là m (gam).
Khi đó, số mol methane: nCH4=![]() ; số mol propane: nC3H8=
; số mol propane: nC3H8=![]()
Nhiệt tỏa ra khi đốt cháy m (gam) methane: Q1=![]() .890 = 55,625m (kJ)
.890 = 55,625m (kJ)
Nhiệt tỏa ra khi đốt cháy m (gam) propane: Q2=![]() .2219 ≈ 50,432m (kJ)
.2219 ≈ 50,432m (kJ)
Vận dụng: Em hãy giới thiệu một số alkane được sử dụng phổ biến trong đời sống
Bài làm chi tiết:
Các alkane thường được sử dụng làm nhiên liệu (như CH4, C3H8 dùng làm khí đốt, khí hóa lỏng…), các alkane chứa từ 20 carbon trở lên thường được dùng làm dầu mỡ bôi trơn, chống gỉ, sáp pha thuốc mỡ, nến, giấy dầu…
