Câu hỏi tự luận mức độ vận dụng cao Hóa học 12 ctst bài 19: Đại cương về kim loại
4. VẬN DỤNG CAO (1 CÂU)
Câu 1: Cho 100 gam hợp kim của Fe, Cr, Al tác dụng với dung dịch NaOH dư thoát ra 5,04 lít khí (đktc) và một phần rắn không tan. Lọc lấy phần không tan đem hòa tan hết bằng dung dịch HCl nóng, dư thấy thoát ra 38,8 lít khí (đktc). Phần trăm khối lượng các chất trong hợp kim là bao nhiêu?
Câu 2: Hòa tan hoàn toàn 30,4 gam chất rắn X gồm Cu, CuS, Cu2S và S bằng HNO3 dư thoát ra 20,16 lít khí NO duy nhất (đktc) và dung dịch Y. Thêm Ba(OH)2 dư vào Y thu được m gam kết tủa. Tính m.
Câu 3: Ngâm sắt dư trong 200ml dung dịch CuSO4 1M. Sau khi phản ứng kết thúc, lọc kết tủa chất rắn A và dung dịch B.
a. Cho A tác dụng với dung dịch HCl dư. Tính khối lượng chất rắn thu được sau phản ứng.
b. Tính thể tích dung dịch NaOH 1M vừa đủ để kết tủa hoàn toàn dung dịch B. Lọc tách kết tủa đem nung ngoài không khí đến khối lượng không đổi thu được bao nhiêu g chất rắn.
Câu 1:
Gọi số mol Fe, Cr và Al lần lượt là x, y và z mol
→ 56x + 52y + 27z = 100 (1)
Cho hợp kim tác dụng với NaOH chỉ có Al phản ứng:
2Al (0,15) + 2NaOH + 2H2O → 2NaAlO2 + 3H2 (0,225 mol)
→ z = 0,15
Sau phản ứng còn Fe, Cr cho vào HCl nóng, dư có phản ứng
Cr (y) + 2HCl → CrCl2 + H2 (y mol)
Fe (x) + 2HCl → FeCl2 + H2 (x mol)
→ x + y = 1,7321
Giải hệ pt được x = 1,4702; y = 0,2691; z = 0,15.
%mFe = 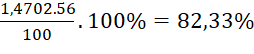 .
.
%mAl = 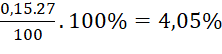 .
.
%mCr = 100 – 82,33 – 4,05 = 13,62%.
Câu 2:
Quy đổi hỗn hợp X thành Cu: x mol và S: y mol
Ta có: mX = 64x+ 32y = 30,4 gam (1)
Cu → Cu2++ 2e
x 2x mol
S → SO42-+ 6e
y y 6y
nNO= 0,9 mol
N+5+ 3e → NO
2,7← 0,9 mol
Theo ĐLBT e : ne cho= ne nhận nên 2x+6y= 2,7 (2)
Từ (1) và (2) suy ra x= 0,3 và y= 0,35
Dung dịch Y có Cu2+, SO42-, H+, NO-3
Khi cho Ba(OH)2 dư vào dung dịch Y thì:
Ba2++ SO42- → BaSO4
y y mol
Cu2++ 2OH- → Cu(OH)2
x x mol
mkết tủa= mCu(OH)2+ mBaSO4 = 98x + 233y = 98.0,3 + 233.0,35 = 110,95 gam.
Câu 3:
a) Fe + CuSO4 → FeSO4+ Cu
Cu + HCl → k phản ứng
Khối lượng chất rắn cần tính sau phản ứng là Cu
nCuSO4 = 0,2 .1 = 0,2 (mol)
Theo phương trình hóa học: nCu = nCuSO4 = 0,2 mol
=> mCu = 0,2.64 = 12,8(g)
b) Phương trình hóa học:
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
nFeSO4 = nCuSO4= 0,2 mol
Theo phương trình: nNaOH = 2nFeSO4 = 0,2.2 = 0,4 (mol)
=> VddNaOH = 0,4:1 = 0,4 lít
Giải những bài tập khác
Giải bài tập những môn khác
Môn học lớp 12 KNTT
5 phút giải toán 12 KNTT
5 phút soạn bài văn 12 KNTT
Văn mẫu 12 KNTT
5 phút giải vật lí 12 KNTT
5 phút giải hoá học 12 KNTT
5 phút giải sinh học 12 KNTT
5 phút giải KTPL 12 KNTT
5 phút giải lịch sử 12 KNTT
5 phút giải địa lí 12 KNTT
5 phút giải CN lâm nghiệp 12 KNTT
5 phút giải CN điện - điện tử 12 KNTT
5 phút giải THUD12 KNTT
5 phút giải KHMT12 KNTT
5 phút giải HĐTN 12 KNTT
5 phút giải ANQP 12 KNTT
Môn học lớp 12 CTST
5 phút giải toán 12 CTST
5 phút soạn bài văn 12 CTST
Văn mẫu 12 CTST
5 phút giải vật lí 12 CTST
5 phút giải hoá học 12 CTST
5 phút giải sinh học 12 CTST
5 phút giải KTPL 12 CTST
5 phút giải lịch sử 12 CTST
5 phút giải địa lí 12 CTST
5 phút giải THUD 12 CTST
5 phút giải KHMT 12 CTST
5 phút giải HĐTN 12 bản 1 CTST
5 phút giải HĐTN 12 bản 2 CTST
Môn học lớp 12 cánh diều
5 phút giải toán 12 CD
5 phút soạn bài văn 12 CD
Văn mẫu 12 CD
5 phút giải vật lí 12 CD
5 phút giải hoá học 12 CD
5 phút giải sinh học 12 CD
5 phút giải KTPL 12 CD
5 phút giải lịch sử 12 CD
5 phút giải địa lí 12 CD
5 phút giải CN lâm nghiệp 12 CD
5 phút giải CN điện - điện tử 12 CD
5 phút giải THUD 12 CD
5 phút giải KHMT 12 CD
5 phút giải HĐTN 12 CD
5 phút giải ANQP 12 CD
Giải chuyên đề học tập lớp 12 kết nối tri thức
Giải chuyên đề Ngữ văn 12 Kết nối tri thức
Giải chuyên đề Toán 12 Kết nối tri thức
Giải chuyên đề Vật lí 12 Kết nối tri thức
Giải chuyên đề Hóa học 12 Kết nối tri thức
Giải chuyên đề Sinh học 12 Kết nối tri thức
Giải chuyên đề Kinh tế pháp luật 12 Kết nối tri thức
Giải chuyên đề Lịch sử 12 Kết nối tri thức
Giải chuyên đề Địa lí 12 Kết nối tri thức
Giải chuyên đề Tin học ứng dụng 12 Kết nối tri thức
Giải chuyên đề Khoa học máy tính 12 Kết nối tri thức
Giải chuyên đề Công nghệ 12 Điện - điện tử Kết nối tri thức
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Kết nối tri thức
Giải chuyên đề học tập lớp 12 chân trời sáng tạo
Giải chuyên đề Ngữ văn 12 Chân trời sáng tạo
Giải chuyên đề Toán 12 Chân trời sáng tạo
Giải chuyên đề Vật lí 12 Chân trời sáng tạo
Giải chuyên đề Hóa học 12 Chân trời sáng tạo
Giải chuyên đề Sinh học 12 Chân trời sáng tạo
Giải chuyên đề Kinh tế pháp luật 12 Chân trời sáng tạo
Giải chuyên đề Lịch sử 12 Chân trời sáng tạo
Giải chuyên đề Địa lí 12 Chân trời sáng tạo
Giải chuyên đề Tin học ứng dụng 12 Chân trời sáng tạo
Giải chuyên đề Khoa học máy tính 12 Chân trời sáng tạo
Giải chuyên đề Công nghệ 12 Điện - điện tử Chân trời sáng tạo
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Chân trời sáng tạo
Giải chuyên đề học tập lớp 12 cánh diều
Giải chuyên đề Ngữ văn 12 Cánh diều
Giải chuyên đề Toán 12 Cánh diều
Giải chuyên đề Vật lí 12 Cánh diều
Giải chuyên đề Hóa học 12 Cánh diều
Giải chuyên đề Sinh học 12 Cánh diều
Giải chuyên đề Kinh tế pháp luật 12 Cánh diều
Giải chuyên đề Lịch sử 12 Cánh diều
Giải chuyên đề Địa lí 12 Cánh diều
Giải chuyên đề Tin học ứng dụng 12 Cánh diều
Giải chuyên đề Khoa học máy tính 12 Cánh diều
Giải chuyên đề Công nghệ 12 Điện - điện tử Cánh diều
Giải chuyên đề Công nghệ 12 Lâm nghiệp thủy sản Cánh diều

Bình luận