Lý thuyết trọng tâm hóa học 11 kết nối bài 23: Hợp chất carbonyl
Tổng hợp kiến thức trọng tâm hóa học 11 kết nối bài 23: Hợp chất carbonyl. Tài liệu nhằm củng cố, ôn tập lại nội dung kiến thức bài học cho học sinh dễ nhớ, dễ ôn luyện. Kéo xuống để tham khảo
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
I. KHÁI NIỆM, DANH PHÁP
1. Khái niệm
Hợp chất carbony: hợp chất trong phân tử có nhóm >C=O
Aldehyde: hợp chất hữu cơ có nhóm -CHO liên kết trực tiếp với nguyên tử carbon (trong gốc hydrocarbon hoặc -CHO) hoặc nguyên tử hydrogen.
Ketone: hợp chất hữu cơ có nhóm >C=O liên kết với hai nhóm hydrocarbon .
2. Danh pháp
a) Tên thay thế
- Aldehyde đơn chức: Tên hydrocarbon tương ứng (bỏ “e” ở cuối) + al
- Ketone đơn chức Tên hydrocarbon tương ứng (bỏ “e” ở cuối) + số chỉ vị trí nhóm C=O + one.
VD:
- HCHO: methanal
- CH3CHO: ethanal
- CH3CH(CH3)CH2CHO 3-methylbutanal.
- CH3COCH3 : propanone.
- CH3COCH2CH3: butan-2-one.
- CH3CH2COCH2CH3: pentan-3-one
b) Tên thông thường
Một số aldehyde và ketone đơn giản được gọi theo tên thông thường có nguồn gốc lịch sử
Tên gọi thông thường của aldehyde có nguồn gốc từ tên acid tương ứng
- HCHO: aldehyde formic.
- CH3CHO: aldehyde acetic.
- C6H5CHO: aldehyde benzoic
- CH3COCH3: acetone
II. ĐẶC ĐIỂM CẤU TẠO
Trong nhóm carbonyl liên kết >C=O phân cực về phía nguyên tử oxygen.
III. TÍNH CHẤT VẬT LÍ
- Ở điều kiện thường HCHO, CH$_{3}$CHO là chất khí, các hợp chất carbonyl thông dụng khác tồn tại ở trạng thái lỏng hoặc rắn.
- Nhiệt độ sôi cao hơn hydrocarbon nhưng thấp hơn alcohol có phân tử khối tương đương.
- Tính tan: mạch ngắn dễ tan, mạch dài ít tan hoặc không tan trong nước.
- Các aldehyde và ketone thơm hầu như không tan trong nước.
- Có mùi đặc trưng.
IV. TÍNH CHẤT HOÁ HỌC
1. Phản ứng khử
Các hợp chất carbonyl bị khử bởi các chất khử: LiAlH$_{4}$, NaBH$_{4}$...thành alcohol.
VD:
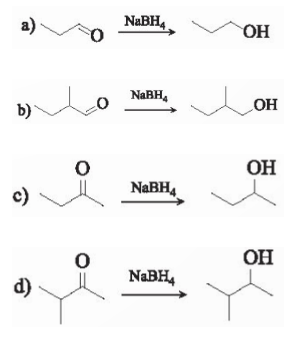
Kết luận:
R-CHO $\overset{LiAlH_{4}}{\rightarrow}$ R-CH$_{2}$-OH
Aldehyde (Alcohol bậc I)
RCOR' $\overset{LiAlH_{4}}{\rightarrow}$ R-CH(OH)-R'
Ketone (Alcohol bậc II)
2. Phản ứng oxi hóa aldehyde
Aldehyde dễ bị oxi hóa bởi các tác nhân oxi hóa thông thường như: Br$_{2}$/H$_{2}$O, [Ag(NH$_{3}$)$_{2}$]OH, Cu(OH)$_{2}$/OH,…
a) Oxi hóa aldehyde bởi nước bromine
Aldehyde bị oxi hóa bởi nước bromine tạo thành carboxylic acid.
Ví dụ: CH3CHO + Br2 + H2O → CH3COOH + 2HBr
b) Oxi hóa aldehyde bởi thuốc thử Tollens, copper (II) hydroxide
Thí nghiệm Aldehyde với thuốc thử Tollens AgNO$_{3}$/NH$_{3}$:
Hiện tượng: Xuất hiện kết tủa đen Ag2O sau đó chất này bị hòa tan bởi ammonia tạo phức
2AgNO3 + 2NaOH → Ag2O + 2NaNO3 + H2O
Ag2O + 4NH3 + H2O → 2[Ag(NH3)2]+OH-
Nhỏ vài giọt dung dịch CH3CHO 5% vào ống nghiệm, lắc đều. Đặt ống nghiệm vào cốc chứa nước nóng (khoảng 70 – 80 °C), để yên khoảng 5 phút tạo kết tủa màu trắng xám của kim loại bạc, bám vào thành ống nghiệm, có thể soi gương được.
CH3CHO + 2[Ag(NH3)2]OH → CH3COONH4 + 2Ag + 3NH3 + H2O
Thí nghiệm phản ứng oxi hoá aldehyde bằng copper(II) hydroxide
Hiện tượng: Khi cho dung dịch CuSO4 vào dung dịch NaOH, hỗn hợp tạo kết tủa màu xanh lam, kết tủa đó là Cu(OH)2 (copper(II) hydroxide).
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
Khi thêm dung dịch CH3CHO 5% vào ống nghiệm, lắc đều, đun nóng, kết quả chuyển từ màu xanh lam sang màu đỏ gạch do hình thành kết tủa Cu2O
CH3CHO + 2Cu(OH)2 → CH3COONa + Cu2O + 3H2O
Kết luận: Aldehyde bị oxi hóa bởi nước bromine => carboxylic acid.
Oxi hóa aldehyde bằng thuốc thử Tollens
RCHO + 2[Ag(NH3)2]OH → RCOONH4 + 2NH3 + 2Ag + H2O
Phản ứng với Cu(OH)2/OH-
RCHO + 2Cu(OH)2 $\overset{t^{o}}{\rightarrow }$ RCOONa + Cu2O + 3H2O
VD: Phản ứng của HCHO với các tác nhân sau:
a) Thuốc thử Tollens:
HCHO + 2[Ag(NH3)2]OH → (NH4)2CO3 + 4Ag + 2H2O + 6NH3
b) Cu(OH)2/NaOH.
HCHO + 4Cu(OH)2 + 2NaOH → 2Cu2O + Na2CO3 + 6H2O
3. Phản ứng cộng
Hợp chất carbonyl có thể tham gia phản ứng cộng với HCN vào liên kết đôi C=O
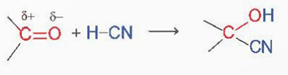
4. Phản ứng tạo iodoform
Hiện tượng: xuất hiện kết tủa màu vàng.
PTHH:
CH3COCH3 + 3I2 + 4NaOH ⟶ CH3COONa + CHI3 + 3NaI+ 3H2O
Kết luận: Các aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl (CH3CO-) tham gia được phản ứng tạo iodoform
V. ỨNG DỤNG
Aldehyde, ketone có nhiều ứng dụng trong sản xuất và đời sống hằng ngày:
- Keo phenolformadehyde dùng trong công nghiệp gỗ dán.
- Formol dùng bảo quản các mẫu sinh vật.
- Các sản phẩm sử dụng Melamine như bát đũa, tô, chén, khay, ly, đĩa nhựa,...
VI. ĐIỀU CHẾ
1. Acetaldehyde từ ethylene
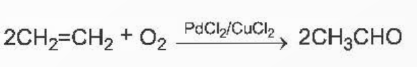
2. Acetone từ cumene
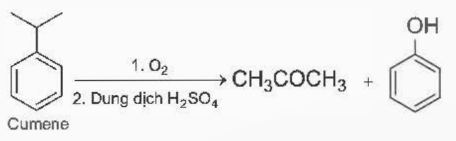
Phương pháp cumene được sử dụng phổ biến nhất vì có thể đồng thời tạo ra 2 hợp chất hữu cơ có tính ứng dụng cao là Acetone và Phenol.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
Giải bài tập những môn khác
Giải sgk lớp 11 KNTT
Giải sgk lớp 11 CTST
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều

Bình luận