Slide bài giảng Khoa học tự nhiên 9 Cánh diều bài 24: Acetic acid
Slide điện tử bài 24: Acetic acid. Kiến thức bài học được hình ảnh hóa, sinh động hóa. Trình bày với các hiệu ứng hiện đại, hấp dẫn. Giúp học sinh hứng thú học bài. Học nhanh, nhớ lâu. Có tài liệu này, hiệu quả học tập của học môn Khoa học tự nhiên 9 Cánh diều sẽ khác biệt
Bạn chưa đủ điều kiện để xem được slide bài này. => Xem slide bài mẫu
Tóm lược nội dung
BÀI 24: ACETIC ACID
Mở đầu: Quan sát hình 24.1, mô tả và giải thích hiện tượng xảy ra. Có hiện tượng trên là do trong giấm ăn có acetic acid. Vậy acetic acid có cấu tạo như thế nào và có những tính chất gì?
Trả lời rút gọn:
Công thức cấu tạo thu gọn của acetic acid là CH3-COOH
Acetic acid có các tính chất chung của acid, có phản ứng tạo ra ester và phản ứng cháy.
I. CẤU TẠO PHÂN TỬ VÀ TÍNH CHẤT VẬT LÝ
Câu 1: Chỉ ra những chất có đặc điểm cấu tạo tương tự cấu tạo của acetic acid trong các chất sau:
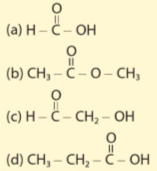
Trả lời rút gọn:
Những chất có đặc điểm cấu tạo tương tự cấu tạo của acetic acid là ý a) và ý d)
Câu 2: Dùng ống hút nhỏ giọt lấy khoảng 2mL acetic acid cho vào ống nghiệm. Quan sát và nêu trạng thái, màu sắc của acetic acid.
Trả lời rút gọn:
- Trạng thái: chất lỏng
- Màu sắc: trong suốt và có thể nhìn thấy qua được.
II. TÍNH CHẤT HÓA HỌC
Câu 1: Trong thí nghiệm 1, sự thay đổi màu của giấy quỳ tím chứng tỏ điều gì?
Trả lời rút gọn:
Quỳ tím chuyển sang màu đỏ chứng tỏ tính axit.
Câu 2: Trong thí nghiệm 1, những dấu hiệu nào chứng tỏ acetic acid đã phản ứng với NaOH? Chất khí nào thoát ra khi cho dung dịch acetic acid vào đá vôi?
Trả lời rút gọn:
Khi NaOH tác dụng với acetic acid, dung dịch sẽ chueyern từ axit sang trạng thái trung tính hoặc bazo. Khi dung dịch trở nên bazo, phenolphthalein sẽ chuyển từ màu không màu hoặc màu nhạt sang màu hồng.
Khi cho dung dịch acetic acid vào đá vôi thì chất khí CO2 sẽ thoát ra.
Câu 3: Viết phường trình hóa học của phản ứng xảy ra khi cho acetic acid tác dụng với Cu(OH)2, MgO,Fe.
Trả lời rút gọn:
- 2CH3COOH + Cu(OH)2 => Cu(CH3COO)2 + 2H2O
- 2CH3COOH + MgO => Mg(CH3COO)2 + H2O
- 2CH3COOH + 2Fe => 2CH3COOFe + H2O + CO2
Câu 4: chọn các chất thích hợp để điền vào dấu ? và hoàn thành các phương trình hóa học sau
a) ? + Na2CO3 = > CH3COONa + ? + ?
b) CH3COOH + ? => (CH3COO)2Mg +H2
Trả lời rút gọn:
a) CH3COOH + Na2CO3 => CH3COONa + H2O + CO2
b) CH3COOH + Mg(OH)2 => (CH3COO)2Mg + H2
Vận dụng: Cặn trong ấm đun nước có thành phần chính là CaCO3(hình 24.3). Có thể làm sạch cặn bằng giấm ăn. Giải thích cách làm trên, phương trình hóa học minh họa.
Trả lời rút gọn:
Giấm ăn, một dung dịch CH3COOH, có khả năng phản ứng với cacbonat canxi để tạo ra muối (Ca(CH3COO)2), nước , và CO2 dưới dạng khí.
CaCO3 + 2CH3COOH => Ca(CH3COO)2 +H2O + CO2
Vận dụng: Trên chai đựng acetic acid đặc có các ký hiệu:

Nêu ý nghĩa của các ký hiệu trên. Cần phải làm gì khi sử dụng và lưu trữ acetic acid đặc ?
Trả lời rút gọn:
Cảnh báo ăn mòn và cảnh báo oxy hóa
Khi sử dụng và lưu trữ acetic acid đặc, cần tuân thủ các biện pháp an toàn sau:
- Sử dụng trong môi trường thông thoáng và đeo đồ bảo hộ để bảo vệ mắt và da
- Tránh hít phải hơi axit và tiếp xúc trực tiếp với da và mắt
- Lưu trữ axit axetic trong bình kín đậy chặt, ở nhiệt độ phòng và tránh xa nguồn nhiệt độ cao
- Phân biệt vị trí lưu trữ và tránh tiếp xúc với các chất có tính oxy hóa mạnh
III. ĐIỀU CHẾ ACETIC ACID
Vận dụng: Khi lên men dung dịch ethylic alcolhol để sản xuất acetic acid trong ông nghiệp, người ta liên tục sục không khi vào dung dịch. Giải thích ý nghĩa của việc làm trên.
Trả lời rút gọn:
Cung cấp oxy cho vi khuẩn acetobacter: vi khuẩn này cần oxy để chuyển đổi ethylix alcolhol thành acetic acid. Giúp oxy trong không khí tiếp xúc với dung dịch một cách hiệu quả. Ngoài ra, hỗ trợ loại bỏ CO2, sản phẩm phụ sinh ra trong quá trình lên men.
IV. ỨNG DỤNG CỦA ACETIC ACID
Câu 1: Dựa vào hình 24.6 nêu một số ứng dụng của acetic acid
Trả lời rút gọn:
- Sản xuất giấm ăn
- Sản xuất dược phẩm
- Sản xuất keo dán
- Sản xuất sơn
- Sản xuất chất dẻo
