Lý thuyết trọng tâm Khoa học tự nhiên 9 Chân trời bài 22: Akene
Tổng hợp kiến thức trọng tâm Khoa học tự nhiên 9 Chân trời sáng tạo bài 22: Akene. Tài liệu nhằm củng cố, ôn tập lại nội dung kiến thức bài học cho học sinh dễ nhớ, dễ ôn luyện. Kéo xuống để tham khảo
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 22. ALKENE
A - MỤC TIÊU BÀI HỌC
- Nêu được khái niệm về alkene.
- Viết được công thức cấu tạo và nêu được tính chất vật lí của ethylene.
- Trình bày được tính chất hóa học của ethylene (phản ứng cháy, phản ứng làm mất màu nước bromine, phản ứng trùng hợp). Viết được các phương trình hóa học xảy ra.
- Tiến hành được thí nghiệm (hoặc quan sát thí nghiệm) của ethylene: phản ứng đốt cháy, phản ứng mất màu nước bromine, quan sát và giải thích được tính chất hóa học cơ bản của alkene.
- Trình bày được một số ứng dụng của ethylene: tổng hợp ethylic alcohol, tổng hợp nhựa polyethylene (PE).
B - NHỮNG KIẾN THỨC CẦN GHI NHỚ
1. Khái niệm alkene
- Khái niệm: Alkene là hydrocarbon mạch hở chứa các liên kết đơn và có một liên kết đôi (C=C) trong phân tử.
- Ethylene là chất khí không màu, không mùi, ít tan trong nước nhẹ hơn không khí.
- Công thức chung alkene:
CnH2n với (![]() )
)
- Đặc điểm cấu tạo alkene:
+ Có liên kết C = C gồm 1 liên kết ![]() và 1 liên kết π.
và 1 liên kết π.
![]() Liên kết π kém bền nên alkene có các phản ứng đặc trưng: phản ứng với Br2, trùng hợp tạo polymer.
Liên kết π kém bền nên alkene có các phản ứng đặc trưng: phản ứng với Br2, trùng hợp tạo polymer.
2. Tính chất hoá học của ethylene
2.1 Tác dụng với oxygen
Hiện tượng: khi đưa que diêm đang cháy vào miệng ống sẽ thấy ngọn lửa bùng sáng lên.
PTHH:
C2H4 + 3O2![]() 2CO2 + 2H2O
2CO2 + 2H2O
2.2 Tác dụng với nước bromine
Hiện tượng: Mất màu nước bromine.

Phương trình hoá học:
C2H4 + Br2 ![]() C2H4Br2
C2H4Br2
Biểu diễn bằng công thức cấu tạo:
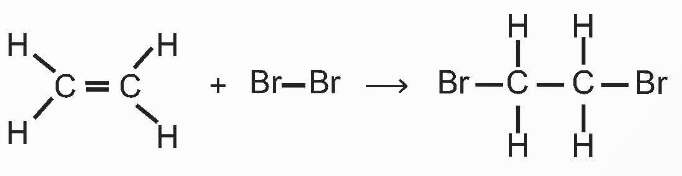
Biểu diễn bằng công thức cấu tạo thu gọn:
CH2 = CH2 + Br2 ![]() CH2Br – CH2Br
CH2Br – CH2Br
2.3 Phản ứng trùng hợp
Khái niệm: Trong điều kiện thích hợp, các phân tử có thể tham gia phản ứng cộng hợpliên tiếp lại với nhau tạo thành một phân tử có khối lượng lớn (polymer).
Phản ứng trùng hợp ethylene tạo thành polethylene (PE) ở nhiệt độ cao, áp suất cà chất xúc tác.
PTHH:
![]()
Kết luận
- Ethylene khi cháy trong không khí tạo CO2 và H2O, tỏa nhiều nhiệt.
- Ethylene làm mất màu nước bromine và tham gia phản ứng trùng hợp tạo PE.
- Tương tự ethylene, các alkene khác cũng có
+ Phản ứng cháy;
+ Phản ứng với nước bromine;
+ Tham gia phản ứng trùng hợp tạo thành polymer.
3. Một số ứng dụng của ethylene
- Sản xuất ethylic alcohol trong công nghiệp:
CH2 = CH2 + H2O![]() C2H5OH
C2H5OH
- Tổng hợp polyethylene (PE) từ phản ứng trùng hợp.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
Tóm tắt kiến thức Khoa học tự nhiên 9 CTST bài 22: Akene, kiến thức trọng tâm Khoa học tự nhiên 9 Chân trời sáng tạo bài 22: Akene, Ôn tập Khoa học tự nhiên 9 Chân trời sáng tạo bài 22: Akene
Giải bài tập những môn khác
Môn học lớp 9 KNTT
5 phút giải toán 9 KNTT
5 phút soạn bài văn 9 KNTT
Văn mẫu 9 kết nối tri thức
5 phút giải KHTN 9 KNTT
5 phút giải lịch sử 9 KNTT
5 phút giải địa lí 9 KNTT
5 phút giải hướng nghiệp 9 KNTT
5 phút giải lắp mạng điện 9 KNTT
5 phút giải trồng trọt 9 KNTT
5 phút giải CN thực phẩm 9 KNTT
5 phút giải tin học 9 KNTT
5 phút giải GDCD 9 KNTT
5 phút giải HĐTN 9 KNTT
Môn học lớp 9 CTST
5 phút giải toán 9 CTST
5 phút soạn bài văn 9 CTST
Văn mẫu 9 chân trời sáng tạo
5 phút giải KHTN 9 CTST
5 phút giải lịch sử 9 CTST
5 phút giải địa lí 9 CTST
5 phút giải hướng nghiệp 9 CTST
5 phút giải lắp mạng điện 9 CTST
5 phút giải cắt may 9 CTST
5 phút giải nông nghiệp 9 CTST
5 phút giải tin học 9 CTST
5 phút giải GDCD 9 CTST
5 phút giải HĐTN 9 bản 1 CTST
5 phút giải HĐTN 9 bản 2 CTST
Môn học lớp 9 cánh diều
5 phút giải toán 9 CD
5 phút soạn bài văn 9 CD
Văn mẫu 9 cánh diều
5 phút giải KHTN 9 CD
5 phút giải lịch sử 9 CD
5 phút giải địa lí 9 CD
5 phút giải hướng nghiệp 9 CD
5 phút giải lắp mạng điện 9 CD
5 phút giải trồng trọt 9 CD
5 phút giải CN thực phẩm 9 CD
5 phút giải tin học 9 CD
5 phút giải GDCD 9 CD
5 phút giải HĐTN 9 CD
Trắc nghiệm 9 Kết nối tri thức
Trắc nghiệm 9 Chân trời sáng tạo
Trắc nghiệm 9 Cánh diều
Tài liệu lớp 9
Văn mẫu lớp 9
Đề thi lên 10 Toán
Đề thi môn Hóa 9
Đề thi môn Địa lớp 9
Đề thi môn vật lí 9
Tập bản đồ địa lí 9
Ôn toán 9 lên 10
Ôn Ngữ văn 9 lên 10
Ôn Tiếng Anh 9 lên 10
Đề thi lên 10 chuyên Toán
Chuyên đề ôn tập Hóa 9
Chuyên đề ôn tập Sử lớp 9
Chuyên đề toán 9
Chuyên đề Địa Lý 9
Phát triển năng lực toán 9 tập 1
Bài tập phát triển năng lực toán 9

Bình luận