Lý thuyết trọng tâm hóa học 11 kết nối bài 17: Arene (Hydrocarbon thơm)
Tổng hợp kiến thức trọng tâm hóa học 11 kết nối bài 17: Arene (Hydrocarbon thơm). Tài liệu nhằm củng cố, ôn tập lại nội dung kiến thức bài học cho học sinh dễ nhớ, dễ ôn luyện. Kéo xuống để tham khảo
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
I. KHÁI NIỆM VÀ DANH PHÁP
1. Khái niệm
- Arene hay còn gọi là hydrocacbon thơm là những hydrocacbon trong phân tử có chứa một hay nhiều vòng benzene.
- Benzene có công thức C6H6 là hydrocacbon thơm đơn giản và điển hình nhất.
- Benzene và các đồng đẳng của nó hợp thành dãy đồng đẳng của benzene có công thức chung là CnH2n-6 (n≥6)
2. Công thức cấu tạo và danh pháp
Tên gốc ![]() là phenyl
là phenyl
Tên gốc ![]() là benzyl
là benzyl
Danh pháp
- Vòng benzen có 1 nhóm thế:
Gọi tên: Tên nhánh alkyl + benzene
- Vòng benzen có 2 hay nhiều nhóm thế:
Gọi tên: Số chỉ vị trí nhánh + tên nhánh + benzene
- Nếu vòng benzen có 2 nhóm ankyl ở vị trí:
- 1,2 gọi là vị trí ortho – kí hiệu (o -).
- 1,3 gọi là meta – kí hiệu ( m -).
- 1,4 gọi là para – kí hiệu ( p -).
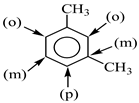
VD:
CTPT | CTCT | Tên gọi |
C6H6 |
| Benzene
|
C7H8 |
| Methylbenzene (toluen) |
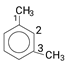
C8H10 |
| 1,2-dimethylbenzene (o-xylene) |
| 1,3-dimethylbenzene (m-xylene) | |
| 1,4-dimethylbenzene (p-xylene) | |
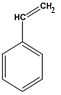
C8H8 |
| Vinylbenzene (styrene) |
II. ĐẶC ĐIỂM CẤU TẠO CỦA BEZENE
Benzene có công thức phân tử C6H6
6 nguyên tử carbon trong phân tử benzene nằm ở sáu đỉnh của một hình lục giác đều, toàn bộ phân tử nằm trên một mặt phẳng, các góc liên kết đều bằng 120o,
Độ dài liên kết carbon-carbon đều bằng 139 pm.
Benzene có công thức cấu tạo như hình
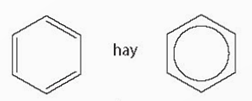
Khác với các hydrocarbon đã học là chỉ cấu tạo mạch hở, benzene có cấu tạo mạch vòng, phân tử có 3 liên kết đôi xen kẽ 3 liên kết đơn.
III. TÍNH CHẤT VẬT LÍ VÀ TRẠNG THÁI TỰ NHIÊN
1. Tính chất vật lí:
- Trong điều kiện thường, trừ naphthalene ở thể rắn, có màu trắng, các arene còn lại đều là những chất lỏng không màu, có mùi đặc trưng.
- Các arene không phân cực/ kém phân cực → hầu như không tan trong nước nhưng tan nhiều trong dung môi hữu cơ như acetone, diethyl ether, chloroform, …
- Hầu hết arene đều có hại cho sức khỏe nếu tiếp xúc trong một thời gian dài.
2. Trạng thái tự nhiên:
- Benzene, toluene, xylene có trong dầu mỏ với hàm lượng thấp.
- Naphthalene và các arene đa vòng khác có trong dầu mỏ và nhựa than đá.
IV. TÍNH CHẤT HOÁ HỌC
1. Phản ứng thế.
- Phản ứng halogen hóa.
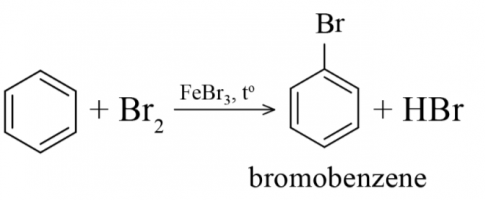
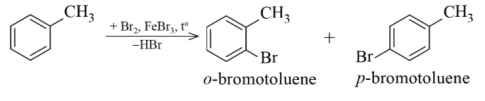
- Phản ứng nitro hóa
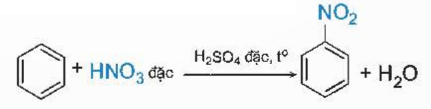
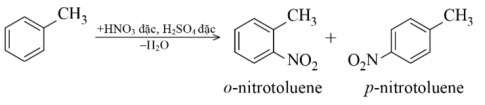
Nhận xét: Khi tham gia phản ứng thế các alkylbenzene dễ tham gia phản ứng thế nguyên tử H của vòng benzen hơn benzene và sự thế ưu tiên vị trí ortho và para so với vị trí nhóm alkyl.
2. Phản ứng cộng.
a) Cộng chlorine
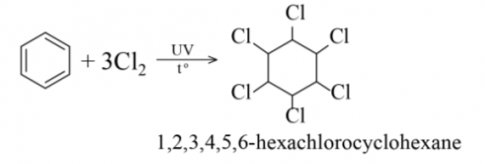
(1,2,3,4,5,6-hexachlorocyclohexane/ hexachlorocyclohexane)
b) Cộng hydrogen
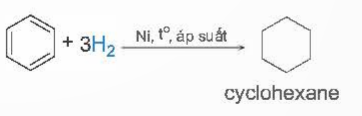
3. Phản ứng oxi hoá.
a) Phản ứng oxi hoá hoàn toàn.
CnH2n -6 + $\frac{3n-3}{2}$O2 $\overset{t^{o}}{\rightarrow }$ nCO2 + (n-3) H2O
Nhận xét: Các arene dễ cháy và tỏa nhiều nhiệt
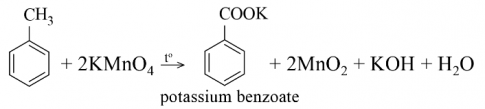
b) Phản ứng oxi hoá không hoàn toàn
- Benzene không làm mất màu dung dịch KMnO4.
- Các alkylbenzene khi đun nóng với KMnO4 thì chỉ có nhóm alkyl bị oxi hóa.
V. ỨNG DỤNG
- Tổng hợp các monomer trong sản xuất polimer làm chất dẻo, cao su, tơ sợi (chẳng hạn polystyrene, cao su buena-styrene, tơ caprone).
- Từ benzene người ta điều chế ra nitrobenzene, aniline, phenol dùng để tổng hợp phẩm nhuộm, dược phẩm, thuốc trừ dịch hại, ...
- Toluen được dùng để sản xuất thuốc nổ TNT (trinitrotoluene).
- Benzene, toluene và các xylene còn được dùng nhiều làm dung môi….
Cách ứng xử thích hợp với việc sử dụng arene trong việc bảo vệ sức khỏe con người - môi trường
- Arene có độc tính, cần được sử dụng một cách hợp lý
- Hạn chế sử dụng thuốc bảo vệ thực vật và chỉ sử dụng thuốc thế hệ mới.
VI. ĐIỀU CHẾ ARENE
Trong công nghiệp, arene hầu như được điều chế từ quá trình reforming phân đoạn dầu mỏ chứa alkane và cycloalkane từ C6 đến C8.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
Giải bài tập những môn khác
Giải sgk lớp 11 KNTT
Giải sgk lớp 11 CTST
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều


Bình luận