Bài 6.33: Trang 63 SBT hóa 10
Ba thí nghiệm được tiến hành với những khối lượng Zn bằng nhau và với \(50 cm^3\) dung dịch loãng \(H_2SO_4\) 2M. PTHH của phản ứng :
\(Zn + H_2SO_4 → ZnSO_4 + H_2↑\)
Bảng dưới đây cho biết các điều kiện của mỗi thí nghiệm :
Thí nghiệm | Kẽm | Nhiệt độ (°C) |
1 | bột | 30 |
2 | lá | 20 |
3 | lá | 30 |
Khí hiđro thu được trong mỗi thí nghiệm được ghi lại theo những khoảng cách nhất định về thời gian cho đến khi phản ứng kết thúc, được biểu diễn bằng đồ thị sau :
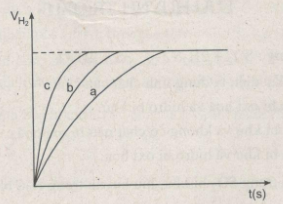
a) Rút ra được những nhận xét gì khi so sánh hiện tượng phản ứng của :
- Thí nghiệm 1 và thí nghiệm 3 ?
- Thí nghiệm 2 và thí nghiệm 3 ?
b) Hãy quan sát đồ thị trên để cho biết các đường cong a, b, c biểu thị cho những thí nghiệm nào ?
c) Ghi thể tích khí \(H_2\) trên trục y khi phản ứng kết thúc. Biết rằng ở điều kiện phòng thí nghiệm, 1 mol khí có thể tích là 24 lít và Zn còn dư sau các thí nghiệm.




Bình luận