Giải bài 5 Giới thiệu về liên kết hóa học
Giải bài 5: Giới thiệu về liên kết hóa học - sách cánh diều khoa học tự nhiên 7. Phần đáp án chuẩn, hướng dẫn giải chi tiết cho từng bài tập có trong chương trình học của sách giáo khoa. Hi vọng, các em học sinh hiểu và nắm vững kiến thức bài học.
I. Đặc điểm cấu tạo vỏ nguyên tử khí hiếm.
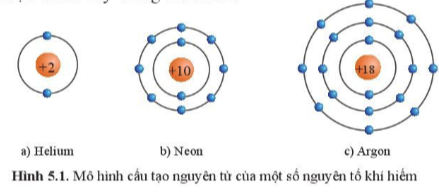
Câu hỏi 1. Quan sát hình 5.1 hãy cho biết số electron ở lớp ngoài cùng của vỏ nguyên tử khí hiếm
Hướng dẫn giải:
Lớp ngoài cùng của vỏ nguyên tử khí hiếm đều có 8 electron ( trừ nguyên tố He là 2 electron)
II. Liên kết ion
1. Sự tạo thành liên kết trong phân tử sodium chloride
Câu hỏi 2. Quan sát hình 5.2 và 5.3, cho biết lớp vỏ của các ion $Na^{+}$ , $Cl^{-}$ tương tự vỏ nguyên tử của nguyên tố khí hiếm nào?
Hướng dẫn giải:
- Xét ion Na+:
- Có 10 electron ở lớp vỏ
- Có 2 lớp electron
=> Lớp vỏ ion Na+ tương tự vỏ nguyên tử của nguyên tố khí hiếm Ne
- Xét ion Cl-
- Có 18 electron ở lớp vỏ
- Có 3 lớp electron
=> Lớp vỏ ion Cl- tương tự vỏ nguyên tử của nguyên tố khí hiếm Aron
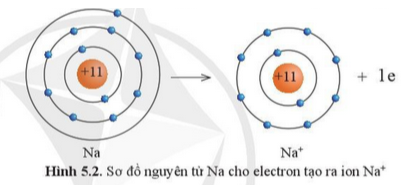
Câu hỏi 3. Quan sát hình 5.2, hãy so sánh về số electron, số lớp electron giữa nguyên tử Na và Na+
Hướng dẫn giải:
- Nguyên tử Na có 11 electron và 3 lớp electron
- Ion Na+ có 10 electron và 2 lớp electron
=> Nguyên tử Na đã mất đi 1 electron để tạo thành ion Na+
Luyện tập 1. Số electron ở lớp ngoài cùng của nguyên tử K và F lần lượt là 1 và 7. Hãy cho biết khi K hết hợp với F để tạo thành phân tử potassium fluoride, nguyên tử K cho hay nhận bao nhiêu electron. Vẽ sơ đồ tạo thành liên kết trong phân tử potassium fluoride
Hướng dẫn giải:
- Khi K liên kết với F tạo thành phân tử potassium fluoride sẽ diễn ra sự cho và nhận electron giữa 2 nguyên tử. Với nguyên tử K có 1 electron ở lớp ngoài cùng => Cho đi 1 electron ở lớp ngoài cùng để đạt cấu hình electron bền vững của khí hiếm
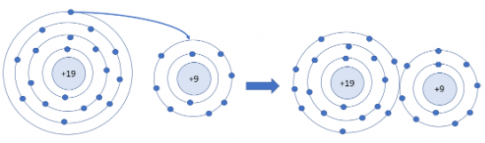
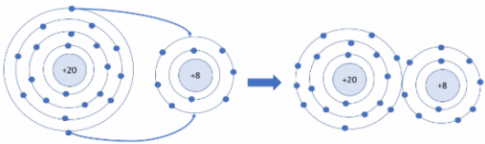
- Sơ đồ tạo thành liên kết trong phân tử potassium fluoride:



Bình luận