Đáp án Hóa học 11 Cánh diều bài 2 Sự điện li trong dung dịch nước, thuyết Bronsted - Lowry về acid - base
Đáp án bài 2 Sự điện li trong dung dịch nước, thuyết Bronsted - Lowry về acid - base. Bài giải được trình bày ngắn gọn, chính xác giúp các em học Hóa học 11 Cánh diều dễ dàng. Từ đó, hiểu bài và vận dụng vào các bài tập khác. Đáp án chuẩn chỉnh, rõ ý, dễ tiếp thu. Kéo xuống dưới để xem chi tiết
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
BÀI 2. SỰ ĐIỆN LI TRONG DUNG DỊCH NƯỚC, THUYẾT BRONSTED - LOWRY VỀ ACID – BASE
Câu 1: Quan sát Hình 2.1, em hãy nêu những sự khác nhau giữa chất điện li và chất không điện li.
Đáp án chuẩn:
| Dung dịch chất điện li | Dung dịch chất không điện li |
| Phân li thành ion | Không phân li thành ion |
| Dẫn điện | Không dẫn điện |
I. SỰ ĐIỆN LI, CHẤT ĐIỆN LI VÀ CHẤT KHÔNG ĐIỆN LI
Bài 1: Trong thí nghiệm trên, đèn sáng hay không sáng...
Đáp án chuẩn:
Tính chất dẫn điện
Bài 2: Dự đoán trong thí nghiệm trên...
Đáp án chuẩn:
Không sáng
Bài 3: Tìm hiểu và cho biết những chất nào sau đây thuộc loại chất điện li...
Đáp án chuẩn:
HCl, BaCl2, Ca(OH)2,CH3COOH.
II. THUYẾT BRONSTED - LOWRY VỀ ACID - BASE
Bài 1: Ở quá trình (3b), nước đóng vai trò là acid hay base? Vì sao?
Đáp án chuẩn:
Base. Vì nước nhận H+ để tạo ion H3O+.
Bài 2: Trong cân bằng (4), hãy chỉ ra hai acid và hai base. Giải thích.
Đáp án chuẩn:
| Chiều thuận | Chiều nghịch | |
| Acid | H2O | NH4+ |
| Base | NH3 | OH- |
Acid là những chất có khả năng cho H+, base là những chất có khả năng nhận +.
Bài 3: Dựa vào cân bằng (4) và (5), hãy giải thích vì sao H2O được cho là chất có tính lưỡng tính (là chất vừa có tính acid, vừa có tính base).
Đáp án chuẩn:
Ở cân bằng (4), H2O đóng vai trò là acid; (5) H2O đóng vai trò là base
Bài 4: Cho các chất sau: HBr, HI, H2S, KOH. Hãy phân loại chúng thành acid mạnh, base mạnh, acid yếu và base yếu.
Đáp án chuẩn:
Acid mạnh: HBr, HI
Acid yếu: H2S
Base mạnh: KOH
Base yếu: NH3
Bài 5: Trong các cân bằng (7), (8a) và (8b), xác định các acid và các base.
Đáp án chuẩn:
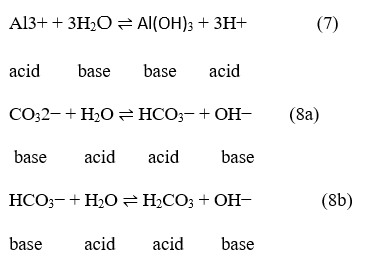
Bài 6: Tương tự Ví dụ 5, hãy cho biết dung dịch phèn...
Đáp án chuẩn:
Phèn sắt có môi trường acid.
Vì nó hoạt động theo nguyên tắc keo tụ, giúp loại bỏ được phosphate và các chất khác,...
BÀI TẬP CUỐI SGK
Bài 1: Nếu dòng điện chạy qua được dung dịch nước của một chất X...
Đáp án chuẩn:
c) d)
Bài 2*: Giải thích vì sao dung dịch HCl dẫn điện tốt hơn dung dịch CH3COOH có cùng nồng độ.
Đáp án chuẩn:
HCl phân li hoàn toàn thành các ion, còn CH3COOH chỉ phân li một phần
Bài 3: Giải thích vai trò của nước trong sự điện li của HCl và NaOH.
Đáp án chuẩn:
Nước là phân tử phân cực nên khi hoà tan một chất điện li (HCl hoặc NaOH) vào nước, xuất hiện tương tác của nước với các ion. Tương tác này sẽ bứt các ion khỏi tinh thể (hoặc phân tử) để tan vào nước.
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
Giải bài tập những môn khác
Giải sgk lớp 11 KNTT
Giải sgk lớp 11 CTST
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều

Bình luận