Soạn giáo án điện tử hóa học 11 CTST Bài 7: Sulfuric acid và muối sulfate
Giáo án powerpoint hóa học 11 chân trời sáng tạo mới. Giáo án soạn theo tiêu chí hiện đại, đẹp mắt với nhiều hình ảnh, nội dung, hoạt động phong phú, sáng tạo. Giáo án điện tử này dùng để giảng dạy online hoặc trình chiếu. Tin rằng, bộ bài giảng này sẽ hỗ trợ tốt việc giảng dạy và đem đến sự hài lòng với thầy cô.
Xem hình ảnh về giáo án








Còn nữa....Giáo án khi tải về là bản đầy đủ. Có full siles bài giảng!
Nội dung giáo án
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC MỚI
KHỞI ĐỘNG
Chất được nhắc đến trong video là gì? Nêu hiểu biết của em về chất đó.
BÀI 7.
SULFURIC ACID VÀ MUỐI SUNFATE
NỘI DUNG BÀI HỌC
SULFURIC ACID
MUỐI SULFATE
SULFURIC ACID
- Tính chất vật lí
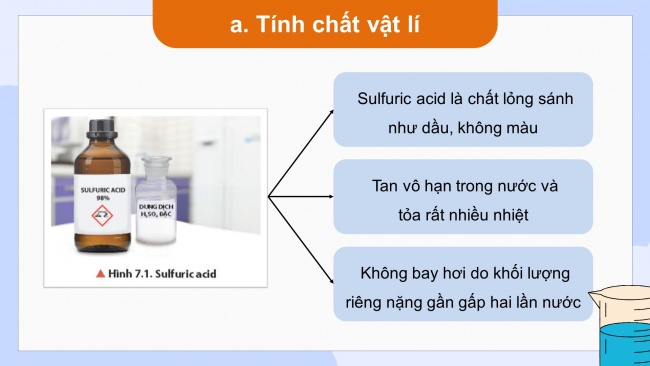
Quan sát hình 7.1 (hoặc mẫu vật thật):
Nhận xét màu, trạng thái của sulfuric acid ở điều kiện thường và cho biết tại sao sulfuric acid lại không bay hơi?
Sulfuric acid là chất lỏng sánh như dầu, không màu
Tan vô hạn trong nước và
tỏa rất nhiều nhiệt
Không bay hơi do khối lượng riêng nặng gần gấp hai lần nước
KẾT LUẬN
Sulfuric acid (H2SO4) là:
- Chất lỏng sánh như dầu, không màu, không bay hơi, nặng gần gấp 2 lần nước (H2SO4 98% có D = 1,84 g/cm3)
- Tan vô hạn trong nước và tỏa nhiệt rất nhiều nhiệt.
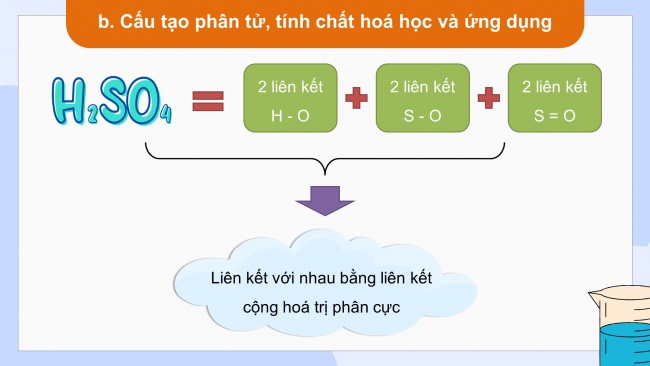
- Cấu tạo phân tử, tính chất hoá học và ứng dụng
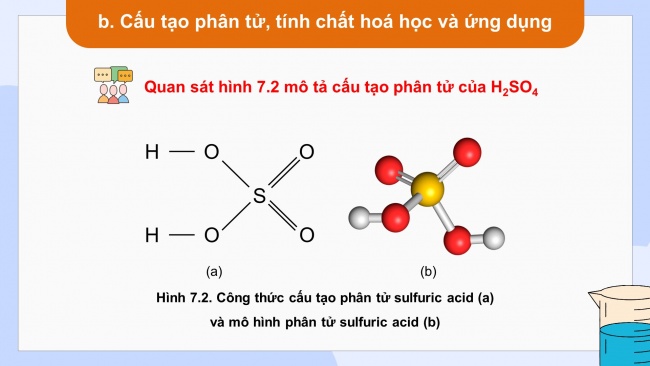
Quan sát hình 7.2 mô tả cấu tạo phân tử của H2SO4
Dựa vào CTCT xác định số OXH của S trong acid, viết phương trình điện li của H2SO4 và dự đoán tính chất hoá học của H2SO4
- Số OXH của S là +6 cao nhất
- Chỉ có xu hướng giảm số OXH khi tham gia phản ứng hoá học.
- Có tính oxi hoá.
- Phương trình điện li
H2SO4 → H + + HSO4-
HSO4- ⇄ H+ + SO42- (Ka ≈ 10-2)
→ H2SO4 là acid mạnh
Tính acid
H2SO4 loãng có đầy đủ tính chất của một acid mạnh
Làm đổi màu quỳ tím thành đỏ.
Tác dụng với nhiều kim loại (Mg, Al, Zn, Fe,...) tạo thành muối sulfate và giải phóng khí H2.
H2SO4(loãng) + Mg → MgSO4 + H2 (↑)
Tác dụng với oxide base, base, muối của các acid yếu → muối sulfate:
H2SO4 + CuO → CuSO4 + H2O
Tính acid
- Hiện tượng: ở ống nghiệm (a) có kết tủa trắng.
- PTHH: Ba(OH)2 + H2SO4 → 2H2O + BaSO4↓
- Hiện tượng: ở ống nghiệm (b) sủi bọt khí
- PTTH: H2SO4 + Na2CO3 → H2O + Na2SO4 + CO2 ↑
Tính oxi hoá
Thí nghiệm 1: Phản ứng của dung dịch H2SO4 đặc, nóng với Cu
- Ống nghiệm, bông, kẹp ống nghiệm, đèn cồn, H2SO4 đặc, dd NaOH, mảnh đồng.
- Cần phải cẩn thận khi sử dụng acid H2SO4 đặc vì khí sinh ra độc.
- Khi đốt chú ý nút kín bình chứa bằng bông tẩm NaOH, hướng miệng ống nghiệm về phía không có người, đeo khẩu trang khi làm thí nghiệm.
- Hiện tượng: Mảnh đồng tan dần, xuất hiện, bọt khí mạnh và tạo dung dịch màu xanh.
- PTHH:
- Cu + 2H2SO4đ → CuSO4 + SO2↑+ 2H2O
Câu hỏi 4. Viết phương viết quá trình oxi hóa và quá trình khử trong phản ứng của dung dịch H2SO4 đặc với Cu ở thí nghiệm 1
Quá trình khử: S+6 + 2e → S+4
Quá trình oxi hoá: Cu0 → Cu+2 + 2e
=> Xem toàn bộ Giáo án điện tử Hóa học 11 chân trời sáng tạo
Nâng cấp lên tài khoản VIP để tải tài liệu và dùng thêm được nhiều tiện ích khác
Xem thêm giáo án khác
GIÁO ÁN TỰ NHIÊN 11 CHÂN TRỜI SÁNG TẠO
Giáo án Toán 11 chân trời sáng tạo
Giáo án điện tử toán 11 chân trời sáng tạo
Giáo án Hóa học 11 chân trời sáng tạo
Giáo án điện tử Hóa học 11 chân trời sáng tạo
Giáo án Vật lí 11 chân trời sáng tạo
Giáo án điện tử vật lí 11 chân trời sáng tạo
Giáo án Sinh học 11 chân trời sáng tạo
Giáo án điện tử Sinh học 11 chân trời sáng tạo
GIÁO ÁN XÃ HỘI 11 CHÂN TRỜI SÁNG TẠO
Giáo án Ngữ văn 11 chân trời sáng tạo
Giáo án điện tử ngữ văn 11 chân trời sáng tạo
Giáo án Lịch sử 11 chân trời sáng tạo
Giáo án điện tử Lịch sử 11 chân trời sáng tạo
Giáo án Địa lí 11 chân trời sáng tạo
Giáo án điện tử địa lí 11 chân trời sáng tạo
Giáo án Kinh tế pháp luật 11 chân trời sáng tạo
Giáo án điện tử Kinh tế pháp luật 11 chân trời sáng tạo
GIÁO ÁN LỚP 11 CÁC MÔN CÒN LẠI
GIÁO ÁN LỚP 11 BỘ SÁCH KHÁC
Giáo án tất cả các môn lớp 11 kết nối tri thứcGiáo án tất cả các môn lớp 11 cánh diều
