Soạn giáo án điện tử hóa học 11 KNTT Bài 2: Cân bằng trong dung dịch nước
Giáo án powerpoint hóa học 11 kết nối tri thức mới. Giáo án soạn theo tiêu chí hiện đại, đẹp mắt với nhiều hình ảnh, nội dung, hoạt động phong phú, sáng tạo. Giáo án điện tử này dùng để giảng dạy online hoặc trình chiếu. Tin rằng, bộ bài giảng này sẽ hỗ trợ tốt việc giảng dạy và đem đến sự hài lòng với thầy cô.
Xem hình ảnh về giáo án










Còn nữa....Giáo án khi tải về là bản đầy đủ. Có full siles bài giảng!
Nội dung giáo án
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC MỚI
KHỞI ĐỘNG
Hình 2.1 cho thấy giá trị pH của dung dịch một số chất thông dụng. Vậy pH là gì? pH có ảnh hưởng gì đến đời sống? Xác định pH như thế nào?
BÀI 2. CÂN BẰNG TRONG DUNG DỊCH NƯỚC
NỘI DUNG BÀI HỌC
SỰ ĐIỆN LI
THUYẾT ACID – BASE CỦA BRONSTED
KHÁI NIỆM pH VÀ Ý NGHĨA CỦA pH TRONG THỰC TIỄN
SỰ THỦY PHÂN CỦA CÁC ION
CHUẨN ĐỘ ACID – BASE
- SỰ ĐIỆN LI
- Hiện tượng điện li
Quan sát thí nghiệm về tính dẫn điện của các chất tinh khiết (H2O và NaCl) và dung dịch NaCl
Thảo luận và trả lời câu hỏi hoạt động I.1 (SGK tr.17)
- Hãy nhắc lại khái niệm dòng điện.
- Đèn sáng cho thấy dung dịch NaCl dẫn điện, chứng tỏ trong dung dịch có hạt mang điện. Đó có thể là loại hạt nào (electron, phân tử NaCl, cation hay anion)?
- Hãy giải thích sự tạo thành hạt mang điện đó.
>>>
- Dòng điện là dòng chuyển dời có hướng của các hạt mang điện.
- Trong dung dịch muối ăn có ion âm (anion và ion dương (cation).
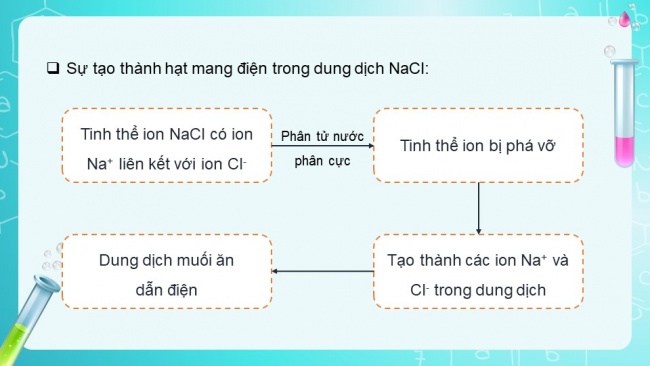
- Sự tạo thành hạt mang điện trong dung dịch NaCl:
Tinh thể ion NaCl có ion Na+ liên kết với ion Cl-
Phân tử nước phân cực
Tinh thể ion bị phá vỡ
Tạo thành các ion Na+ và Cl- trong dung dịch
Dung dịch muối ăn dẫn điện
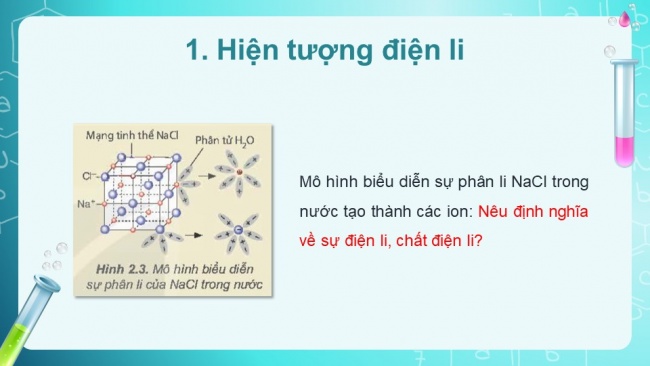
- Hiện tượng điện li
Mô hình biểu diễn sự phân li NaCl trong nước tạo thành các ion: Nêu định nghĩa về sự điện li, chất điện li?
Khái niệm
Quá trình phân li các chất trong nước tạo thành ion được gọi là sự điện li. Những chất khi tan trong nước phân li ra các ion được gọi là chất điện li.
- Chất điện li
Kết quả thử tính dẫn điện với các dung dịch hydrochloric acid (HCl), sodium hydroxide (NaOH), saccharose (C12H22O11), ethanol (C2H5OH) được trình bày trong bảng dưới đây.
Hãy hoàn thành các thông tin còn thiếu trong bảng vào vở.
| Dung dịch HCl | Dung dịch NaOH | Dung dịch saccharose | Dung dịch ethanol |
Hiện tượng | Đèn sáng | Đèn sáng | Đèn không sáng | Đèn không sáng |
Dung dịch dẫn điện/không dẫn điện | ? | ? | ? | ? |
Có/không có các ion trái dấu trong dung dịch | ? | ? | ? | ? |
Chất điện li/chất không điện li | ? | ? | ? | ? |
- Chất điện li và chất không điện li
- Các acid, base, muối khi hòa tan trong nước phân li ra các ion nên chúng là chất điện li.
- Nước tinh khiết, đường và ethanol trong nước không phân li ra các ion nên chúng là chất không điện li.
- Cách viết phương trình điện li:
- Acid H+ + anion gốc acid
- Acid H+ + anion gốc acid
- Base cation kim loại/ + OH-
- Muối cation kim loại/ + anion gốc acid
- Chất điện li mạnh và chất điện li yếu
Kết quả thử tính dẫn điện với dung dịch HCl 0,1M và dung dịch CH3COOH 0,1M cho thấy trường hợp cốc đựng dung dịch HCl 0,1M bóng đèn sáng hơn.
HOẠT ĐỘNG NHÓM
Hãy so sánh số ion mang điện trong hai dung dịch trên, từ đó cho biết acid nào phân li mạnh hơn?
- Số ion mang điện trong dung dịch HCl 0,1M nhiều hơn trong dung dịch CH3COOH 0,1M.
- Trong dung dịch, HCl phân li mạnh hơn CH3
Dựa vào mức độ phân li thành các ion, chất điện li được chia thành hai loại
Chất điện li mạnh
Là chất khi tan trong nước, hầu hết các phân tử chất tan đều phân li ra ion
Chất điện li yếu
Là chất khi tan trong nước chỉ có một phần số phân tử chất tan phân li ra ion, phần còn lại vẫn tồn tại ở dạng phân tử trong dung dịch
- Các chất điện li mạnh thường gặp:
- Acid mạnh: HCl, HNO3, H2SO4,...
- Base mạnh: NaOH, KOH, Ca(OH)2, Ba(OH)2,...
- Hầu hết các muối
- Quá trình phân li của chất điện li mạnh xảy ra gần như hoàn toàn và được biểu diễn bằng mũi tên một chiều.
- HNO3 H+ +
- NaOH Na+ + OH-
- Na2CO3 2Na+ +
- Những chất điện li yếu gồm:
- Các acid yếu: CH3COOH, HClO, HF, H2CO3,...
- Các base yếu: Cu(OH)2, Fe(OH)2,...
- Quá trình phân li của chất điện li yếu là một phản ứng thuận nghịch và được biểu diễn bằng hai nửa mũi tên ngược chiều nhau:
CH3COOH H+ + CH3COO-
Phương trình phân tử, phương trình ion và ion rút gọn
Nâng cấp lên tài khoản VIP để tải tài liệu và dùng thêm được nhiều tiện ích khác
Xem thêm giáo án khác
GIÁO ÁN TỰ NHIÊN 11 KẾT NỐI TRI THỨC
Giáo án Toán 11 kết nối tri thức
Giáo án điện tử toán 11 kết nối tri thức
Giáo án Vật lí 11 kết nối tri thức
Giáo án điện tử vật lí 11 kết nối tri thức
Giáo án Hóa học 11 kết nối tri thức
Giáo án điện tử Hóa học 11 kết nối tri thức
Giáo án Sinh học 11 kết nối tri thức
Giáo án điện tử Sinh học 11 kết nối tri thức
Giáo án Công nghệ cơ khí 11 kết nối tri thức
Giáo án điện tử Công nghệ cơ khí 11 kết nối tri thức
Giáo án Công nghệ chăn nuôi 11 kết nối tri thức
Giáo án điện tử Công nghệ chăn nuôi 11 kết nối tri thức
Giáo án Tin học ứng dụng 11 kết nối tri thức
Giáo án điện tử Tin học ứng dụng 11 kết nối tri thức
Giáo án Khoa học máy tính 11 kết nối tri thức
Giáo án điện tử Khoa học máy tính 11 kết nối tri thức
GIÁO ÁN XÃ HỘI 11 KẾT NỐI TRI THỨC
Giáo án Ngữ văn 11 kết nối tri thức
Giáo án điện tử ngữ văn 11 kết nối tri thức
Giáo án Lịch sử 11 kết nối tri thức
Giáo án điện tử Lịch sử 11 kết nối tri thức
Giáo án Địa lí 11 kết nối tri thức
Giáo án điện tử địa lí 11 kết nối tri thức
Giáo án Kinh tế pháp luật 11 kết nối tri thức
Giáo án điện tử Kinh tế pháp luật 11 kết nối tri thức
GIÁO ÁN LỚP 11 CÁC MÔN CÒN LẠI
Giáo án Hoạt động trải nghiệm 11 kết nối tri thức
Giáo án điện tử Hoạt động trải nghiệm 11 kết nối tri thức
GIÁO ÁN LỚP 11 BỘ SÁCH KHÁC
Giáo án tất cả các môn lớp 11 cánh diềuGiáo án tất cả các môn lớp 11 chân trời sáng tạo
