Hợp chất X được sử dụng làm thuốc pháo, ngòi nổ, thuốc đầu diêm, thuốc giúp nhãn ra hoa,... X có khối lượng mol bằng 122,5 g/mol, chứa ba nguyên tố, trong đó nguyên tố s có 7 electron s, nguyên tố p có 11 electron p và nguyên tố p có 4 electron p. Thành p
14.17. Hợp chất X được sử dụng làm thuốc pháo, ngòi nổ, thuốc đầu diêm, thuốc giúp nhãn ra hoa,... X có khối lượng mol bằng 122,5 g/mol, chứa ba nguyên tố, trong đó nguyên tố s có 7 electron s, nguyên tố p có 11 electron p và nguyên tố p có 4 electron p. Thành phần phần trăm khối lượng nguyên tố có 4 electron p trong X bằng 39,19%.
a) Xác định công thức phân tử của X.
b) Viết công thức câu tạo Lewis, chỉ rõ loại liên kết có trong X.
a) Nguyên tố s có 7 electron s là K ($1s^{2}2s^{2}2p^{6}3s^{2}3p^{6}4s^{1}$);
nguyên tố p có 11 electron p là Cl ($1s^{2}2s^{2}2p^{6}3s^{2}3p^{5}$);
nguyên tố p có 4 electron p là O ($1s^{2}2s^{2}2p^{4}$);
Khối lượng O trong X là: 122,5 . 0,3919 ≈ 48 (amu) ứng với 3 nguyên tử O.
Công thức X có dạng KxClyO3.
Theo bài ra ta có: 39x + 35,5y = 122,5 - 48 = 74,5.
⇒x = y = 1 = công thức X: KClO3.
b) Cấu tạo X: 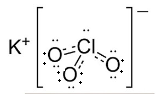
gồm liên kết K$^{+}$ và ClO3$^{-}$ là liên kết ion; liên kết đơn Cl - O và liên kết kép Cl = O là các liên kết cộng hoá trị phân cực
Xem toàn bộ: Giải SBT Hoá 10 kết nối bài 14: Ôn tập chương 3

Bình luận