3. Sự lai hoá obital nguyên tử
Câu hỏi 9: Vì sao góc liên kết HCH trong phân tử methane không thể là 90o?
Câu hỏi 10: Em có nhận xét gì về hình dạng, kích thước, năng lượng và hướng của các orbital nguyên tử lai hóa?
Câu hỏi 11: Nếu tổng số các AO tham gia lai hóa là 3 sẽ tạo ra bao nhiêu AO lai hóa?
Câu hỏi 12: Nguyên tử carbon trong phân tử CO2 ở trạng thái lai hóa nào? Giải thích liên kết hóa học tạo thành trong phân tử CO2 theo thuyết lai hóa.
Câu hỏi 13: Theo mô hình VSEPR, phân tử formaldehyde có dạng tam giác phẳng. Xác định trạng thái lai hóa của nguyên tử trung tâm carbon. Cho biết formaldehyde có công thức như hình sau đây:
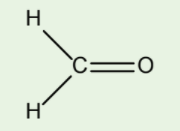
Câu hỏi 14: Tương tự như công thức VSEPR, có thể dự đoán nhanh trạng thái lai hóa của nguyên tử A (nguyên tố s, p) trong một phân tử bất kì như sau:
- Xác định số nguyên tử liên kết trực tiếp với A.
- Xác định số cặp electron hóa trị riêng của A.
- Nếu tổng hai giá trị là 2; 3 hoặc 4 thì trạng thái lai hóa của A lần lượt là sp; sp2 hoặc sp3
Dự đoán trạng thái lai hóa của nguyên tử C, S và N trong các phân tử CO2, SO2 và NH3
Câu hỏi 15: Phân tử chứa nguyên tử lai hóa sp3 có cấu trúc phẳng không? Giải thích và cho ví dụ.
Câu hỏi luyện tập: Biết nguyên tử oxygen trong phân tử H2O ở trạng thái lai hóa sp3. Trình bày sự hình thành liên kết hóa học trong phân tử H2O



Bình luận