Slide bài giảng Vật lí 12 Cánh diều bài 1: Cấu trúc hạt nhân
Slide điện tử bài 1: Cấu trúc hạt nhân. Trình bày với các hiệu ứng hiện đại, hấp dẫn. Giúp học sinh hứng thú học bài. Học nhanh, nhớ lâu. Có tài liệu này, hiệu quả học tập của môn Vật lí 12 Cánh diều sẽ khác biệt
Bạn chưa đủ điều kiện để xem được slide bài này. => Xem slide bài mẫu
Tóm lược nội dung
BÀI 1. CẤU TRÚC HẠT NHÂN
MỞ ĐẦU
Câu hỏi: Vào đầu những năm 1900, các nhà khoa học đã khám phá ra rằng nguyên tử có dạng hình cầu và trung hòa về điện với điện tích âm là các hạt electron. Nhưng người ta chưa biết điện tích dương được phân bố thế nào trong hình cầu nguyên tử.
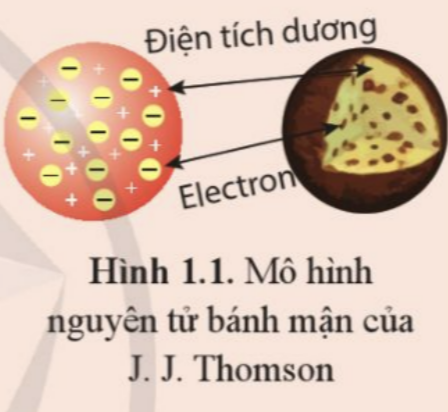
Năm 1904, Joseph John Thomson (Giô-dép Giôn Tôm-xơn) đã để xuất một mô hình nguyên tử được gọi là mô hình nguyên tử bánh mận (Plum Pudding Atomic Model). Theo mô hình này các electron nằm rải rác trong một hình cầu tích điện dương giống như các quả mận nằm rải rác trong cái bánh (Hình 1.1).
Người ta đã kiểm chứng mô hình nguyên tử của Thomson như thế nào?
Trả lời rút gọn:
Mô hình nguyên tử bánh mận của Joseph John Thomson, đã được kiểm chứng thông qua nhiều thí nghiệm, trong đó nổi bật là thí nghiệm hạt Rutherford.
I. PHÁT HIỆN RA HẠT NHÂN NGUYÊN TỬ
Câu 1: Bằng chứng cụ thể nào trong thí nghiệm tán xạ hạt ![]() của Rutherford chứng tỏ hạt nhân có kích thước rất nhỏ nhưng tập trung toàn bộ điện tích dương và phần lớn khối lượng của nguyên tử?
của Rutherford chứng tỏ hạt nhân có kích thước rất nhỏ nhưng tập trung toàn bộ điện tích dương và phần lớn khối lượng của nguyên tử?
Trả lời rút gọn:
Trong thí nghiệm tán xạ hạt α của Rutherford, các hạt α (hạt Helium với điện tích dương) được bắn vào mẫu vật chứa nguyên tử, trong trường hợp này là một lá vàng mỏng. Khi các hạt α đi qua mẫu vật, một phần chúng bị phản xạ lại, trong khi một phần khác bị giảm tốc và thay đổi hướng do tương tác với các thành phần của nguyên tử, tuy nhiên phần lớn các hạt vẫn đi thẳng và không bị đổi hướng, do đó ông đã kết luận rằng hầu hết khối lượng và tất cả điện tích dương của nguyên tử tập trung ở một vùng nhỏ tại trung tâm của nguyên tử, gọi là hạt nhân.
Trong thí nghiệm tán xạ hạt α của Rutherford, các hạt α được bắn vào mẫu vật chứa nguyên tử (lá vàng mỏng). . Kết quả cho thấy rằng hầu hết khối lượng và toàn bộ điện tích dương của nguyên tử tập trung ở một vùng nhỏ tại trung tâm của nguyên tử, được gọi là hạt nhân.
II. CẤU TRÚC HẠT NHÂN
Luyện tập 1: Hạt nhân ![]() có bao nhiêu nucleon, bao nhiêu proton và bao nhiêu neutron?
có bao nhiêu nucleon, bao nhiêu proton và bao nhiêu neutron?
Trả lời rút gọn:
Số proton = Z = 30 hạt.
Số nucleon = A = 67 hạt.
Số neutron = N = A – Z = 67 – 30 = 37 hạt.
Luyện tập 2: Xác định điện tích của hạt nhân ![]()
Trả lời rút gọn:
Số proton = 30 hạt => điện tích của hạt nhân là +30e.
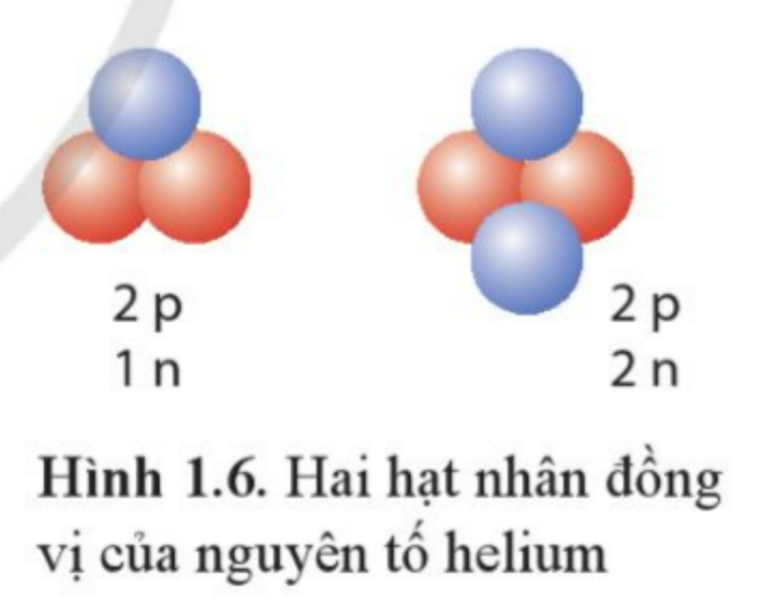
Luyện tập 3: Helium có hai đồng vị mà hạt nhân được biểu diễn như Hình 1.6. Viết kí hiệu hạt nhân của hai đồng vị helium đó.
Trả lời rút gọn:
Đồng vị số 1: Z = 2 và A = 2 +1 = 3 => 32He
Đồng vị số 2: Z = 2 và A = 2 + 2 = 4 => 42He
Vận dụng: Hầu hết các nguyên tố đều có nhiều đồng vị. Khối lượng nguyên tử của nguyên tố trong bảng tuần hoàn là khối lượng trung bình của các nguyên tử đồng vị có trong tự nhiên. Nguyên tố chlorine (Cl) có hai đồng vị bền là:
+ ![]() có khối lượng nguyên tử m = 34,96885 u và chiếm 75,77% chlorine trong tự nhiên.
có khối lượng nguyên tử m = 34,96885 u và chiếm 75,77% chlorine trong tự nhiên.
+ ![]() có khối lượng nguyên tử m = 36,96590 u và chiếm 24,23% chlorine trong tự nhiên.
có khối lượng nguyên tử m = 36,96590 u và chiếm 24,23% chlorine trong tự nhiên.
Tính khối lượng nguyên tử trung bình của nguyên tố chlorine.
Trả lời rút gọn:
Nguyên tử khối trung bình của nguyên tố chlorine:
![]()
