Slide bài giảng Hóa học 12 Chân trời bài 16: Hợp kim, sự ăn mòn kim loại
Slide điện tử bài 16: Hợp kim, sự ăn mòn kim loại. Trình bày với các hiệu ứng hiện đại, hấp dẫn. Giúp học sinh hứng thú học bài. Học nhanh, nhớ lâu. Có tài liệu này, hiệu quả học tập của môn Hóa học 12 Chân trời sáng tạo sẽ khác biệt
Bạn chưa đủ điều kiện để xem được slide bài này. => Xem slide bài mẫu
Tóm lược nội dung
BÀI 16. HỢP KIM – SỰ ĂN MÒN KIM LOẠI
MỞ ĐẦU
Thiết bị, vật dụng, công trình làm bằng kim loại thường bị hư hỏng sau một thời gian do sự ăn mòn kim loại. Tuy nhiên, nếu hiểu rõ nguyên nhân của quá trình ăn mòn kim loại, con người có thể giảm thiểu tác động của quá trình ăn mòn. Ăn mòn kim loại là gì? Làm thế nào để chống ăn mòn kim loại?
Trả lời rút gọn:
Ăn mòn kim loại là sự phá huỷ kim loại hoặc hợp kim do tác dụng của các chất trong môi trường.
Để chống ăn mòn kim loại, người ta có thể dùng phương pháp bảo vệ bề mặt và phương pháp điện hoá.
1. HỢP KIM
Thảo luận 1: Hãy kể tên một số hợp kim thường gặp trong cuộc sống.
Trả lời rút gọn:
Một số hợp kim thường gặp trong cuộc sống: gang, thép, đồng nickel, inox,…
Thảo luận 2: Nêu một số ví dụ về tính chất của hợp kim mà em biết.
Trả lời rút gọn:
Một số ví dụ về tính chất của hợp kim:
Hợp kim nhôm nhẹ, bền dùng để chế tạo các chi tiết máy bay, ô tô,…
Hợp kim thép cứng và bền dùng để xây dựng nhà cửa, cầu cống,…
- Inox (thép không gỉ) ít bị ăn mòn nên được dùng để chế tạo các dụng cụ y tế, dụng cụ nhà bếp,…
Thảo luận 3: Hãy so sánh thành phần, tính chất và ứng dụng của gang và thép.
Trả lời rút gọn:
| Gang | Thép |
Thành phần | Là hợp kim của sắt với carbon, hàm lượng carbon chiếm từ 2 – 5%, ngoài ta còn một số lượng nhỏ các nguyên tố khác. | Là hợp kim của sắt với carbon và một số nguyên tố khác, trong đó hàm lượng carbon chiếm dưới 2%. |
Tính chất | Tính cứng và giòn hơn sắt. | Cứng, chống ăn mòn. |
Ứng dụng | Luyện thép, đúc bệ máy, ống dẫn nước,… | Vật liệu xây dựng, chế tạo máy, dụng cụ lao động,… |
2. ĂN MÒN KIM LOẠI
Thảo luận 4: Hãy tìm hiểu và cho biết các yếu tố nào có thể gây nên sự ăn mòn kim loại. Cho biết bản chất của quá trình này.
Trả lời rút gọn:
Các yếu tố gây nên sự ăn mòn kim loại O2 trong không khí, các acid yếu trong nước mưa, một số muối NaCl, MgCl2 trong nước biển,… Những chất này tác dụng với kim loại hoặc hợp kim tạo ra gỉ sắt xốp, giòn làm đồ vật bị ăn mòn.
- Bản chất của quá trình này là quá trình oxi hoá – khử.
Thảo luận 5: Xác định chất oxi hoá, chất khử trong các phản ứng ở Ví dụ 2. Viết quá trình oxi hoá, quá trình khử của các phản ứng đó.
Trả lời rút gọn:
Trong phản ứng trên: chất khử là Fe, chất oxi hoá là O2.
- Quá trình oxi hoá: 3Fe →
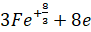
Quá trình khử: O2 + 4e → 2O2-
Quá trình oxi hoá: 3Fe →
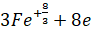
Trong phản ứng dưới: chất khử là Fe, chất oxi hoá là H2O
Quá trình khử: 2H+ + 2e → H2
Thảo luận 6: Tiến hành Thí nghiệm 1, nêu hiện tượng xảy ra khi chưa nối dây dẫn điện và sau khi nối dây dẫn.
Trả lời rút gọn:
- Khi chưa nối dây dẫn điện, thanh sắt bị hoà tan trong dung dịch, có khí thoát ra
- Sau khi nối dây dẫn điện, giữa thanh sắt và thanh đồng hình thành một pin điện hoá cung cấp dòng điện làm cho đèn sáng.
Thảo luận 7: Xác định các quá trình oxi hoá, quá trình khử xảy ra ở Thí nghiệm 1.
Trả lời rút gọn:
Quá trình oxi hoá: Fe → Fe2+ + 2e
Quá trình khử: 2H+ + 2e → H2
Luyện tập: Một sợi dây đồng được nối với một dây nhôm. Có hiện tượng gì xảy ra ở chỗ nối của hai kim loại khi để lâu ngoài không khí ẩm? Giải thích.
Trả lời rút gọn:
Nối một sợi dây nhôm với một sợi dây đồng rồi để lâu trong không khí ẩm sẽ xảy ra hiện tượng ăn mòn điện hoá, tại chỗ nối của hai kim loại xảy ra quá trình oxi hoá nhôm vì tính khử của Al mạnh hơn Cu nên Al sẽ bị ăn mòn.
3. CHỐNG ĂN MÒN KIM LOẠI
Thảo luận 8: Thực hiện trước Thí nghiệm 2 ở nhà và nêu hiện tượng xảy ra. Giải thích.
Trả lời rút gọn:
Ở cốc 1 có hiện tượng đinh sắt bị ăn mòn điện hoá và tốc độ ăn mòn khá nhanh vì NaCl là chất điện li mạnh, khi kim loại tiếp xúc với dung dịch điện li sẽ xảy ra quá trình ăn mòn điện hoá.
Ở cốc 2 có hiện tượng dây kẽm bị ăn mòn còn đinh sắt phần bị dây kẽm quấn bị ít ăn mòn thậm chí không bị ăn mòn vì đinh sắt có dây kẽm bảo vệ bên ngoài, kim loại mạnh hơn sắt nên khi tiếp xúc với dung dịch điện li thì kẽm sẽ bị ăn mòn trước.
Vận dụng: Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn các khối kẽm vào phía ngoài vỏ tàu ở phần chìm trong nước biển. Hãy giải thích.
Trả lời rút gọn:
Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn các khối kẽm vào phía ngoài vỏ tàu ở phần chìm trong nước biển vì trong dãy hoạt động hoá học, kẽm hoạt động mạnh hơn sắt (thép) nên kẽm sẽ bị ăn mòn trước và vỏ tàu sẽ có tuổi thọ lâu hơn.
BÀI TẬP
Bài 1: Phân biệt ăn mòn hoá học và ăn mòn điện hoá.
Trả lời rút gọn:
Yếu tố | Ăn mòn hoá học | Ăn mòn điện hoá |
Điều kiện xảy ra ăn mòn | Thường xảy ra khi kim loại tiếp xúc với không khí, không khí ẩm | Các điện cực phải khác nhau, có thể cặp hai kim loại khác nhau hoặc cặp kim loại – phi kim hoặc cặp kim loại – hợp chất hoá học. Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn, các điện cực phải tiếp xúc với dung dịch điện li. |
Bản chất của sự ăn mòn | Là quá trình oxi hoá – khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường, ăn mòn xảy ra chậm. | Là sự ăn mòn kim loại do tác dụng của dung dịch điện li tạo nên dòng điện, ăn mòn điện hoá xảy ra nhanh hơn ăn mòn hoá học. |
Bài 2: Ăn mòn điện hoá các hợp kim của sắt (gang, thép) trong không khí ẩm ảnh hưởng lớn đối với nền kinh tế của các quốc gia. Hãy giải thích quá trình ăn mòn này.
Trả lời rút gọn:
Sự ăn mòn điện hoá một vật bằng sắt (gang, thép) trong môi trường không khí ẩm có hoà tan khí CO2, SO2, O2,… sẽ tạo ra một lớp dung dịch điện li phủ bên ngoài kim loại, cực âm là Fe, cực dương là C.
Ở cực dương xảy ra phản ứng khử: H2O + 4e +
 O2 → 2OH-
O2 → 2OH-Ở cực âm xảy ra phản ứng oxi hoá: Fe → Fe2+ + 2e
Ion Fe2+ tan vào trong dung dịch và tạo thành gỉ sắt có thành phần Fe2O3.nH2O
Bài 3: Một vật bằng sắt tây (sắt tráng thiếc) bị xây xát chạm tới lớp sắt bên trong. Nêu hiện tượng xảy ra khi để vật này lâu trong không khí ẩm. Giải thích.
Trả lời rút gọn:
Hiện tượng xảy ra khi để vật này lâu trong không khí ẩm là ăn mòn điện hoá vì khi cả hai kim loại đều tiếp xúc với không khí ẩm sắt hoạt động mạnh hơn thiếc nên sắt bị oxi hoá, còn ở cực dương xảy ra sự khử H2O; kết quả tạo ra gỉ sắt.
