Giải SBT hóa 11: bài tập 8.14 trang 59
Bài 8.14: Trang 59 SBT hóa 11
Chất A là một ancol no mạch hở. Để đốt cháy hoàn toàn 0,35 mol A phải dùng vừa hết 31,36 lít O2 (đktc). Hãy xác định công thức phân tử, công thức cấu tạo và tên của A.
Ancol no mạch hở có CTTQ: CnH2n+2Ox.
nO2 = $\frac{31,36}{22,4}$ = 1,4 mol
PTHH:
\({C_n}{H_{2n + 2}}{O_x} + \frac{{3n + 1 - x}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
0,35 1,4 (mol)
Theo PTHH: => \(\frac{{3n + 1 - x}}{2}\) = \(\frac{{1,4}}{{0,35}}\) = 4
=>3n + 1 - x = 8 => x = 3n - 7
Mặt khác ta có: Ở các ancol đa chức, mỗi nguyên tử cacbon không thể kết hợp với quá 1 nhóm OH => n ≥ x ≥ 1
<=> n ≥ 3n – 7 ≥ 1
<=> n ≥ 3n – 7 và 3n – 7 ≥ 1
<=> n ≤ 3,5 và n ≥ 2,67
<=> 3,5 ≥ n ≥ 2,67, mà n là số nguyên => n = 3
=>x = 2 => Công thức phân tử : C3H8O2.
Các công thức cấu tạo có thể có của A:
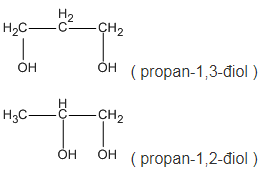
Xem toàn bộ: Giải SBT hóa 11 bài 40: Ancol trang 59
Giải những bài tập khác
Giải bài tập những môn khác
Đang cập nhật dữ liệu...

Bình luận