Lý thuyết trọng tâm hóa học 11 kết nối bài 10: Hợp chất hữu cơ và hóa học hữu cơ
Tổng hợp kiến thức trọng tâm hóa học 11 kết nối bài 10: Hợp chất hữu cơ và hóa học hữu cơ. Tài liệu nhằm củng cố, ôn tập lại nội dung kiến thức bài học cho học sinh dễ nhớ, dễ ôn luyện. Kéo xuống để tham khảo
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
I. HỢP CHẤT HỮU CƠ VÀ HÓA HỌC HỮU CƠ
1. Khái niệm
- Hợp chất của carbon là hợp chất hữu cơ (trừ một số hợp chất như carbon monoxide, carbon dioxide, muối carbonate, cyanide, carbide, ...)
- Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
2. Đặc điểm chung của các hợp chất hữu cơ
- Thành phần phân tử nhất thiết phải chứa nguyên tố carbon
- Liên kết hóa học chủ yếu là liên kết cộng hóa trị
- Nhiệt độ nóng chảy và nhiệt độ sôi thấp, không tan hoặc ít tan trong nước, tan trong các dung môi hữu cơ
- Dễ cháy, kém bền với nhiệt nên dễ bị phân hủy
- Phản ứng của các hợp chất hữu cơ thường xảy ra chậm, theo chiều hướng tạo ra hỗn hợp các sản phẩm.
II. PHÂN LOẠI HỢP CHẤT HỮU CƠ
Dựa vào thành phần nguyên tố, hợp chất hữu cơ phân thành hai loại:
- Hydrocarbon: là những hợp chất hữu cơ chỉ được tạo thành từ hai nguyên tố carbon và hydrogen
Ví dụ: Alkane (CH$_{4}$), alkene (CH$_{2}$=CH$_{2}$), alkyne (CH☰CH), arene (C$_{6}$H$_{6}$)
- Dẫn xuất của hydrocarbon: là những hợp chất hữu cơ mà trong phân tử ngoài nguyên tố carbon còn có các nguyên tố như oxygen, nitrogen, sulfur, halogen,...
Ví dụ: Dẫn xuất halogen (CH$_{3}$Cl), alcohol (C$_{2}$H$_{5}$OH), carboxylic acid (CH$_{3}$COOH)
III. NHÓM CHỨC TRONG PHÂN TỬ HỢP CHẤT HỮU CƠ
1. Khái niệm
Nhóm chức là nguyên tử hoặc nhóm nguyên tử trong phân tử gây ra những tính chất hóa học đặc trưng của hợp chất hữu cơ.
Ví dụ:
- Dimethyl ether và enthanol đều có cùng CTPT C$_{2}$H$_{6}$O
- Cấu tạo ethanol có nhóm –OH, dimethyl ether có nhóm –O–
- Ethanol tác dụng được với Na, dimethyl ether không tác dụng được với Na:
2C$_{2}$H$_{5}$OH + Na → 2C$_{2}$H$_{5}$ONa + Na
2. Một số loại nhóm chức cơ bản
Loại hợp chất | Nhóm chức | Ví dụ |
Dẫn xuất halogen | –X (F, Cl, Br, I) | CH$_{3}$Cl |
Alcohol | –OH | CH$_{3}$OH |
Aldehyde | –CHO | CH$_{3}$CHO |
Ketone | >CO | CH$_{3}$COCH$_{3}$ |
Carboxylic acid | –COOH | CH$_{3}$COOH |
Ester | –COO– | CH$_{3}$COOCH$_{3}$ |
Amine | –NH$_{2}$ | CH$_{3}$NH$_{2}$ |
Ether | –O– | CH$_{3}$OCH$_{3}$ |
3. Pha hồng ngoại và nhóm chức
- Phương pháp phổ hồng ngoại (Infrared Spectroscopy, viết tắt IR) là phương pháp vật lí rất quan trọng và phổ biến để nghiên cứu cấu tạo phân tử hợp chất hữu cơ.
- Mỗi liên kết trong phân tử hợp chất hữu cơ hấp thụ một vài bức xạ hồng ngoại đặc trưng cho liên kết đó
Nhóm chức/liên kết | Số sóng (cm$^{-1}$) |
-OH (alcohol) | 3 500 – 3 200 |
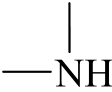
(amine) | 3 300 – 3 000 |
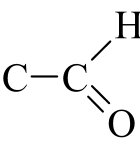
(aldehyde) | 2 830 – 2695 (C–H) 1 740 – 1 685 (C=O) |
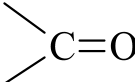
(ketone) | 1 715 – 1 666 (C=O) |
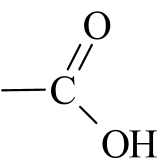
(carboxylic) | 3 300 – 2 500 (O–H) 1 760 – 1 690 (C=O) |
(ester) | 1 750 – 1 715 (C=O) |
Bảng 10.2. Số sóng hấp thụ đặc trưng trên phổ hồng ngoại của một số nhóm chức cơ bản
Nếu chưa hiểu - hãy xem: => Lời giải chi tiết ở đây
Nội dung quan tâm khác
Thêm kiến thức môn học
Giải bài tập những môn khác
Giải sgk lớp 11 KNTT
Giải sgk lớp 11 CTST
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều

Bình luận