Lý thuyết trọng tâm hóa học 11 cánh diều bài 4: Đơn chất Nitrogen
Tổng hợp lý thuyết trọng tâm hóa học 11 cánh diều bài 4: Đơn chất Nitrogen. Tài liệu nhằm củng cố, ôn tập lại nội dung kiến thức bài học cho học sinh dễ nhớ, dễ ôn luyện. Kéo xuống để tham khảo.
I. TRẠNG THÁI TỰ NHIÊN CỦA NGUYÊN TỐ NITROGEN
- Nguyên tố nitrogen có kí hiệu hóa học là N, số hiệu nguyên tử là 7, độ âm điện là 3,04.
- Trong tự nhiên, nitrogen tồn tại ở cả dạng đơn chất và hợp chất.
- Trong khí quyển, nguyên tố nitrogen tồn tại chủ yếu ở dạng đơn chất, N2. Khí nitrogen chiếm khoảng 78% thể tích không khí.
- Trong đất và nước, nitrogen tồn tại chủ yếu dưới dạng ion nitrate ($NO_{3}^{-}$), nitrite ($NO_{2}^{-}$) và ammonium ($NH_{4}^{+}$).
- Nguyên tố nitrogen có trong cơ thể của mọi sinh vật, chủ yếu ở dạng các hợp chất hữu cơ như amino acid, nucleic acid, protein, chlorophyll (chất diệp lục),…
II. ĐƠN CHẤT NITROGEN
1. Đặc điểm liên kết
- Phân tử N2 có liên kết ba giữa hai nguyên tử nitrogen, cả hai nguyên tử này đều thỏa mãn quy tắc octet với công thức Lewis như sau:
∶N≡N∶
2. Tính chất cơ bản
a) Tính kém hoạt động hóa học (tính trơ) ở nhiệt độ thấp
- Liên kết ba giữa hai nguyên tử N trong phân tử nitrogen có năng lượng liên kết rất lớn (946 kJ mol-1) nên rất khó bị phá vỡ.
- Vì vậy, ở nhiệt độ và áp suất thường, nitrogen rất khó tham gia các phản ứng hóa học. Đặc điểm này được gọi là tính kém hoạt động hóa học hay tính trơ của đơn chất nitrogen.
b) Tính hoạt động hóa học ở nhiệt độ cao
- Phản ứng nitrogen và hydrogen diễn ra thuận nghịch, được thực hiện ở điều kiện nhiệt độ và áp suất khá cao cùng với chất xúc tác là bột sắt.
$N_{2}(g)+3H_{2}(g)\overset{t^{o},p,xt}{\rightleftharpoons }2NH_{3}(g)$
- Nitrogen phản ứng với oxygen ở nhiệt độ rất cao, khoảng 3000°C, tạo ra nitrogen monoxide (NO).
$N_{2}(g)+O_{2}(g)\overset{t^{o}}{\rightleftharpoons }2NO(g)$
- Trong khí quyển, phản ứng này chính là sự khởi đầu cho quá trình tạo thanh ion nitrate ($NO_{3}^{-}$), được coi là một nguồn cung cấp đạm cho đất.
c) Tính hoạt động hóa học ở nhiệt độ cao
- Nitrogen monoxide được tạo thành từ nitrogen và oxygen khi có sấm sét.

Tiếp theo là quá trình nitrogen dioxide chuyển thành acid trong nước mưa,
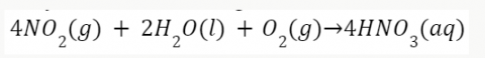
- Nước mưa có nồng độ acid phù hợp sẽ giúp cung cấp đạm cho đất ở dạng ion nitrate cần thiết cho cây trồng.
3. Ứng dụng
- Mỗi năm có hàng trăm triệu tấn nitrogen được sản xuất trên toàn cầu.
- Người ta thường dùng khí nitrogen để thay thế hoàn toàn hoặc một phần không khí trong rất nhiều trường hợp khác nhau để giảm nguy cơ cháy nổ.
- Nitrogen hóa lỏng ở nhiệt động thấp, -196°C. Vì vậy, nitrogen lỏng được sử dụng để làm lạnh nhanh, bảo quản thực phẩm,…
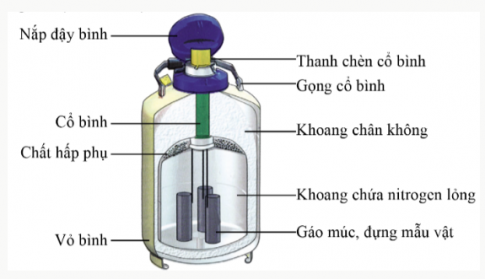
- Trong lĩnh vực sinh học và y học, các mẫu vật sinh học được bảo quản trong bình nitrogen lỏng.
Nội dung quan tâm khác
Giải bài tập những môn khác
Giải sgk lớp 11 kết nối tri thức
Giải sgk lớp 11 chân trời sáng tạo
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều
Bình luận